
ΓΨΧβΡΩΓΩΔώ.άϊ”ΟΚœ≥…ΤχΘ®÷ς“Σ≥…Ζ÷ΈΣCOΓΔCO2ΚΆH2Θ©‘Ύ¥ΏΜ·ΦΝΒΡΉς”Οœ¬Κœ≥…ΦΉ¥ΦΘ§ΖΔ…ζΒΡ÷ςΖ¥”Π»γœ¬ΘΚ
ΔΌCO2(g)+3H2(g)![]() CH3OHΘ®gΘ©+H2O(g) ΓςH1ΘΜ
CH3OHΘ®gΘ©+H2O(g) ΓςH1ΘΜ
ΔΎCO(g)+2H2(g)![]() CH3OH(g) ΓςH2
CH3OH(g) ΓςH2
ΔέCO2(g)+H2(g)![]() CO(g)+H2O(g) ΓςH3ΘΜ
CO(g)+H2O(g) ΓςH3ΘΜ
Μ·―ßΦϋ | H-H | C-O | C | H-O | C-H |
E/Θ®kJΓΛmol-1Θ© | 436 | 343 | 1076 | 465 | X |
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)“―÷ΣΓςH2=-99 kJΓΛmol-1Θ§‘ρΗυΨί…œ±μœύΙΊΒΡΜ·―ßΦϋΦϋΡήΘ®ΓΑC![]() OΓ±±μ ΨCOΒΡΜ·―ßΦϋΘ©ΦΤΥψX=_______ kJΓΛmol-1ΓΘ
OΓ±±μ ΨCOΒΡΜ·―ßΦϋΘ©ΦΤΥψX=_______ kJΓΛmol-1ΓΘ
(2)Ζ¥”ΠΔΌΓΔΔΎΓΔΔέΕ‘”ΠΒΡΤΫΚβ≥Θ ΐK1ΓΔK2ΓΔK3÷°ΦδΒΡΙΊœΒ ΫΈΣ___________ΓΘ
(3)ΗυΨίΜ·―ßΖ¥”Π‘≠άμΘ§Ζ÷Έω‘ω¥σ―Ι«ΩΕ‘Ζ¥”ΠΔέΒΡ”ΑœλΈΣ_______________ΓΘΘ®Χα ΨΘΚ¥”Ε‘Ζ¥”ΠΥΌ¬ ΓΔΤΫΚβΉ¥Χ§ΓΔΉΣΜ·¬ Ϋ«Ε»ΜΊ¥πΘ©
Δρ.«εΫύΡή‘¥ΨΏ”–ΙψάΪΒΡΩΣΖΔΚΆ”Π”Ο«ΑΨΑΘ§Ω…Φθ–ΓΈέ»ΨΫβΨωΈμω≤Έ ΧβΘ§Τδ÷–ΦΉ¥ΦΓΔΦΉΆι «”≈÷ ΒΡ«εΫύ»ΦΝœΘ§Ω…÷ΤΉς»ΦΝœΒγ≥ΊΓΘ“ΜΕ®ΧθΦΰœ¬”ΟCOΚΆH2Κœ≥…CH3OHΘΚCOΘ®gΘ©+2H2Θ®gΘ©![]() CH3OHΘ®gΘ©ΓςH=-99kJmol-1ΓΘœρΧεΜΐΈΣ2LΒΡΟή±’»ίΤς÷–≥δ»κ2molCOΚΆ4molH2Θ§≤βΒΟ≤ΜΆ§Έ¬Ε»œ¬»ίΤςΡΎΒΡ―Ι«ΩΘ®PΘΚkPaΘ©Υφ ±ΦδΘ®minΘ©ΒΡ±δΜ·ΙΊœΒ»γΆΦ÷–ΔώΓΔΔρΓΔΔσ«ζœΏΥυ ΨΘΚ
CH3OHΘ®gΘ©ΓςH=-99kJmol-1ΓΘœρΧεΜΐΈΣ2LΒΡΟή±’»ίΤς÷–≥δ»κ2molCOΚΆ4molH2Θ§≤βΒΟ≤ΜΆ§Έ¬Ε»œ¬»ίΤςΡΎΒΡ―Ι«ΩΘ®PΘΚkPaΘ©Υφ ±ΦδΘ®minΘ©ΒΡ±δΜ·ΙΊœΒ»γΆΦ÷–ΔώΓΔΔρΓΔΔσ«ζœΏΥυ ΨΘΚ

ΔΌΔρΚΆΔώœύ±»Θ§ΗΡ±δΒΡΖ¥”ΠΧθΦΰ «_________ΘΜ
ΔΎΖ¥”ΠΔώ‘Ύ6min ±¥οΒΫΤΫΚβΘ§‘Ύ¥ΥΧθΦΰœ¬¥”Ζ¥”ΠΩΣ ΦΒΫ¥οΒΫΤΫΚβ ±vΘ®CH3OHΘ©=_____ΘΜ
ΔέΖ¥”ΠΔρ‘Ύ2min ±¥οΒΫΤΫΚβΘ§ΤΫΚβ≥Θ ΐKΘ®ΔρΘ©=_________ΘΜ
Δή±»ΫœΖ¥”ΠΔώΒΡΈ¬Ε»Θ®T1Θ©ΚΆΖ¥”ΠΔσΒΡΈ¬Ε»Θ®T3Θ©ΒΡΗΏΒΆΘΚT1_____T3Θ®ΧνΓΑΘΨΓ±ΓΑΘΦΓ±ΓΑ=Γ±Θ©
ΓΨ¥πΑΗΓΩ413 K1=K2ΓΛK3Θ®Μρ’ΏK3=K1/K2Θ© ‘ω¥σ―Ι«ΩΘ§Ζ¥”ΠΥΌ¬ Φ”ΩλΘ§ΤΫΚβ≤Μ“ΤΕ·Θ§Ζ¥”ΠΈοΒΡΉΣΜ·¬ ≤Μ±δ Ι”Ο¥ΏΜ·ΦΝ 0.125 mol/Θ®LΓΛminΘ© 12 ΘΨ
ΓΨΫβΈωΓΩ
Θ®1Θ©”…ΔΎCO(g)+2H2(g)![]() CH3OH(g) ΓςH2=-99 kJΓΛmol-1Θ§‘ρΗυΨί±μ÷–œύΙΊΒΡΜ·―ßΦϋΦϋΡήΩ…÷ΣΘΚ1076+2ΓΝ436-3X-343-465=-99Θ§ΫβΒΟX=+413ΘΜ
CH3OH(g) ΓςH2=-99 kJΓΛmol-1Θ§‘ρΗυΨί±μ÷–œύΙΊΒΡΜ·―ßΦϋΦϋΡήΩ…÷ΣΘΚ1076+2ΓΝ436-3X-343-465=-99Θ§ΫβΒΟX=+413ΘΜ
(2)”…ΔΌCO2(g)+3H2(g)![]() CH3OHΘ®gΘ©+H2O(g) Ω…÷ΣΘΚK1=
CH3OHΘ®gΘ©+H2O(g) Ω…÷ΣΘΚK1=
ΔΎCO(g)+2H2(g)![]() CH3OH(g) Ω…÷ΣΘΚK2=
CH3OH(g) Ω…÷ΣΘΚK2=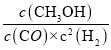
ΔέCO2(g)+H2(g)![]() CO(g)+H2O(g) Ω…÷ΣΘΚK3==
CO(g)+H2O(g) Ω…÷ΣΘΚK3==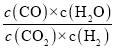
K2![]() K3=
K3= =K1Θ§Υυ“‘Ζ¥”ΠΔΌΓΔΔΎΓΔΔέΕ‘”ΠΒΡΤΫΚβ≥Θ ΐK1ΓΔK2ΓΔK3÷°ΦδΒΡΙΊœΒ ΫΈΣK1=K2
=K1Θ§Υυ“‘Ζ¥”ΠΔΌΓΔΔΎΓΔΔέΕ‘”ΠΒΡΤΫΚβ≥Θ ΐK1ΓΔK2ΓΔK3÷°ΦδΒΡΙΊœΒ ΫΈΣK1=K2![]() K3ΘΜ
K3ΘΜ
(3)ΗυΨίΖ¥”Π ΔέCO2(g)+H2(g)![]() CO(g)+H2O(g) ΓςH3Ω…÷ΣΘ§Ζ¥”Π«ΑΚσΜ·―ßΦΤΝΩ ΐœύΒ»ΒΡΤχΧεΖ¥”ΠΘ§‘ω¥σ―Ι«ΩΜ·―ßΖ¥”ΠΥΌ¬ ‘ωΦ”Θ§Μ·―ßΤΫΚβ≤Μ“ΤΕ·Θ§ΤΫΚβΉΣΜ·¬ ≤Μ±δΘΜ¥πΑΗΘΚ‘ω¥σ―Ι«ΩΘ§Ζ¥”ΠΥΌ¬ Φ”ΩλΘ§ΤΫΚβ≤Μ“ΤΕ·Θ§Ζ¥”ΠΈοΒΡΉΣΜ·¬ ≤Μ±δΘΜ
CO(g)+H2O(g) ΓςH3Ω…÷ΣΘ§Ζ¥”Π«ΑΚσΜ·―ßΦΤΝΩ ΐœύΒ»ΒΡΤχΧεΖ¥”ΠΘ§‘ω¥σ―Ι«ΩΜ·―ßΖ¥”ΠΥΌ¬ ‘ωΦ”Θ§Μ·―ßΤΫΚβ≤Μ“ΤΕ·Θ§ΤΫΚβΉΣΜ·¬ ≤Μ±δΘΜ¥πΑΗΘΚ‘ω¥σ―Ι«ΩΘ§Ζ¥”ΠΥΌ¬ Φ”ΩλΘ§ΤΫΚβ≤Μ“ΤΕ·Θ§Ζ¥”ΠΈοΒΡΉΣΜ·¬ ≤Μ±δΘΜ
Δρ.ΔΌ”…CO(g)+2H2(g)![]() CH3OH(g)ΓςH=-99kJmol-1ΚΆΆΦœώΩ…÷ΣΘ§ΔρΚΆΔώ¥οΒΫΤΫΚβΉ¥Χ§ ±―Ι«ΩœύΒ»Θ§ΒΪΔρ±»Δώœ»¥οΒΫΤΫΚβΉ¥Χ§Θ§Υυ“‘ΗΡ±δΒΡΖ¥”ΠΧθΦΰ”Π « Ι”ΟΝΥ¥ΏΜ·ΦΝΘΜ¥πΑΗΘΚ Ι”Ο¥ΏΜ·ΦΝΘΜ
CH3OH(g)ΓςH=-99kJmol-1ΚΆΆΦœώΩ…÷ΣΘ§ΔρΚΆΔώ¥οΒΫΤΫΚβΉ¥Χ§ ±―Ι«ΩœύΒ»Θ§ΒΪΔρ±»Δώœ»¥οΒΫΤΫΚβΉ¥Χ§Θ§Υυ“‘ΗΡ±δΒΡΖ¥”ΠΧθΦΰ”Π « Ι”ΟΝΥ¥ΏΜ·ΦΝΘΜ¥πΑΗΘΚ Ι”Ο¥ΏΜ·ΦΝΘΜ
ΔΎΗυΨί»ΐΕΈ ΫΘΚ
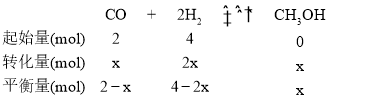
ΗυΨίΆΦœώΤπ Φ ±―Ι«ΩΈΣΈΣΤΫΚβ ±―Ι«ΩΒΡ2±ΕΘ§Φ¥![]() =
=![]() Θ§ΫβΒΟx=15Θ§‘ρΖ¥”ΠΔώ‘Ύ6min ±¥οΒΫΤΫΚβ ±v(CH3OH)=
Θ§ΫβΒΟx=15Θ§‘ρΖ¥”ΠΔώ‘Ύ6min ±¥οΒΫΤΫΚβ ±v(CH3OH)=![]() =0.125 mol/(LΓΛminΘ©ΘΜ
=0.125 mol/(LΓΛminΘ©ΘΜ
ΔέΖ¥”ΠΔρ‘Ύ2min ±¥οΒΫΤΫΚβΘ§ΗυΨί…œ ωΖ÷ΈωΩ…÷ΣΤΫΚβ ±c(CH3OH)=![]() =0.75 mol/LΘ§c(CO)=
=0.75 mol/Lȧc(CO)=![]() =0.25 mol/Lȧc(H2)=
=0.25 mol/LΘ§c(H2)=![]() =0.5 mol/LΘ§”…CO(g)+2H2(g)
=0.5 mol/LΘ§”…CO(g)+2H2(g)![]() CH3OH(g)÷ΣK=
CH3OH(g)÷ΣK=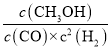 =
=![]() =12ΘΜ¥πΑΗΘΚ12ΘΜ
=12ΘΜ¥πΑΗΘΚ12ΘΜ
Δή”…CO(g)+2H2(g)![]() CH3OH(g)ΚΆΆΦœώΩ…÷ΣΘ§¥οΒΫΤΫΚβΚσΔσΒΡ―Ι«Ω–Γ”ΎΔώΘ§ΥΒΟςΤΫΚβ’ΐœρ“ΤΕ·Θ§“ρΈΣ «Ζ≈»»Ζ¥”ΠΘ§Υυ“‘T1ΘΨT3ΓΘ
CH3OH(g)ΚΆΆΦœώΩ…÷ΣΘ§¥οΒΫΤΫΚβΚσΔσΒΡ―Ι«Ω–Γ”ΎΔώΘ§ΥΒΟςΤΫΚβ’ΐœρ“ΤΕ·Θ§“ρΈΣ «Ζ≈»»Ζ¥”ΠΘ§Υυ“‘T1ΘΨT3ΓΘ


 ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ
ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ –Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
–Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ298K ±Θ§‘Ύ20.0mL0.10molΓΛL-1¬»Υ°÷–ΒΈ»κ0.10molΓΛL-1ΒΡ―ΈΥαΘ§»ή“ΚΒΡpH”κΥυΦ”―ΈΥαΒΡΧεΜΐΙΊœΒ»γΆΦΥυ ΨΓΘΦΚ÷Σ0.10molΓΛL-1Α±Υ°ΒΡΒγάκΕ»ΈΣ1.32%Θ§œ¬Ν–”–ΙΊ–π ω’ΐ»ΖΒΡ «

A. ΗΟΒΈΕ®Ιΐ≥Χ”ΠΗΟ―Γ‘ώΖ”ΧΣΉςΈΣ÷Η ΨΦΝ
B. MΒψΕ‘”ΠΒΡ―ΈΥαΧεΜΐΈΣ20.0mL
C. MΒψ¥ΠΒΡ»ή“Κ÷–c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. NΒψ¥ΠΒΡ»ή“Κ÷–pHΘΦ12
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩCl2 «“Μ÷÷÷Ί“ΣΒΡΜ·ΙΛ‘≠ΝœΘ§“≤ «“Μ÷÷ΨγΕΨΤχΧεΓΘΡ≥Μ·―ß–Υ»Λ–ΓΉι÷Τ±ΗCl2≤ΔΧΫΨΩCl2œύΙΊ–‘÷ ΒΡΙΐ≥Χ»γœ¬ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)¬»ΤχΒΡ÷Τ±Η
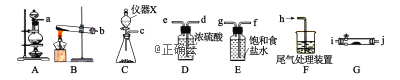
ΔΌ…œΆΦ÷–“«ΤςXΒΡΟϊ≥Τ «_________________Θ§»τ”ΟKMnO4ΚΆ≈®HClΖ¥”Π÷Τ±ΗCl2‘ρΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ_______________________________________________________ΘΜ
ΔΎ”ϊ”ΟΕΰ―θΜ·ΟΧΚΆ≈®―ΈΥα÷Τ±Η¥ΩΨΜΗ…‘οΒΡCl2Θ§“«ΤςΫ”ΩΎΒΡΝ§Ϋ”Υ≥–ρΈΣ_______________ΘΜΘ®ΗυΨίΤχΝςΖΫœρΘ§Α¥’’–Γ–¥Ή÷ΡΗΥ≥–ρΧν–¥Θ©ΓΘ
(2)÷Τ±ΗΒΡ¬»Τχ”κFeΖέ‘Ύ”≤÷ ≤ΘΝßΙήG÷–ΒΡΖ¥”ΠΘ§–η≤…»Γ________Ζ¥”ΠΧθΦΰΘ§ΫΪΖ¥”ΠΚσΒΡ”≤÷ ≤ΘΝßΙή÷–ΙΧΧε»ή”ΎœΓ―ΈΥαΘ§»Γ…ΌΝΩ»ήΫβΚσΒΡ»ή“ΚΘ§Φλ≤βΤδ÷–Ϋπ τ―τάκΉ”÷÷άύΘΚ
Β―ι±ύΚ≈ | Β―ι≤ΌΉς | Β―ιœ÷œσ | Β―ιΫα¬έ |
ΔΌ | »Γ…ΌΝΩ¥ΐ≤β“ΚΘ§ΒΈΦ”______»ή“Κ | ____________ | Κ§”–Fe2+ |
ΔΎ | »Γ…ΌΝΩ¥ΐ≤β“ΚΘ§ΒΈΦ”______»ή“Κ | ____________ | Κ§”–Fe3+ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΚ§”–Ζ”άύΈο÷ ΒΡΖœΥ°ά¥‘¥ΙψΖΚΘ§ΈΘΚΠΫœ¥σΓΘΚ§Ζ”ΖœΥ°≤ΜΨ≠¥Πάμ≈≈»κΥ°ΧεΘ§ΜαΈΘΚΠΥ°…ζ…ζΈοΒΡΖ±÷≥ΚΆ…ζ¥φΘΜ“ϊ”ΟΥ°Κ§Ζ”Θ§Μα”Αœλ»ΥΧεΫΓΩΒΓΘΡ≥ΩΤ―–ΫαΙΙ―–ΨΩ≥ω“Μ÷÷ΗΏ–ßΙβ¥ΏΜ·ΦΝBMOΘ®Bi2MoO6)Θ§Ω…”Ο”ΎΙβ¥ΏΜ·ΫΒΫβΕΓΜυΖ”Θ§‘≠άμ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ® Θ©
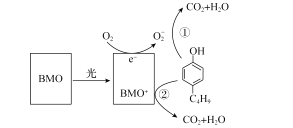
A.Ιβ¥ΏΜ·ΦΝBMOΩ…ΫΒΒΆΕΓΜυΖ”―θΜ·Ζ¥”ΠΒΡΠΛH
B.‘ΎΕΓΜυΖ”―θΜ·Ιΐ≥Χ÷–BMO±μœ÷≥ω«ΩΜΙ‘≠–‘
C.±ΫΜΖ…œΝ§”–“ΜOHΚΆ“ΜC4H9ΒΡΆ§Ζ÷“λΙΙΧεΙ≤”–12÷÷Θ®≤ΜΩΦ¬«ΝΔΧε“λΙΙΘ©
D.Ζ¥”Π÷–BMO≤Έ”κΖ¥”ΠΙΐ≥Χ«“Ω…“‘―≠ΜΖάϊ”Ο
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΆΦ Ψ”κΕ‘”ΠΒΡ–π ω¥μΈσΒΡ «

A. ΆΦΦΉ±μ ΨΖ÷±π”ΟNaOH»ή“ΚΒΈΕ®Β»≈®Ε»Β»ΧεΜΐΒΡ―ΈΥαΚΆ¥ΉΥα»ή“ΚΖ¥”Π±δΜ·«ζœΏΘ§÷Η ΨΦΝΕΦΩ…”ΟΖ”ΧΣ
B. ΆΦ““±μ ΨΖ÷±π”ΟΒ»≈®Ε»AgNO3»ή“ΚΒΈΕ®Β»≈®Ε»Β»ΧεΜΐΒΡNaClΓΔNaBrΦΑNaI»ή“ΚΖ¥”Π±δΜ·«ζœΏ(X-±μ ΨCl-ΓΔBr-ΓΔI-)Θ§‘ρcΈΣI®C(»ήΕ»Μΐ≥Θ ΐΘΚKsp(AgI)ΘΦKsp(AgBr)ΘΦKsp(AgCl))
C. ΆΦ±ϊ±μ Ψ“ΜΕ®Έ¬Ε»œ¬Θ§Υ°»ή“Κ÷–HΘΪΚΆOHΘ≠ΒΡ≈®Ε»±δΜ·«ζœΏΘ§bΓζaΩ…Ρή «Φ”CuCl2»ή“ΚΒΦ÷¬ΒΡ
D. ΆΦΕΓ±μ ΨΤδΥϊΧθΦΰ≤Μ±δ ±Θ§Ω…ΡφΖ¥”ΠA(g)+3B(g) ![]() 2C(g) ΠΛHΘΦ0 Θ§ CΒΡΈο÷ ΒΡΝΩΖ÷ ΐ”κΈ¬Ε»ΒΡΙΊœΒ
2C(g) ΠΛHΘΦ0 Θ§ CΒΡΈο÷ ΒΡΝΩΖ÷ ΐ”κΈ¬Ε»ΒΡΙΊœΒ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΧΦΚΆΧΦΒΡΜ·ΚœΈο‘Ύ…ζ≤ζΓΔ…ζΜν÷–ΒΡ”Π”ΟΖ«≥ΘΙψΖΚΘ§‘ΎΧα≥ΪΫΓΩΒ…ζΜν“―≥…≥±ΝςΒΡΫώΧλΘ§ΓΑΒΆΧΦ…ζΜνΓ±≤Μ‘Ό÷Μ «“Μ÷÷άμœκΘ§Ηϋ «“Μ÷÷÷ΒΒΟΤΎ¥ΐΒΡ–¬ΒΡ…ζΜνΖΫ ΫΓΘ
(1)ΦΉΆι»Φ…’Ζ≈≥ω¥σΝΩΒΡ»»Θ§Ω…ΉςΈΣΡή‘¥”Ο”Ύ»ΥάύΒΡ…ζ≤ζΚΆ…ζΜνΓΘ
“―÷ΣΘΚΔΌ2CH4(g)+3O2(g)=2CO(g)+4H2O(l) ΓςH=ΓΣ1214 kJ/mol
ΔΎ2CO(g)+O2(g)=2CO2(g) ΓςH= ΓΣ566kJ/mol
‘ρ±μ ΨΦΉΆι»Φ…’»»ΒΡ»»Μ·―ßΖΫ≥Χ Ϋ_______________________ΓΘ
(2)…ζ≤ζΦΉ¥ΦΒΡ‘≠ΝœCOΚΆH2ά¥‘¥”ΎΘΚCH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
ΔΌ“ΜΕ®ΧθΦΰœ¬CH4ΒΡΤΫΚβΉΣΜ·¬ ”κΈ¬Ε»ΓΔ―Ι«ΩΒΡΙΊœΒ»γΆΦΘ§‘ρPl_______P2ΘΜAΓΔBΓΔC»ΐΒψ¥ΠΕ‘”ΠΤΫΚβ≥Θ ΐ(KAΓΔKBΓΔKC)ΒΡ¥σ–ΓΥ≥–ρΈΣ___________(ΧνΓΑΘΦΓ±ΓΔΓΑΘΨΓ±ΓΑ=Γ±)ΓΘ
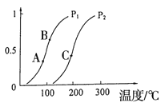
ΔΎ100Γφ ±Θ§ΫΪ1mol CH4ΚΆ2mol H2OΆ®»κ»ίΜΐΈΣ10LΒΡΖ¥”Π “Θ§Ζ¥”Π¥οΤΫΚβΒΡ±ξ÷Ψ «ΘΚ_______ΓΘ
aΘ°»ίΤςΒΡ―Ι«ΩΚψΕ®
bΘ°ΒΞΈΜ ±ΦδΡΎœϊΚΡ0.1mol CH4Ά§ ±…ζ≥…0.3mol H2
cΘ°»ίΤςΡΎΤχΧεΟήΕ»ΚψΕ®
dΘ°3v(CH4)=v(H2)
e. »ίΤςΡΎΤχΧεΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩΚψΕ®
(3)“―÷Σ2H2(g)+CO(g)![]() CH3OH(g)ΓςH=-akJmol-1(aΘΨ0)Θ§‘Ύ“ΜΗω»ίΜΐΙΧΕ®ΒΡ»ίΤς÷–Φ”»κ2mol H2ΚΆ1mol COΘ§‘Ύ500Γφ ±≥δΖ÷Ζ¥”ΠΘ§¥οΤΫΚβΚσCH3OHΒΡ≈®Ε»ΈΣW molL-1ΓΘΖ¥”ΠΤΫΚβΚσΘ§»τœρ‘≠ά¥»ίΤς÷–‘ΌΦ”»κ2mol H2ΚΆ1mol COΘ§500Γφ≥δΖ÷Ζ¥”Π‘Ό¥Έ¥οΤΫΚβΚσΘ§‘ρCH3OH≈®Ε»___________2WmolL-1(ΧνΓΑΘΨΓ±ΓΔΓΑΘΦΓ±ΜρΓΑ=Γ±)ΓΘ
CH3OH(g)ΓςH=-akJmol-1(aΘΨ0)Θ§‘Ύ“ΜΗω»ίΜΐΙΧΕ®ΒΡ»ίΤς÷–Φ”»κ2mol H2ΚΆ1mol COΘ§‘Ύ500Γφ ±≥δΖ÷Ζ¥”ΠΘ§¥οΤΫΚβΚσCH3OHΒΡ≈®Ε»ΈΣW molL-1ΓΘΖ¥”ΠΤΫΚβΚσΘ§»τœρ‘≠ά¥»ίΤς÷–‘ΌΦ”»κ2mol H2ΚΆ1mol COΘ§500Γφ≥δΖ÷Ζ¥”Π‘Ό¥Έ¥οΤΫΚβΚσΘ§‘ρCH3OH≈®Ε»___________2WmolL-1(ΧνΓΑΘΨΓ±ΓΔΓΑΘΦΓ±ΜρΓΑ=Γ±)ΓΘ
(4)Ρ≥ Β―ι–ΓΉιάϊ”ΟCO(g)ΓΔO2(g)ΓΔKOH(aq)…ηΦΤ≥…»γΆΦΥυ ΨΒΡΒγ≥ΊΉΑ÷ΟΘ§
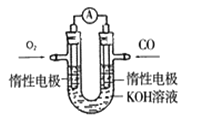
ΔΌΗΚΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ___________ΓΘ
ΔΎ”ΟΗΟ‘≠Βγ≥ΊΉωΒγ‘¥Θ§”ΟΕη–‘ΒγΦΪΒγΫβ200mL±ΞΚΆ ≥―ΈΥ°(ΉψΝΩ)Θ§œϊΚΡ±ξΉΦΉ¥Ωωœ¬ΒΡCO 224mLΘ§‘ρ»ή“ΚΒΡpH=___________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ«ζΟάΧφΡα «“Μ÷÷“÷÷ΤΚΎ…ΪΥΊΝωΒΡ–¬–ΆΩΙΑ©“©ΈοΘ§œ¬Οφ «Κœ≥…«ζΟάΧφΡα÷–ΦδΧεGΒΡΖ¥”Π¬ΖœΏΘΚ
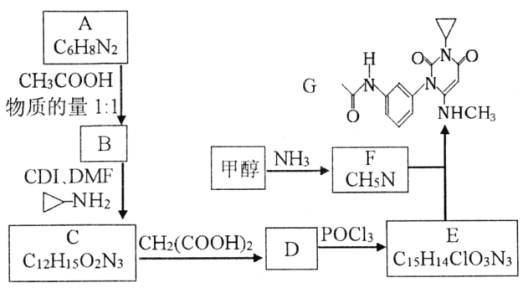
“―÷ΣΘΚΔΌDΖ÷Ή”÷–”–2Ηω6‘ΣΜΖΘΜ
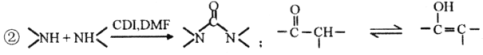
«κΜΊ¥πΘΚ
Θ®1Θ©Μ·ΚœΈοAΒΡΫαΙΙΦρ Ϋ___________ΓΘA…ζ≥…BΒΡΖ¥”Πάύ–Ά___________ΓΘ
Θ®2Θ©œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «___________ΓΘ
A.BΦ»Ρή±μœ÷Φν–‘”÷Ρή±μœ÷Υα–‘
B.1moC‘ΎΦν»ή“Κ÷–Άξ»ΪΥ°ΫβΉνΕύΩ…“‘œϊΚΡ4 molOHΘ≠
C.D”κPOCl3ΒΡΖ¥”ΠΜΙΜα…ζ≥…EΒΡ“Μ÷÷Ά§Ζ÷“λΙΙΧε
D.GΒΡΖ÷Ή” ΫΈΣC16H18O3N4
Θ®3Θ©–¥≥ωCΓζDΒΡΜ·―ßΖΫ≥Χ Ϋ____________________________________________ΓΘ
Θ®4Θ©X «±»AΕύ2ΗωΧΦ‘≠Ή”ΒΡAΒΡΆ§œΒΈοΘ§–¥≥ωΖϊΚœœ¬Ν–ΧθΦΰΒΡXΩ…ΡήΒΡΫαΙΙΦρ ΫΘΚ_______________________________________________________ΓΘ
ΔΌ1H-NMRΤΉœ‘ ΨΖ÷Ή”÷–”–3÷÷«β‘≠Ή”Θ§ΔΎIRΤΉœ‘ ΨΖ÷Ή”÷–”–±ΫΜΖ”κΘ≠NH2œύΝ§ΫαΙΙ
Θ®5Θ©Νς≥Χ÷– Ι”ΟΒΡDMFΦ¥NΘ§N-ΕΰΦΉΜυΦΉθΘΑΖΫαΙΙΦρ ΫΈΣ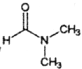 Θ§ «≥Θ”ΟΒΡ”–Μζ»ήΦΝΓΘ…ηΦΤ“‘ΦΉ¥ΦΚΆΑ±ΈΣ÷ς“Σ‘≠Νœ÷Τ»ΓDMFΒΡΚœ≥…¬ΖœΏ(”ΟΝς≥ΧΆΦ±μ ΨΘ§ΤδΥϊΈόΜζ ‘ΦΝ»Έ―Γ)ΓΘ_____________
Θ§ «≥Θ”ΟΒΡ”–Μζ»ήΦΝΓΘ…ηΦΤ“‘ΦΉ¥ΦΚΆΑ±ΈΣ÷ς“Σ‘≠Νœ÷Τ»ΓDMFΒΡΚœ≥…¬ΖœΏ(”ΟΝς≥ΧΆΦ±μ ΨΘ§ΤδΥϊΈόΜζ ‘ΦΝ»Έ―Γ)ΓΘ_____________
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ―θΜ·–ΩΈΣΑΉ…ΪΖέΡ©Θ§Ω…”Ο”Ύ Σ’νΓΔ―ΔΒ»ΤΛΖτ≤ΓΒΡ÷ΈΝΤΓΘΙΛ“ΒZnO÷–Κ§”–Fe(Δρ)ΓΔMn(Δρ)ΓΔNi(Δρ)Θ§¥ΩΜ·ΙΛ“ΒZnOΒΡΝς≥Χ»γœ¬ΘΚ

Χα ΨΘΚ‘Ύ±Ψ Β―ιΧθΦΰœ¬Θ§Ni(Δρ)≤ΜΡή±Μ―θΜ·ΓΘ
Θ®1Θ©ΓΑΥαΫΰΓ± ±–η≤ΜΕœΆ®»κσ{Έ¬Υ°’τΤχΘ§ΤδΡΩΒΡ « ________________ΓΘ
Θ®2Θ©ΓΑ≥ΐ‘”IΓ±÷–…ζ≥…FeΘ®OHΘ©3Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ______________________________ΓΘ
Θ®3Θ©ΓΑ≥ΐ‘”2Γ±÷–ΥυΒΟ¬Υ‘ϋ÷ς“Σ≥…Ζ÷ «____________ΓΘ
Θ®4Θ©¬Υ±ΐ“Σ”ΟΥ°œ¥Θ§Φλ―ι «Ζώœ¥Β”Η…ΨΜΒΡΖΫΖ® «_________________ΓΘ
Θ®5Θ©“―÷ΣΘΚZnΘ®OHΘ©2 ΒΡ Ksp=lΓΝ10-17ΓΘ “Έ¬œ¬ΈΣ ΙZn2+Άξ»Ϊ≥ΝΒμ(Τδ≈®Ε»<1ΓΝ10-5molΓΛL-1)Θ§–ηΒςΫΎ»ή“ΚpHΖΕΈßΈΣ____________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ―«œθθΘ¬»(NOCl) «”–ΜζΈοΚœ≥…÷–ΒΡ÷Ί“Σ ‘ΦΝΘ§ΈΣΚλΚ÷…Ϊ“ΚΧεΜρΜΤ…ΪΤχΧεΘ§ΨΏ”–¥Χ±«Εώ≥τΈΕΘ§”ωΥ°Ζ¥”Π…ζ≥…“Μ÷÷Ν“Μ·ΈοΚΆΝΫ÷÷―θΜ·ΈοΓΘΡ≥―ßœΑ–ΓΉι‘Ύ Β―ι”ΟC12ΚΆNO÷Τ±ΗNOCl≤Δ≤βΕ®Τδ¥ΩΕ»Θ§œύΙΊ Β―ι(ΉΑ÷Ο¬‘»Ξ)»γœ¬ΓΘ«κΜΊ¥π:
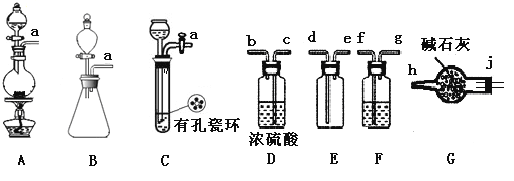
(1)÷Τ±ΗCl2ΖΔ…ζΉΑ÷ΟΩ…______ (Χν¥σ–¥Ή÷ΡΗ)Θ§Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_______ΓΘ
(2)”ϊ ’Φ·“ΜΤΩΗ…‘οΒΡ¬»ΤχΘ§―Γ‘ώΉΑ÷ΟΘ§ΤδΝ§Ϋ”Υ≥–ρΈΣ:aΓζ________(Α¥ΤχΝςΖΫœρΘ§”Ο–Γ–¥Ή÷ΡΗ±μ Ψ)Θ§»τ”ΟΒΫFΘ§Τδ ΔΉΑ“©ΤΖΈΣ_________ΓΘ
(3) Β―ι “Ω…”Οœ¬ΆΦΉΑ÷Ο÷Τ±Η―«œθθΘ¬»(NOCl)
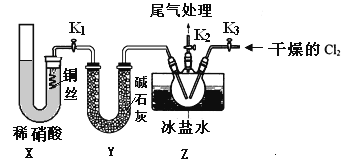
ΔΌ Β―ι ““≤Ω…”ΟBΉΑ÷Ο÷Τ±ΗNOΘ§…œΆΦXΉΑ÷ΟΒΡ”≈ΒψΈΣ__________(÷Ν…Ό–¥≥ωΝΫΒψ)
ΔΎΦλ―ιΉΑ÷ΟΤχΟή–‘≤ΔΉΑ»κ“©ΤΖΘ§¥ρΩΣk2,»ΜΚσ‘Ό¥ρΩΣ____(ΧνΓΑk1Γ±ΜρΓΑk3Γ±)Θ§Ά®»κ“ΜΕΈ ±ΦδΤχΧεΘ§ΤδΡΩΒΡΈΣ________Θ§»ΜΚσΫχ––ΤδΥϊ≤ΌΉςΘ§Β±Z”–“ΜΕ®ΝΩ“ΚΧε…ζ≥… ±Θ§ΆΘ÷Ι Β―ιΓΘ
Δέ»τΈόΉΑ–ΛY,‘ρZ÷–NOClΩ…ΡήΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ_________
(4)»ΓZ÷–ΥυΒΟ“ΚΧεmg»ή”ΎΥ°Θ§≈δ÷Τ≥…250mL»ή“ΚΘ§»Γ≥ω25.00mL,“‘K2CrO4»ή“ΚΈΣ÷Η ΨΦΝΘ§”Οcmol/LAgNO3±ξΉΦ»ή“ΚΒΈΕ®÷Ν÷’ΒψΘ§œϊΚΡ±ξΉΦ»ή“ΚΒΡΧεΜΐΈΣ22.50mL.“―÷Σ:Ag2CrO4ΈΣΉ©Κλ…ΪΙΧΧε;Ksp(AgCl)=1.56ΓΝ10-10,Ksp(Ag2CrO4)=1ΓΝ10-12,‘ρ―«œθθΘ¬»(NOC1)ΒΡ÷ ΝΩΖ÷ ΐΈΣ____(”Ο¥ζ ΐ Ϋ±μ ΨΘ§≤Μ±ΊΜ·Φρ)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com