
【题目】联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为_______(已知:N2H4+H+![]() N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为 。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为 。
【答案】(4)8.7×10-7,N2H6(HSO4)2
【解析】
试题分析:
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,则联氨第一步电离的方程式为N2H4+H2O![]() N2H5++OH-,已知:N2H4+H+
N2H5++OH-,已知:N2H4+H+![]() N2H5+的K=8.7×107;KW=1.0×10-14,联氨第一步电离的平衡常数K=[c(N2H5+)×c(OH-)]÷c(N2H4)= [c(N2H5+)×c(OH-)×c(H+)]÷[c(N2H4)×c(H+)]=K×Kw=8.7×107×1.0×10-14=8.7×10-7 ;联氨为二元弱碱,酸碱发生中和反应生成盐,则联氨与硫酸形成酸式盐的化学式为N2H6(HSO4)2 。
N2H5+的K=8.7×107;KW=1.0×10-14,联氨第一步电离的平衡常数K=[c(N2H5+)×c(OH-)]÷c(N2H4)= [c(N2H5+)×c(OH-)×c(H+)]÷[c(N2H4)×c(H+)]=K×Kw=8.7×107×1.0×10-14=8.7×10-7 ;联氨为二元弱碱,酸碱发生中和反应生成盐,则联氨与硫酸形成酸式盐的化学式为N2H6(HSO4)2 。


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】将0.4gNaOH和1.06g![]() 混合并配成溶液,向溶液中滴加0.1mol·
混合并配成溶液,向溶液中滴加0.1mol·![]() 稀盐酸。下列图像能正确表示加入盐酸的体积和生成
稀盐酸。下列图像能正确表示加入盐酸的体积和生成![]() 的物质的量的关系的是( )
的物质的量的关系的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2016·银川模拟)工业上通常以铝土矿(主要成分为Al2O3,含有少量Fe2O3、SiO2等杂质)为原料制备无水氯化铝:2Al2O3+6Cl2![]() 4AlCl3+3O2。
4AlCl3+3O2。
(1)为促进反应的进行,实际生产中需加入焦炭,其原因是_____________________。
(2)加入焦炭后的化学反应可表示为Al2O3+C+Cl2AlCl3+X↑,设计实验确定气体X的__________________。
(3)在提纯AlCl3粗产品时,需加入少量铝粉,可使熔点较低的FeCl3转化为熔点较高的FeCl2,从而避免在AlCl3中混入铁的氯化物。该反应的化学方程式为________________________。
(4)以铝土矿为原料可以通过以下途径提纯氧化铝:

①写出滤液甲中溶质的化学式:___________________________。
②写出滤液乙中加入过量氨水得到Al(OH)3的离子方程式:__________________________。
③要进一步获得金属铝,工业上采用的冶炼方法是_______________,
有关反应的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届 江西省五市八校第二次联考】【化学——选修5:有机化学】
以有机物A为原料合成重要精细化工中间体TMBA(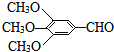 )和抗癫痫药物H(
)和抗癫痫药物H( )的路线如图(部分反应略去条件和试剂):
)的路线如图(部分反应略去条件和试剂):
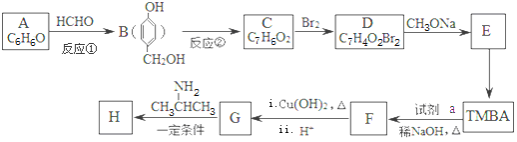
已知:I.RONa+R′X→ROR′+NaX;
II.RCHO+ R′CH2CHO ![]()
![]() +H2O(R、R′表示烃基或氢)
+H2O(R、R′表示烃基或氢)
(1)A的名称是 ;C能发生银镜反应,则C分子中含氧官能团的名称是 .
(2)①和②的反应类型分别是 、 .
(3)E的结构简式是 ,试剂a的分子式是 .
(4)C→D的化学方程式是 .
(5)D的同分异构体有多种,其中属于芳香族酯类化合物的共有 种.
(6)F与新制Cu(OH)2悬浊液发生反应的化学方程式是 .
(7)已知酰胺键(![]() )有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。
)有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为某种甲醇燃料电池示意图,工作时电子流向如图所示。下列判断正确的是
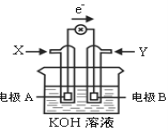
A.X为氧气
B.电极A反应式:CH3OH-6e-+H2O = CO2+6H+
C.B电极附近溶液pH增大
D.电池工作时,溶液中电子由电极B流向电极A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有SO42-、CO32-、Cl-。为了检验其中是否含有SO42-,除BaCl2溶液外,还需要的溶液是
A.H2SO4 B.HCl C.NaOH D.NaNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图依次为气体制得、除杂并检验其性质的装置(加热及夹持仪器省略)。下列设计不能达到目的的是( )
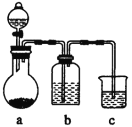
选项 | 气体 | 装置中药品 | ||
a | b | c | ||
A | C2H2 | 饱和食盐水+电石 | CuS04溶液 | 溴水 |
B | CO2 | 稀盐酸+石灰石 | 饱和NaHC03溶液 | 苯酚蚋溶液 |
C | C2H4 | 溴乙烷+ NaOH乙醇溶液 | 水 | K2z Cr207,酸性溶液 |
D | SO2 | 碳+浓硫酸 | 新制氯水 | 品红溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醇是重要的化工原料,又可做燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,主要反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2= -58 kJ/mol
CH3OH(g)+H2O(g) △H2= -58 kJ/mol
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
已知反应①中的相关的化学键键能数据如下:
化学键 | H-H | C-O | C (CO中的化学键) | H-O | C-H |
E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
回答下列问题:
①△H3=_____kJ/mol
②25℃,101 kPa条件下,测得16g甲醇完全燃烧释放出Q kJ的热量,请写出表示甲醇燃烧热的热化学方程式_______________
(2)25℃,将a mol·L-1氨水与b mol·L-1盐酸等体积混合后溶液呈中性,则此时溶液中c(NH4+)__________c(Cl-)(填“>”、“<”或“﹦”);用含a、b的代数式表示该温度下NH3·H2O的电离平衡常数Kb = _________
(3)800℃时,在2L密闭容器中发生反应2NO(g)+O2(g)![]() 2NO2(g),在反应体系中,n(NO)随时间的变化如下表所示:
2NO2(g),在反应体系中,n(NO)随时间的变化如下表所示:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①下图中表示NO2变化的曲线是___________用O2表示从0~2s内该反应的平均速率v=____
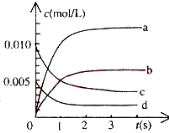
②能说明该反应已经达到平衡状态的是_______
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。
① 若加入锌粒,最终产生无色无味的气体;
② 若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是()
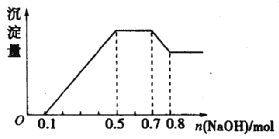
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中n(NH4+)=0.2mol
C.溶液中一定不含CO32-,可能含有SO42-和NO3-
D.n(H+):n(Al3+):n(Mg2+)=1:1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com