
【题目】19世纪中叶,俄国化学家门捷列夫对化学学科的巨大贡献是( )
A.提出了原子学说
B.提出了元素周期律
C.提出了分子学说
D.制定了科学的元素周期表
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
【题目】以含有Al2O3、Fe2O3等杂质的铬铁矿[主要成分为Fe(CrO2)2]为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O)的主要工艺流程如下:

己知:铬铁矿在空气中与纯减煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,
且 Al2O3+Na2CO3![]() 2NaAlO2+ CO2↑。请回答:
2NaAlO2+ CO2↑。请回答:
(1)在铬铁矿Fe(CrO2)2中,Cr的化合价为___________。
(2)滤渣2的成分为_____________。
(3)将滤渣1放入稀硫酸溶解后得溶液W,检验该溶液中金属离子的方法是_________。
(4)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol/L以下才能排放。含CrO42-的废水处理通常有以下两种方法。
①沉淀法:
加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于________________mol/L,后续废水处理方能达到国家排放标准。
②还原法:CrO42-![]() Cr3+
Cr3+![]() Cr(OH)3。写出酸性条件下CrO42-与绿巩在溶液中反应的离子方程式:_________________________________。
Cr(OH)3。写出酸性条件下CrO42-与绿巩在溶液中反应的离子方程式:_________________________________。
(5)某高效净水剂是由K2FeO4得到的,工业上以溶液w、次氯酸钾和氢氧化钾为原料制备K2FeO4,该反应的离子方程式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图是课外活动小组的同学设计的 4 个喷泉实验方案。下列有关操作不可能引发喷泉现象的是( )
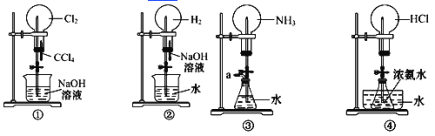
A.挤压装置①的胶头滴管使 CCl4。全部进入烧瓶,片刻后打开止水夹
B.挤压装置②的胶头滴管使 NaOH 溶液全部进入烧瓶,片刻后打开止水夹
C.用鼓气装置从装置③的 a 处不断鼓入空气并打开止水夹
D.向装置④的水槽中慢慢加入足量浓硫酸并打开止水夹
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有Ti3+的配合物 [TiCl(H2O)5]Cl2·H2O ,其中配离子[TiCl(H2O)5]2+中含有的化学键类型分别是
A. 离子键、配位键 B. 非极性共价键、配位键
C. 极性共价键、非极性共价键 D. 极性共价键、配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A.用惰性电极电解NaH2PO2溶液,其阳极反应式为:2H2O-4e-=O2↑+4H+
B.H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C.将H3PO2溶液加入到酸性重铬酸钾溶液中,H3PO2的还原产物可能为H3PO4
D.H3PO2溶于水时电离方程式为:H3PO2![]() H++H2PO22-
H++H2PO22-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(1)用不到的仪器 (填字母)
A.烧杯 |
B.托盘天平 |
C.量筒 |
D.胶头滴管 |
E.玻璃棒
F.500mL容量瓶;
(2)实验开始前需要检验容量瓶 ;
(3)需要量取浓硫酸的体积为 ;
(4)将量取的浓硫酸沿烧杯壁慢慢注入盛有适量水的烧杯中,并不断搅拌,然后________________;
(5)将上述烧杯中的硫酸溶液转移至容量瓶时,某实验小组同学操作的示意图如下。请你指出图中错误。_______________________;
(6)某实验小组其它操作均正确,但未用蒸馏水洗涤烧杯,则其所配制溶液的浓度 ;定容时若仰视刻度线,则所配制溶液的浓度____________(填“偏大”、“偏小”或“无影响”);
(7)溶液转移及洗涤完成后,应向容量瓶中直接加水到离刻度线下__________时,改用胶头滴管加水,使溶液的凹液面正好跟刻度线水平相切。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向一个容积不变的容器中,通入2mol SO2和2mol O2及固体催化剂,使之反应。2SO2(g)+O2(g)![]() 2SO3(g);ΔH=-196 KJ/mol。平衡时容器内气体压强为起始时的90%。此时
2SO3(g);ΔH=-196 KJ/mol。平衡时容器内气体压强为起始时的90%。此时
(1)加入2mol SO2和2mol O2发生反应,达到平衡时,放出的热量为 ;
(2)保持同一反应温度,在相同的容器中,将起始物质的量改为amol SO2、bmol O2、cmol SO3(g),欲使平衡时SO3的体积分数为2/9,
①达到平衡时,⑴与⑵放出的热量 (填序号)。
A.一定相等 B.前者一定小 C.前者大于或等于后者
②a、b、c必须满足的关系是 、 (一个用a、c表示,另一个用b、c表示),
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,下列各组热化学方程式中,△H1<△H2是
A.C(s)+![]() O2(g)=CO(g);△H1 C(s)+O2(g)=CO2(g);△H2
O2(g)=CO(g);△H1 C(s)+O2(g)=CO2(g);△H2
B.![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2
Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2
C.2H2(g)+O2(g)=2H2O(g);△H1 2H2(g)+O2(g)=2H2O(l);△H2
D.S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g);△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+O2(g)=CO2(g) △H1=-395kJ/mol,
CO(g)+1/2O2(g)=CO2(g) △H2=-283kJ/mol,
则反应C(s)+1/2O2(g)=CO(g)的反应热△H3等于 ( )
A. -112 kJ/mol B. -395 kJ/mol C. + 112 kJ/mol D. -283 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com