
����Ŀ�������(LiMn2O4)����Ϊ����ӵ�ص��������ϡ���ҵ���������̿����պ���������SO2 ��O2���Ʊ�����ﮣ������������£�
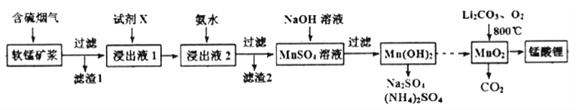
��֪�������̿���Ҫ�ɷ�ΪMnO2��������Fe2O3��FeO��Al2O3��SiO2�����ʡ�
�����̿������պ��������Ĺ�������������ǿ��
�۲����������������ص���ҺpH���±���
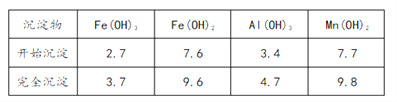
��1����֪��
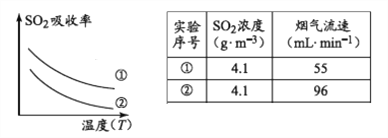
���д�ʩ�����SO2�����ʵ���__________������ţ�
a.����ͨ�뺬���������¶� b.����ͨ�뺬���������¶�
c.�������̿Ľ����� d.��Сͨ�뺬������������
��2�������Լ�X����߲�Ʒ���ȣ���X������_____________���ѧʽ��
��3���Ӱ�ˮ����ҺpH��5��6֮�䣬Ŀ����_______________��
��4������﮿ɳ���ص��ܷ�ӦʽΪ��Li1-xMnO2+LixC ![]() LiMn2O4+C(x<1)
LiMn2O4+C(x<1)
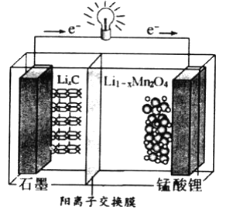
�ٷŵ�ʱ����ص�������ӦʽΪ__________________
�ڳ��ʱ����ת��1mole-����ʯī�缫������__________g��
���𰸡� a��d H2O2����O3�� ��ȥ��Ԫ�غ���Ԫ��[���γ�Fe(OH)3��Al(OH)3��������ȥ] Li1��xMn2O4+ xLi++ xe��==LiMn2O4 7
����������1��a.����ͼ���¶�Խ�ߣ�SO2������Խ�ͣ���˽���ͨ�뺬���������¶ȿ������SO2�����ʣ���ȷ�� b. ����ͼ���¶�Խ�ߣ�SO2������Խ�ͣ�����ͨ�뺬���������¶ȣ�SO2�����ʽ��ͣ�����c.�������̿Ľ�����������������Ӧ���Ӳ���֣�SO2�����ʽ��ͣ�����d.��Сͨ�뺬�����������٣���Ӧ���ӳ�֣��ܹ����SO2�����ʣ���ȷ����ѡad��
��2�����̿���Ҫ�ɷ�ΪMnO2��������Fe2O3��FeO��Al2O3��SiO2�����ʣ��������������̿��������������̺������������������������ȣ��������費��Ӧ�����˳�Ϊ���������������������ص���ҺpH��֪������������Ҫ������������Ҫ��ȥ����������������������ȥ��������ʱ������Ҳ������������Ҫ����������ת��Ϊ������������Լ�X���������ԣ�����ѡ��H2O2����O3�����ʴ�Ϊ��H2O2����O3����
��3���Ӱ�ˮ����ҺpH��5��6֮�䣬����ʹ��Ԫ�غ���Ԫ���γ�Fe(OH)3��Al(OH)3��������ȥ���ʴ�Ϊ����ȥ��Ԫ�غ���Ԫ�أ�
��4�����ŵ�ʱ����ص�����������ԭ��Ӧ����ӦʽΪLi1��xMn2O4+ xLi++ xe��==LiMn2O4���ʴ�Ϊ��Li1��xMn2O4+ xLi++ xe��==LiMn2O4��
�����ʱ��ʯī�缫�Ϸ����ķ�ӦΪC+xe��+ xLi+=LixC����ת��1mole-��ʯī�缫�����ص�����Ϊ1molLi+��������Ϊ7g���ʴ�Ϊ��7��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����ԭ�ӡ����ӵIJ������о����ʵ���ɡ��ṹ�����ʼ��仯���ɵĿ�ѧ������ˮΪ��������ѧ��֪ʶ�ش��������⣮
��1������ˮ�����ӿɱ�ʾΪ������ţ���
��2���Ӻ���Ͽ���ˮ����Ԫ����ɣ�
��3����ˮ�����������У�����˵����ȷ����������ţ���
A.ˮ����֮��������
B.ˮ�����ڲ����˶�
C.�Ƿ��ӷֽ����ԭ�Ӻ���ԭ��
D.ˮ���ӱ����
��4��ˮ�dz��õ��ܼ������������ʼ���ˮ�У���ֽ��裬�����γ���Һ����������ţ���
A.�ƾ�
B.����
C.������
D.�������
��5����Ȼˮ��ΪӲˮ�������п�ͨ������ʹ������������Ӳˮ����ˮ�ķ����ɼ������м���
��6������ˮ��������ϧˮ��Դ����ÿ������Ӧ�������κ��������������������ˮ����Ⱦ����������ţ���
A.����ʹ��ũҩ����
B.���Ͼɵ������������
C.������ֳ����ˮֱ�����뽭����
D.��ˮ��Դ��������ֲ������
��7��д��������ˮ�йصĻ�ѧ��Ӧ����ʽ��ˮͨ��ֽ���
��ˮ����ʯ�ҷ�Ӧ��ȡ��ʯ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ����̬�⻯�ﻯѧʽΪH2R����������������Ӧ��ˮ���ﻯѧʽΪ
A. H2RO3 B. H2RO4 C. HRO3 D. H3RO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ƿ��Ϳɵ����ᣬΪ�о�����ķ�����ɺͽṹ������������ʵ�飺
��1����ȡ����0.90g����ij��״����ʹ����ȫ��������ͬ״����ͬ�����H2������Ϊ0.02g�����������Է�������Ϊ ��
��2��������������������������ȼ��ֻ����CO2��H2O��g������ȫ������ʯ������ʱ����ʯ�ҵ���������1.86g�������˲���ͨ�����ʯ��ˮ�У������3.00g��ɫ������������ķ���ʽΪ ��
��3����ȡ0.90g���ᣬ�������������Ʒ�Ӧ������H2224mL����״��������������̼�����Ʒ�Ӧ������224mLCO2����״������������Ľṹ��ʽ����Ϊ�� ��
��4���������Ƿ���ֻ�������ᣬ�䷴Ӧ�Ļ�ѧ����ʽΪ ��
��5�����������ᡢ�������Ҵ����ܷ���������Ӧ����ͬ�������������ɵ�������������л����������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Һ©����֪��R��OH+HX��R��X+H2O
��ͼ��ʵ�������Ҵ���Ũ������廯�Ʒ�Ӧ�Ʊ��������װ�ã�ͼ��ʡȥ�˼���װ�ã��й����ݼ�����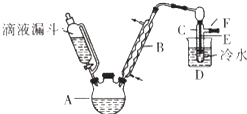
�Ҵ��������顢���йز���
�Ҵ� | ������ | �� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | �����ɫҺ�� |
�ܶ�/gcm��3 | 0.79 | 1.44 | 3.1 |
�е�/�� | 78.5 | 38.4 | 59 |
��1���Ʊ������У������Ũ����������ϡ�ͣ���Ŀ���� ��
a���ٸ�����ϩ���ѵ����� b������Br2������c����HBr�Ļӷ� d��ˮ�Ƿ�Ӧ�Ĵ���
��2�����ȵ�Ŀ�����������ʺ���������ش𣩣�Ӧ��ȡ�ļ��ȷ�ʽ�� ��
��3��Ϊ��ȥ��Ʒ�е�һ����Ҫ���ʣ����ѡ��������Һ��ϴ�Ӳ�Ʒ��
A.��������
B.�⻯��
C.��������
��4���ڣ�3������ʵ������Ҫ����Ҫ���������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��ں����ܱ������з������·�Ӧ��2A(g)��B(g) ![]() 3C(g)������Ӧ��ʼʱ����2mol A��2mol B����ƽ���A���������Ϊa%��������������ʱ�������������������Ϊ��ʼ���ʣ�ƽ���A�������������a%������ ��
3C(g)������Ӧ��ʼʱ����2mol A��2mol B����ƽ���A���������Ϊa%��������������ʱ�������������������Ϊ��ʼ���ʣ�ƽ���A�������������a%������ ��
A. 2mol C B. 2mol A��3mol B��1mol He��He���μӷ�Ӧ��
C. 1mol B��1mol C D. 2mol A��3mol B��3mol C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ع��������÷������ˮ����������ȼӹ����ɵ���ʳ�������������й�˵������ȷ����( )
A. ���ع���������Ҫ�ɷ��ǵ����ʣ������н϶����Ԫ��
B. ���ع������������ͨʳ����һ�����������������ع��������й̶����۷е�
C. ���ع������ڼ������ݼ���������������彡����Ӱ��
D. ���ع����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����㷺�����������ʡ�������ȷ��档�ش�����������
(1)ʵ���ҿ�����ͼ��ʾװ�úϳɰ���
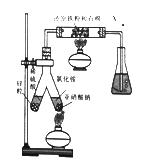
�ٺϳɰ�ʱ����ԭ���۵�������________________��
����ƿ��ʢ��һ������ˮ�������м��η�̪�Լ�����Ӧ����ʱ�������ƿ����Һ�����������X�ijɷ�ΪN2��ˮ������____________��_________________��
�����˹̹����ѧ�о���Ա������һ��SUNCAT���ѭ��ϵͳ���ɳ����ϳɰ�����ԭ����ͼ��ʾ��
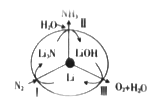
��ͼ�з�Ӧ���Ļ�ѧ����ʽΪ____________________��
�ڷ�Ӧ��������ת���ķ�ʽ��__________________(�����ת��Ϊ��ѧ�ܡ���ѧ��ת��Ϊ���ܡ�)��
(3)Һ���������������Һ������ʱ__________(��ͷ��������ա�)������Һ��й©������ᷢ����ը����֪���ֻ�ѧ���ļ����������±���ʾ��
���ۼ� | N-H | O=O | N��N | O-H |
����/kJ��mol-1 | 391 | 498 | 946 | 463 |
��Ӧ 4NH3(g)+3O2(g)=2N2(g)+6H2O(g)�ķ�Ӧ����H=____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.1 Lˮ���ܽ���58.5 g NaCl������Һ�����ʵ���Ũ��Ϊ1 mol/L
B.��1 L 2 mol/L��H2SO4��Һ��ȡ��0.5 L������Һ��Ũ��Ϊ1 mol/L
C.����480 mL 0.5 mol/L��CuSO4��Һ����62.5 g����
D.10 g 98%�����ᣨ�ܶ�Ϊ1.84 gcm��3����10 mL18.4 molL��1�������Ũ�Ȳ�ͬ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com