
【题目】纳米级Fe3O4呈黑色,因其有磁性且粒度小而在磁记录材料、生物功能材料等诸多领域有重要应用,探究其制备和用途意义重大。
(1)还原-沉淀法:①用还原剂Na2SO3将一定量Fe3+可溶盐溶液中的1/3Fe3+还原,使Fe2+和Fe3+的物质的量比为1:2。②然后在①所得体系中加入氨水,铁元素完全沉淀形成纳米Fe3O4。写出②过程的离子方程式:__________________________。
当还原后溶液中c(Fe2+):c(Fe3+)=2:1时,由下表数据可知,产品磁性最大,可能的原因是___________________________ 。
c(Fe2+):c(Fe3+) | 沉淀性状 | 磁性大小 |
1:3 | 红棕色 | 92.7% |
1:2 | 棕色 | 96.5% |
2:1 | 黑色 | 100% |
(2)电化学法也可制备纳米级Fe3O4,用面积为4cm2的不锈钢小球(不含镍、铬)为工作电极,铂丝作阴极,用Na2SO4溶液作为电解液,电解液的pH维持在10左右,电流50mA。生成Fe3O4的电极反应为________________________。
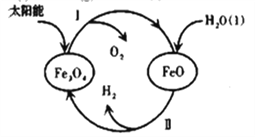
(3)已知:H2O(l)=H2(g)+1/2O2(g) △H=+285.5kJ·mol-1,以太阳能为热源分解Fe3O4,经由热化学铁氧化合物循环分解水制H2的过程如下,完善以下过程Ⅰ的热化学方程式。
过程Ⅰ:________________________________,
过程Ⅱ:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) △H=+128.9kJ·mol-1
(4)磁铁矿(Fe3O4)常作冶铁的原料,主要反应为:Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2(g),该反应的△H<0,T℃时,在IL恒容密闭容器中,加入Fe3O4、CO各0.5mol,10min后反应达到平衡时,容器中CO2的浓度是0.4mol·L-1。
3Fe(s)+4CO2(g),该反应的△H<0,T℃时,在IL恒容密闭容器中,加入Fe3O4、CO各0.5mol,10min后反应达到平衡时,容器中CO2的浓度是0.4mol·L-1。
①T℃时,10min内用Fe3O4表示的平均反应速率为_____g·min-1。
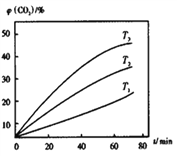
②其他条件不变时,该反应在不同温度下,CO2含量随时间的变化φ(CO2)-t曲线如图所示,温度T1、T2、T3由大到小的关系是_________________,判断依据是___________________。
【答案】 Fe2++2Fe3++8NH3·H2O==Fe3O4↓+8NH4++4H2O Fe2+容易被氧化为Fe3+ 3Fe-8e-+8OH-=Fe3O4↓+2H2O 2Fe3O4(s)=6FeO(s)+O2(g) △H=+313.2kJ·mo1-1 2.32 T3>T2>T1 其他条件相同时,图像斜率:T3>T2>T1而温度越高,反应速率越快,所以T3>T2>T1
【解析】(1)根据题意可知,混合液中使Fe2+和Fe3+的物质的量比为1:2,加入氨水后,铁元素完全沉淀形成纳米Fe3O4,反应的离子方程式:Fe2++2Fe3++8NH3·H2O==Fe3O4↓+8NH4++4H2O; 当还原后的溶液中c(Fe2+):c(Fe3+)=2:1时,由于Fe2+还原性较强,被氧气氧化为Fe3+,生成Fe3O4的量增多,产品磁性最大;正确答案:Fe2++2Fe3++8NH3·H2O==Fe3O4↓+8NH4++4H2O;Fe2+容易被氧化为Fe3+ 。
(2) 不锈钢小球(不含镍、铬)为电解池的阳极,金属铁在阳极失电子,在碱性环境下,生成Fe3O4,电极反应为3Fe-8e-+8OH-=Fe3O4↓+2H2O;正确答案:3Fe-8e-+8OH-=Fe3O4↓+2H2O。
(3) 已知:H2O(l)=H2(g)+1/2O2(g) △H=+285.5kJ·mol-1,过程Ⅱ:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) △H=+128.9kJ·mol-1,根据盖斯定律可知:总反应减去反应Ⅱ,再乘以2,得过程Ⅰ为:2Fe3O4(s)=6FeO(s)+O2(g)△H=+313.2kJ·mo1-1 ;正确答案:2Fe3O4(s)=6FeO(s)+O2(g)△H=+313.2kJ·mo1-1 。
(4)磁铁矿(Fe3O4)常作冶铁的原料,主要反应为:Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2(g),该反应的△H<0,T℃时,在IL恒容密闭容器中,加入Fe3O4、CO各0.5mol,10min后反应达到平衡时,容器中CO2的浓度是0.4mol·L-1。
3Fe(s)+4CO2(g),该反应的△H<0,T℃时,在IL恒容密闭容器中,加入Fe3O4、CO各0.5mol,10min后反应达到平衡时,容器中CO2的浓度是0.4mol·L-1。
①10min后反应达到平衡时,容器中CO2的浓度是0.4mol·L-1,CO2的量是0.4mol,则消耗Fe3O4的量0.1mol,质量为0.1×232=23.2 g,所以10min内用Fe3O4表示的平均反应速率为23.2/10=2.32g·min-1;正确答案:2.32。
②其它条件相同时,图像斜率:T3>T2>T1,而温度越高,反应速率越快,所以T3>T2>T1;正确答案:T3>T2>T1;其他条件相同时,图像斜率:T3>T2>T1而温度越高,反应速率越快,所以T3>T2>T1。


科目:高中化学 来源: 题型:
【题目】NaOH溶液可用于多种气体的处理。
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①溶液中粒子种类:Na2CO3溶液_____NaHCO3溶液(填“>”、“<”或“=”)。
②已知25℃时CO32-第一步水解的平衡常数K1=2×10-4mol/L.溶液中c(HCO3-):c(CO32-)=20:1时,溶液的pH=______。
③泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式__________。
(2)金属与浓硝酸反应产生的NO2可用NaOH溶液吸收,反应方程式:2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2mol NO2恰好完全反应得IL溶液A,溶液B为0.1mol/LCH3COONa溶液,则两份溶液中c(NO3-)、c( NO2-)和c(CH3COO-)由小到大的顺序为___________(已知HNO2的电离常数Ka=7.1×10-4mol/L,CH3COOH的电离常数Ka=1.7×10-5mol/L)。可使溶液A和溶液B的pH相等的方法是_____(填字母序号)。
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH
(3) SO2会引起酸雨,可利用氢氧化钠溶液吸收,吸收SO2的过程中,pH随n(SO32-)、n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显_______性,用化学平衡原理解释:______________。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):____
a. c(Na+)=2c(SO32-) +c(HSO3-)
b. c(Na+)>c(HSO3-)>c(SO32-)>c(H+) = c(OH-)
c.(Na+)+c(H+)=c(SO32-)+c(HSO3-) +c(OH-)
③当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如下:
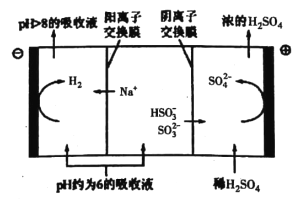
HSO3-在阳极放电的电极反应式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.Fe在氯气中燃烧生成FeCl2
B.将AlCl3溶液逐滴滴入到NaOH溶液,先产生白色沉淀,最后沉淀消失
C.电解氯化钠溶液制取金属单质钠
D.常温下,铝制品用浓硫酸或浓硝酸处理过,可耐腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冰晶石(Na3AlF6)微溶于水,工业上用萤石(CaF2含量为96%)、二氧化硅为原料,采用氟硅酸钠法制备冰晶石,其工艺流程如下:
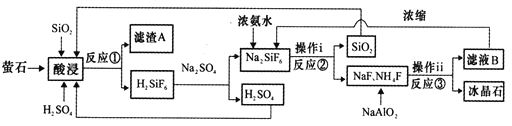
(1)Na3AlF6中氟、铝以共价键结合,写出Na3AlF6中所含阳离子的电子式________________,滤渣A的主要成分是_______________________(填名称)。
(2)为探究适合“酸浸”的条件,取4份相同样品进行实验,所得结果如下表所示:
实验编号 | 萤石品位 | 硫酸的 | 反应温度/℃ | 获得 Na2SiF6的质量 |
(CaF2含量) | 质量分数 | |||
1 | 96% | 25% | 60~70 | 120 |
2 | 96% | 35% | 60~70 | 153 |
3 | 96% | 35% | 80~90 | 100 |
4 | 96% | 40% | 60~70 | 141 |
①实验3比实验2获得Na2SiF6的质量低的原因可能是___________________。
②选择“酸浸”时所采用的最适合条件为____________________________。
(3)写出反应③的离子方程式:______________________________。
(4)“操作ⅰ”不能用硅酸盐质设备进行分离的原因__________________________。
(5)经测定,操作ⅰ所得滤液中所含杂质中K+浓度为0.05mol·L-1,当Na+浓度降为0.01mol·L-1时,若不考虑其它离子影响和溶液体积变化,K+___________(填“是”或“否”)开始沉淀。(已知25℃时,Ksp(Na3AlF6)=4.0×10-10,Ksp(K3AlF6)=6.0·10-8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用于合成树脂的四溴双酚F、药物透过性材料高分子化合物PCL合成如下。
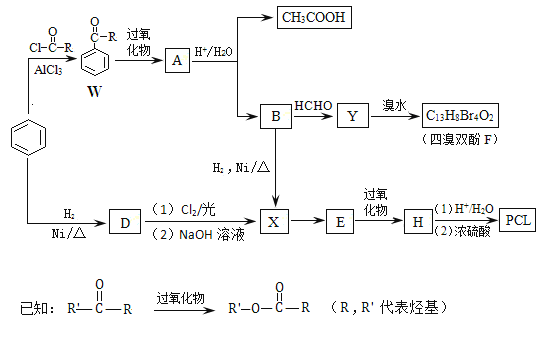
(1)W中—R是_________________________________。
(2)A的结构简式是_____________________________。
(3)A生成B和CH3COOH的反应类型是________________________。
(4)D→X过程中所引入的官能团分别是_________________________。
(5)E的分子式是C6H10O,E与H2反应可生成X。H的结构简式是____________________。
(6)有机物Y的苯环上只有2种不同化学环境的氢原子。
① 由B生成Y的反应方程式是___________________________________。
② 由Y生成四溴双酚F的反应方程式是_______________________________。
③ 在相同条件下,由B转化成四溴双酚F的过程中有副产物生成,该副产物是四溴双酚F的同分异构体,其结构简式可能是_________________________________。
(7)高分子化合物PCL的结构简式是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中的每一方格表示相关的一种反应物或生成物。其中B是一种单质,其余物质也都是含有B元素的化合物。C是一种钠盐,E是C对应的酸,B的结构类似金刚石,D为氧化物。
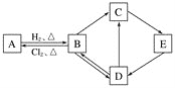
请回答下列问题:
(1)A、D、E的化学式分别为________、________、________。
(2)A和B的互相转化在工业上有什么实际意义?_____________________。
(3)写出D→C反应的化学方程式:_____________________。
(4)写出E→D反应的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A由Al2O3、Fe2O3、Al、Cu中的某几种粉木混合而成,设计成份分析实验方案如下,下列分析不正确的是

A. 当m1>m2时,固体中一定存在A1元素
B. 生成蓝色溶液的离子方程式: Cu+2Fe3+=Cu2++2Fe2+
C. 当m2-m3=2.96g,Fe3O4的质量至少为2.32g
D. 溶液a中一定存在c(Na+)>c(A102-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(1)用双线桥表示出电子转移的方向和数目________,题干中反应改写成离子方程式是____。
(2)电解食盐水的过程中,被还原的元素是____________,氧化产物是______。
Ⅱ.四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是:3Fe2++2S2O32-+O2+xOH-=Fe3O4↓+S4O62-+2H2O。请回答下列问题。
(1)水热法制备Fe3O4纳米颗粒的反应中,还原剂是__________。
(2)反应的化学方程式中x=______。
(3)每生成1 mol Fe3O4,反应转移的电子为____mol,被Fe2+还原的O2的物质的量为_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是关于多电子原子核外电子运动规律的叙述,其中叙述正确的是( )
A. 核外电子是分层运动的B. 所有电子在同一区域里运动
C. 能量高的电子在离核近的区域运动D. 同一能层的电子能量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com