
Ŀǰ�г��ϵ�����Ӧ���ƣ���Ҫ�õ��ǡ���Һ�ɷۡ�Ǧ�����أ���ԭ���ǽ�ǿ��ʴ�Ե�Ũ�����ע���轺�У�ʹ�������Һ������й©���������˵�ص����ܣ����õ�ԭ����Ȼ��Pb��PbO2��H2SO4�����й��ڸ�Ǧ�����ص�˵����ȷ���ǣ�������
| �� | A�� | ���ʱ����Դ�����������رꡰ+����һ��������ϱ��С�������һ������������Ӧ |
| �� | B�� | ����Һ�ɷۡ�Ǧ�����س��ı���ԭ����Ǧ�����ص�ԭ�� |
| �� | C�� | �ŵ�ʱ����Ǧ�����صĸ���������ԭ��Ӧ |
| �� | D�� | ���ô�Ǧ�����ص�ⱥ��NaCl��Һ����״�����Ʊ�1.12LCl2���������������H2SO40.10 mol |
| ԭ��غ͵��صĹ���ԭ���� . | |
| ר�⣺ | �绯ѧר�⣮ |
| ������ | A���������ǵ��أ�����PbO2������������Ǧ�������� B������Һ�ɷۡ�Ǧ�����غ�Ǧ�����صķ�Ӧԭ���Աȵó��𰸣� C��ԭ��صĸ����Ϸ���ʧ���ӵ�������Ӧ�� D�����ݵ�ⷽ��ʽ��ϵ����غ���㣮 |
| ��� | �⣺A�����ʱ����Դ�����������رꡰ+����һ����������������ԭ����еĸ���Ǧ���ӱ��С�����һ�������������������ϱ��С�������һ���õ��ӷ�����ԭ��Ӧ����A���� B������Һ�ɷۡ�Ǧ�����غ�ԭ����Ǧ�����صķ�Ӧԭ����һ���ģ���B���� C���ŵ�ʱ��Ǧ�����صĸ�������������Ӧ����C���� D����״�����Ʊ�1.12LCl2�������������ʵ���Ϊ0.05mol��ת�Ƶ���Ϊ0.1mol��Ǧ�����صķ�ӦΪ��PbO2+Pb+2H2SO4�T2PbSO4+2H2O������ת�Ƶ���Ϊ0.1mol����������0.1mol����D��ȷ�� ��ѡ��D�� |
| ������ | ���⿼��ѧ�����ε��Ǧ���صĹ���ԭ��֪ʶ�������ۺ�ԭ��غ͵��ع���ԭ��֪ʶ�Ŀ��飬�����ڻ���֪ʶ�Ŀ��飬��Ŀ�ѶȲ��� |


 ����������������ϵ�д�
����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ֽ�1mo1Cu2S��144��FeOͶ�뵽����ϡ������Һ�У���ַ�Ӧ�õ�Fe(NO3)3��Cu(NO3)2 ��CuSO4�Ļ����Һ��������NO���塣�����շ�Ӧ����NO���ʵ���Ϊ
A��4 mo1 B��5 mo1 C��6 mo1 D��7 mo1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȼ�ϵ�����ں���ɴ����缫��Ӧ������ˮ���������������������Ա������ˮ����缫��Ӧ���£�������2H2 + 4OH- - 4e- = 4H2O ������O2 + 2H2O + 4e- = 4OH�������õ�1.8L����ˮʱ�������ת�Ƶĵ�����ԼΪ �� ��
A.1.8mol B.3.6mol C.100mol D.200mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ԭ����������缫�����Ʋ�����缫���ϵ������йأ�Ҳ��������Һ�йأ������ɲ�ͬ������ɵ�ԭ��أ��缫��Ӧ��ȷ���ǣ�������
A����Fe��Cu��ϡ������Һ��ɵ�ԭ��أ��为����ӦʽΪ��Fe��3e���TFe3+
B����Al��Mg������������Һ��ɵ�ԭ��أ��为����ӦʽΪ��Mg��2e��+2OH���TMg��OH��2
C����Pb��Cu���Ȼ�����Һ��ɵ�ԭ��أ���������ӦʽΪ��Cu��2e���TCu2+
D����Al��Cu��Ũ������ɵ�ԭ��أ��为����ӦʽΪ��Cu��2e���TCu2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ�顰�����������롰���ۡ���Ӧ��ϵ��ȷ���ǣ�������
| ���������� | ���� | |
| A | ������¯ˮ���е�CaSO4ʱ�����μ��뱥��Na2CO3��Һ�����ᣬˮ���ܽ� | �ܽ�ȣ�S��CaCO3����S��CaSO4�� |
| B | ��ʯī���缫���MgSO4��Һ��ij�缫�����а�ɫ�������� | �õ缫Ϊ���� |
| C | ��FeCl3��CuCl2�����Һ�м������ۣ��к�ɫ�������� | �����ԣ�Cu2+��Fe3+ |
| D | ��ij��Һ���ȵμ������ữ���ٵμ�BaCl2��Һ���а�ɫ�������� | ����Һ��һ������Ag+ |
| �� | A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
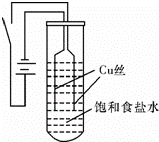
ijУ��ѧ�о���ѧϰС����ͭΪ�缫��ⱥ��ʳ��ˮ��̽���������£�
��ʵ�����ͼװ�ã���Դ��ͨ�����ظ���������ͭ˿���д������ݲ�������������������ͭ˿�ɴֱ�ϸ����ʼ30s�ڣ������������ְ�ɫ���ǣ�Ȼ��ʼ���ֳȻ�ɫ���ǣ���ʱ�ⶨ��Һ��pHԼΪ10�����ų������������ӣ��Ȼ�ɫ���������ۼ����Թܵײ�������Һʼ��δ������ɫ��
��ʵ���ʵ������Թܵײ��ijȻ�ɫ����ȡ������װ����֧С�Թ��У������ܿ�ת��Ϊש��ɫ�������IJ������������£�
| ��� | ���� | ���� |
| �� | ����ϡ���� | ש��ɫ�����ܽ⣬����ɫ���ݲ��������յõ���ɫ��Һ |
| �� | ����ϡ���� | ש��ɫ����ת��Ϊ�Ϻ�ɫ�������Һ����ɫ |
��֪����ͭ�Ļ�������ɫ���£�
| ���� | ��ɫ | ���� | ��ɫ |
| �Ȼ�ͭ | �������ɫ��Ũ��Һ����ɫ��ϡ��Һ����ɫ | ��������ͭ�����ȶ��� | �Ȼ�ɫ |
| ��ʽ�Ȼ�ͭ | ��ɫ | ������ͭ | ��ɫ |
| ������ͭ | ש��ɫ | �Ȼ���ͭ | ��ɫ |
��ش��������⣺
��1��ͭ�ij������ϼ�Ϊ��+1������+2�����ۼ����Թܵײ��ijȻ�ɫ�����Ļ�ѧʽΪ��Cu2O����
��2�������ĵ缫��ӦʽΪ��2Cu+2Cl����2e��=2CuCl������
��3��д��ʵ����Т١��ڵ����ӷ���ʽ���١�3Cu2O+2H++2NO3��=6Cu2++2NO��+7H2O�����ڡ�Cu2O+2H+=Cu+Cu2++H2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
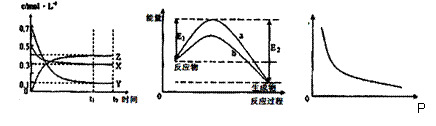
X��Y��Z��������̬���ʣ���һ���¶�����仯������ͼ������˵������ȷ����
 |
 ͼI ͼII ͼIII
ͼI ͼII ͼIII
 A���÷�Ӧ�Ļ�ѧ����ʽΪX(g) +3Y(g) 2Z(g)
A���÷�Ӧ�Ļ�ѧ����ʽΪX(g) +3Y(g) 2Z(g)
B��ͼIII�е�������ɱ�ʾ���������Z�ĺ�������������ƽ��Ħ������
C���������¶ȣ��÷�Ӧ��ƽ�ⳣ����С��Y��ת���ʽ���
D��ͼII�����߿ɱ�ʾ�������������仯����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ײ�����ȱλ�����Σ�MFe2Ox ����3��x��4��M��ʾMn��Co��Zn��Ni�Ķ������ӣ��������£�����ʹ��ҵ�����е�SO2��NO2��������ת��Ϊ���ʣ�ת��������ͼ��ʾ���й�����ת�����̵�����������ȷ���ǣ�������

| �� | A�� | MFe2O4�����˻�ԭ�� | B�� | MFe2Ox�����˻�ԭ�� |
| �� | C�� | SO2��NO2�����˻�ԭ�� | D�� | SO2��NO2�����˷ֽⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и�������Щ�ǵ���ʣ���Щ�Ƿǵ���ʣ�
KCl BaSO4 CH3CH2OH NaOH Fe H2SO4 H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com