
A、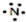 |
B、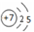 |
| C、1s22s22p3 |
D、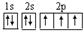 |
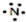 表示N原子最外层有5个电子;
表示N原子最外层有5个电子;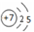 表示N原子的电子层数和每层的电子数;
表示N原子的电子层数和每层的电子数; 表示出N原子的原子轨道,各轨道中的电子数,以及电子的自旋方向.
表示出N原子的原子轨道,各轨道中的电子数,以及电子的自旋方向.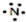 表示N原子最外层有5个电子,不能说明原子核外电子运动状态,故A不选;
表示N原子最外层有5个电子,不能说明原子核外电子运动状态,故A不选;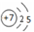 表示N原子的电子层数和每层的电子数,不能说明原子核外电子运动状态,故B不选;
表示N原子的电子层数和每层的电子数,不能说明原子核外电子运动状态,故B不选; 表示出N原子的原子轨道,各轨道中的电子数,以及电子的自旋方向,所以能说明原子核外电子运动状态,故D选.
表示出N原子的原子轨道,各轨道中的电子数,以及电子的自旋方向,所以能说明原子核外电子运动状态,故D选.

科目:高中化学 来源: 题型:
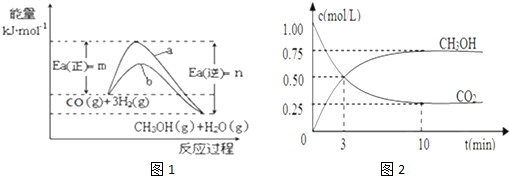
| n(CH3OH) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若A2和B2的总能量之和大于生成的2AB的总能量,则反应放热 |
| B、若A2和B2的总能量之和小于生成的2AB的总能量,则反应放热 |
| C、若该反应为放热反应,则Q1+Q2>Q3 |
| D、若该反应为吸热反应,则Q1+Q2<Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它们相差一个电子层 |
| B、它们都能与水反应 |
| C、钠原子、钠离子均为同一元素,因此是同种微粒 |
| D、灼烧时,它们的焰色反应都呈紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 编号 | 待测氢氧化钠溶液体积(mL) | 滴定开始读数(mL) | 滴定结束读数(mL) | 消耗盐酸体积(mL) |
| ① | 25.00 | 0.02 | 26.40 | |
| ② | 25.00 | 0.04 | 25.81 | |
| ③ | 25.00 | 0.03 | 25.78 | |
| ④ | 25.00 | 0.20 | 25.96 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Al3+)=0.1mol/L的溶液中:Na+、K+、[Al(OH)4]-、SO42- |
| B、使酚酞呈红色的溶液中:K+、Ba2+、I-、NO3- |
| C、由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、HCO3-、Cl-、Br- |
| D、加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
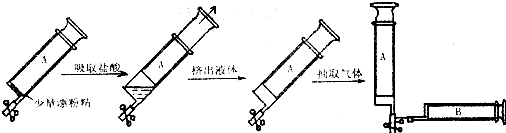
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com