
【题目】盛有NO和NO2 的混合气体的量筒倒立在盛有水的水槽中,过一段时间后,量筒内的气体体积减小为原来的一半.
(1)写出有关反应的化学方程式.
(2)原混合气体中NO和NO2的体积比是多少?
【答案】
(1)解:NO2通入水中,发生反应:3NO2+H2O=2HNO3+NO,
答:有关反应方程式为3NO2+H2O=2HNO3+NO.
(2)解:过一段时间后,量筒内的气体体积减小为原来的一半,则物质的量减小一半,
设混合气体中含有xmolNO,ymolNO2,则:
3NO2+ | H2O | = | 2HNO3+ | NO |
3 | 1 | |||
ymol |
|
所以,(x+ ![]() ):(x+y)=1:2,
):(x+y)=1:2,
解之得:x:y=1:3,
答:原混合气体中NO和NO2的体积比是1:3.
【解析】NO2通入水中,发生:3NO2+H2O=2HNO3+NO,过一段时间后,量筒内的气体体积减小为原来的一半,则物质的量减小一半,设混合气体中含有xmolNO,ymolNO2 , 根据方程式计算.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】如表所示为自然界中的多种铜矿石的主要成分:
矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
主要成分 | CuFeS2 | Cu5FeS4 | Cu2S | CuCO3Cu(OH)2 |
请回答:
(1)上表所列铜化合物中,铜的质量百分含量最高的是(填化学式)
(2)工业上以黄铜矿为原料.采用火法溶炼工艺生产铜.该工艺的中间过程包含反应: 2Cu2O+Cu2S ![]() 6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是
6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是
(3)火法溶炼工艺生产铜的尾气直接排放到大气中造成环境污染的后果是;处理该尾气可得到有价值的化学品,写出其中一种酸和一种盐的名称或化学式、 .
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是(填字母).
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 铜绿的主成分是碱式碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
C | 铁比铜活泼 | 铆在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4HCO3是一种离子化合物,下列关于该物质的叙述错误的是( )
A.所含四种元素的原子半径由小到大的顺序为:H<O<N<C
B.同周期的三种元素的得电子能力由大到小的顺序为:O>N>C
C.与足量烧碱溶液共热的离子方程式为:NH4++OHˉ ![]() NH3↑+H2O
NH3↑+H2O
D.除去NaCl固体中混有少量的NH4HCO3固体可以采用加热的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为有机物,其中A 常用来衡量一个国家石油化工发展水平的标志性物质,它们之间有如下转化关系.已知醛基在氧气中易氧化成羧基,请回答下列问题: 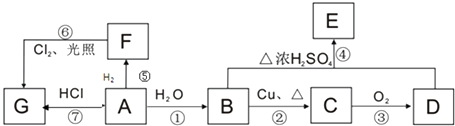
(1)A、B中官能团的名称:A、B;
(2)在F的同系物中最简单的有机物的空间构型为;
(3)写出与F互为同系物的含5个碳原子的所有同分异构体中一氯代物种类最少的结构简式;
(4)写出下列编号对应反应的化学反应方程式,并注明反应类型: ②、反应;
④、反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g),是工业制硫酸的主要反应之一。
2SO3(g),是工业制硫酸的主要反应之一。
(1)该反应过程的能量变化如图所示:

由图中曲线变化可知,该反应为______(填“放热”或“吸热”)反应。该反应通常用V2O5作催化剂,加入V2O5后,改变的是图中的_____。
A.△H B.E C.△H-E D.△H+E
(2)在2L绝热密闭容器中投入2molSO2和bmolO2,下图是部分反应物随时间的变化曲线。

①10min时,v(SO3)=_____。
②反应达到平衡时,SO2的转化率为______。
③下列情况能说明该反应达到化学平衡的是_____
A. v(SO3)=v(SO2) B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变 D.混合气体的总物质的量不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 在O2参与的反应中,1molO2作氧化剂时得到的电子数一定是4NA
B. 25℃、1.01×105Pa条件下,11.2L丙炔分子中所含碳氢键数为2NA
C. 常温下,2.7g铝分别与足量的盐酸或烧碱溶液反应时,失去的电子数都为0.3NA
D. 1molNO2与足量H20反应,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,A、B反应生成C和D,在2L的密闭容器中进行,起始时加入了4molA和2molB,经过一段时间达到反应限度,测得C的浓度为1mol/L,D的平均反应速率为0.2 mol·L-·min-,A与B都反应了50%,且D与A的化学计量数相同,请回答下列问题:
(1)达到反应限度这段时间内A的反应速率为______________。
(2)写出该反应的化学方程式:________________________________。
(3)达到化学反应限度所用的时间为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置,研究非金属元素性质变化规律。

已知:高锰酸钾在常温下与浓盐酸反应产生氯气。
(1)利用如图装置证明Cl2氧化性强于I2的氧化性。则A中装浓盐酸,B中装入高锰酸钾粉末, C中装入淀粉KI溶液,则C中现象是___________________________
(2)如果C中装饱和的H2S溶液,A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀,证明硫的非金属性比氯的非金属性________(填“强”或“弱”或“无法判断”)。
(3)现有浓硝酸、大理石、澄清石灰水、硅酸钠溶液,选择试剂用如图装置证明:非金属性:N > C > Si。C中装试剂________________,实验现象为_________________________该装置存在不足之处,改进措施为:______________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com