
【题目】工业上用CO和H2合成CH3OH:CO(g)+2H2(g)![]() CH3OH(g)。反应的平衡常数如下表:
CH3OH(g)。反应的平衡常数如下表:

下列说法正确的是( )
A.该反应的△H>0
B.加压、增大H2浓度和加入催化剂都能提高CO的转化率
C.工业上采用高温高压的条件,目的都是提高原料气的转化率
D.t℃时,向1L密闭容器中投入0.1molCO和0.2molH2,平衡时CO转化率为50%,则该温度时反应的平衡常数的数值为100
【答案】D
【解析】
A.根据表中数据可知:温度升高,化学平衡常数减小,说明升高温度化学平衡逆向移动,根据平衡移动原理:升高温度,平衡向吸热反应方向移动,逆反应为吸热反应,则该反应的正反应是放热反应,△H<0,A错误;
B.催化剂对正、逆反应速率影响相同,因此不能使化学平衡状态发生移动,因此使用催化剂不能改变CO的转化率,B错误;
C.该反应为放热反应,所以采用高温不能提高反应物的转化率,C错误;
D. t℃时,向1L密闭容器中投入0.1molCO和0.2molH2,平衡时CO转化率为50%,则此时c(CH3OH)=0.05mol/L,△c(CO)=0.05mol/L,△c(H2)=0.1mol/L,平衡时各种气体的物质的量c(CO)=0.1mo/L-0.05mol/L=0.05mol/L,c(H2)=0.1mol/L-0.1mol/L=0.1mol/L,c(CH3OH)=0.05mol/L,所以该温度下平衡常数K=![]() =100,D正确;
=100,D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
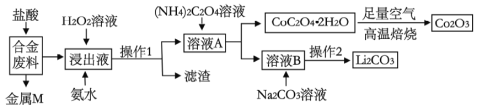
(1)合金废料中加入盐酸浸取,此处盐酸不能换为硝酸,原因是_______________。
(2)操作1用到的玻璃仪器有__________________________。
(3)浸出液中加入H2O2溶液和氨水,应先加入_____________,加入氨水发生反应的离子方程式为____________________。
(4)在空气中焙烧CoC2O4·2H2O的化学方程式是____________________。
(5)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表
温度/℃ | 10 | 30 | 60 | 90 |
浓度/molL-1 | 0.21 | 0.17 | 0.14 | 0.10 |
则操作2的具体流程是_______________、_____________、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ:用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________。
(2)如果按图中所示的装置进行试验,求得的中和热数值_______(填“偏大、偏小、无影响”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与(2)中实验相比,所求中和热_________ (填“相等”或“不相等”)。
Ⅱ: (1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6),丙烷脱氢可得丙烯。已知:C3H8(g) === CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6 kJ·mol-1
CH3CH=CH2(g)=== CH4(g)+ HC≡CH(g ) △H2=+32.4 kJ·mol-1
则C3H8(g) === CH3CH=CH2(g)+H2(g) △H =______________ kJ·mol-1。
(2)发射火箭时用肼(N2H4)作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知32gN2H4(g)完全发生上述反应放出568kJ的热量,热化学方程式是:____________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用有关概念,判断下列叙述正确的是![]()
A.![]() 溶于水后能导电,故C
溶于水后能导电,故C![]() 为电解质
为电解质
B.![]() 、
、![]() 、
、![]() 、
、![]() 互为同素异形体
互为同素异形体
C.NaCl溶液和![]() 溶液均显中性,故两溶液中水的电离程度相同
溶液均显中性,故两溶液中水的电离程度相同
D.溶液与胶体本质区别为分散质微粒直径的大小不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大.金属W是制备手机电池的常用材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是它的电子层数的2倍。下列说法正确的是![]()
A.金属W具有两性
B.X、Z形成的化合物为离子化合物
C.Y与Z生成的化合物在水中会发生双水解
D.元素X与氢形成的原子个数比为1:1的化合物只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于难溶盐MX,其饱和溶液中M+和X-浓度之间的关系为Ksp=c(M+)c(X-),现将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的顺序是( )
①20mL0.01molL-1KCl溶液;②30mL0.02molL-1CaCl2溶液;③40mL0.03molL-1HCl溶液;④10mL蒸馏水;⑤50mL0.05molL-1AgNO3溶液
A.①>②>③>④>⑤B.④>①>③>②>⑤
C.⑤>④>②>①>③D.④>③>⑤>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4-溴环己烯(![]() )可与下列4种物质发生反应:①HBr、②酸性高锰酸钾溶液、③氢氧化钠的水溶液、④氢氧化钠的乙醇溶液。下列有关这些反应的说法中正确的是( )
)可与下列4种物质发生反应:①HBr、②酸性高锰酸钾溶液、③氢氧化钠的水溶液、④氢氧化钠的乙醇溶液。下列有关这些反应的说法中正确的是( )
A.与①反应后的有机产物只有一种
B.与②的反应原理类似于烯烃使溴水褪色
C.与③反应后得到的有机产物可被氧化为醛
D.与④反应后得到的有机产物只有一种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各电离方程式中,书写正确的是( )
A.CH3COOH![]() H++CH3COO-
H++CH3COO-
B.KHSO4![]() K++H++ SO42-
K++H++ SO42-
C.Al(OH)3![]() Al3++3OH-
Al3++3OH-
D.H2CO3![]() 2H++ CO32-
2H++ CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com