
| A、在多电子的基态原子中,不可能有运动状态完全相同的两个电子存在 |
| B、在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| C、在多电子的基态原子中,能量最高的电子往往是距离原子核最近的电子 |
| D、对于多电子原子,其核外电子完全按能层次序排布,填满一个能层才开始填下一能层 |


科目:高中化学 来源: 题型:
| 元素符号 | 元素性质或原子结构 |
| A | A是形成化合物最多的元素 |
| B | B元素的单质在空气中含量最多 |
| C | C元素在地壳中含量最多 |
| D | D元素在同周期中金属性最强 |
| E | 常温常压下,E元素形成的单质是淡黄色固体,常在火山口附近沉积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①② | B、只有④ |
| C、只有①②③ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A、反应前2min的平均速率v(Z)=0.04 mol/(L?min) |
| B、其他条件不变,升高温度,v(逆)增大,v(正)减小 |
| C、该温度下此反应的平衡常数K=1.44 |
| D、其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、14.2g |
| B、19.6g |
| C、28.4g |
| D、30.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:
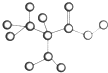 如图是某种只含有C、H、O、N的有机物简易球棍模型.请回答下列各题.
如图是某种只含有C、H、O、N的有机物简易球棍模型.请回答下列各题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、m=4 | B、a=b |
| C、a<b | D、m≤2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验内容以及现象 | 结论 |
| ①取少量N溶液滴加足量的硝酸钡溶液,无沉淀产生 | |
| ② | 确定M溶液中含有Na+,不含K+ |
| ③用pH试纸检测M溶液,pH试纸呈蓝色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com