
【题目】在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
(1)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ/mol;
2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol;
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol。
尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH__________。
(2)某研究性学习小组在技术人员的指导下,按下列流程探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。
![]()
①实验过程中除空燃比不同外,其他条件:汽车尾气的流速、_____________等必须相同。
②在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如图所示。空燃比约为____________时,催化剂对汽车尾气的催化效果最好。

【答案】(1)-746.5 kJ/mol;(2) ①催化反应的温度; ②c;
【解析】
试题分析:(1)N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol①,2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol②,C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol ③,方程式③×2-②-①得NO (g)+2CO(g)=N2(g)+2CO2(g),所以△H=(-393.5kJ/mol)×2-(-221.0kJ/mol)-(+180.5kJ/mol)=-746.5 kJ/mol,故答案为:-746.5 kJ/mol;
(2)①探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果,必须控制其它条件相同,即汽车尾气的流速,催化反应的温度相同,故答案为:催化反应的温度;
②由图象可知,在c点时NO和CO的转化率最高,催化效果最好,故答案为:c。


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A.钠放入水中 Na+H2O=Na++OH-+H2↑
B.电解饱和食盐水 2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.实验室用氯化铝溶液和氨水制氢氧化铝 Al3++3OH-=Al(OH)3↓
D.向碳酸氢铵溶液中加入足量氢氧化钠溶液 HCO3-+OH-=CO32-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图①﹣⑩分别代表有关反应中的一种物质,请填写以下空白.

(1)已知①中阴阳离子个数比为1:1,则①的化学式是_________,②的电子式为_________;
(2)图中涉及的氧化还原反应共有_________个
(3)③与④反应的化学方程式为:_______________。
(4)⑧与⑨反应的化学方程式为:_______________。
(5)一定条件下,将2amL④和⑦的混合气体用排水法收集,得amL气体,则原混合气体中④和⑦的体积比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述正确的是( )
H++CH3COO-,下列叙述正确的是( )
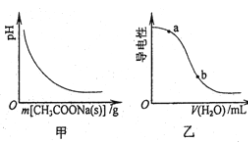
A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b
C.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
D.0.10mol·L-1的CH3COOH溶液中加水稀释,溶液中c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A.78gNa2O2固体中阴离子的个数为2NA
B.标准状况1.12L氯气与H2O反应,反应中转移的电子数为0.1NA
C.CO2通过Na2O2使其增重ag时,反应中转移的电子数为aNA/56
D.60gSiO2含有的化学键数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热化学方程式的书写。
①已知0.4mol液态肼(N2H4)和足量H2O2反应,生成氮气和水蒸气时放出256.65kJ的热量.写出该反应的热化学方程式: 。
②已知化学方程式:H2(g)+O2(g)=![]() H2O(g),该反应的活化能为167.2kJ/mol,其逆反应的活化能为409.0kJ/mol,写出该反应的热化学方程式: 。
H2O(g),该反应的活化能为167.2kJ/mol,其逆反应的活化能为409.0kJ/mol,写出该反应的热化学方程式: 。
③已知白磷(P4)和PCl3的分子结构如图所示,现提供以下的化学键的键能(KJ/mol):P-P 198,Cl-Cl 243, P-Cl 331。则写出1mol白磷完全反应生成PCl3(s)时的热化学方程式:_____________.

④已知S(s)+O2(g)![]() SO2(g)当有4NA个电子转移时,放出297.23kJ的热量.写出该反应的热化学方程式 .
SO2(g)当有4NA个电子转移时,放出297.23kJ的热量.写出该反应的热化学方程式 .
⑤常温常压下,1克CH4完全燃烧生成CO2和H2O时,放出Q kJ的热量.写出此反应的热化学方程式: 。
⑥酒精燃烧的化学方程式为:C2H6O(l)+3O2(g)=2CO2(g)+3H2O(l),完全燃烧一定量的无水酒精,放出的热量为Q kJ,当完全吸收生成的CO2,消耗8mol/L的NaOH溶液50mL时恰好生成正盐.写出此反应的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把 VL含有 MgSO4和 K2SO4的混合溶液分成两等份,一份加入含 a mol NaOH 的溶液, 恰好使Mg2+完全沉淀为 Mg(OH)2; 另一份加入含 b mol BaCl2的溶液, 恰好使SO42-完全沉淀为 BaSO4。则原混合溶液中 K+的浓度为
A. ![]() mol·L1 B.
mol·L1 B. ![]() mol·L1 C.
mol·L1 C. ![]() mol·L1 D.
mol·L1 D. ![]() mol·L1
mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
(一)分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6.72L(标准状况下),则该物质中各元素的原子个数比是____________。
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为____________,该物质的分子式是____________。
(3)根据价键理论,预测A的可能结构并写出结构简式____________。
(二)结构式的确定:

核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(Cl2—CH2—O—CH3)有两种氢原子如图②。经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝合金5.1 g溶于300 ml 2mol/L的盐酸中,标准状况下,放出气体的体积为5.6 L,向反应后的溶液中加入500 ml NaOH溶液,充分反应后,最终产生白色沉淀。
下列有关说法不正确的是( )
A、5.1 g镁铝合金中含有镁和铝的质量分别为2.4g、2.7g
B、若白色沉淀只有Mg(OH)2,该NaOH溶液的浓度至少为1.2mol/L
C、生成沉淀的最大质量为13.6 g
D、溶解5.1 g镁铝合金时,剩余盐酸的物质的量为0.1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com