
����Ŀ��Q��W��X��Y��Z��ԭ��������������Ķ�����Ԫ�أ�X��Y�ǽ���Ԫ�أ�Q��W��Z�Ƿǽ���Ԫ�أ�X��ͬ�����н�������ǿ��Ԫ�أ�����Ԫ�غ˵����֮��Ϊ55����Ӧԭ������������֮��Ϊ21��W��Z������������ͬ����Z�ĺ˵������W��2����
��1��Q�����ڱ���λ���� ��
��2��X��Y���Ե�����������Ӧ��ˮ������Է�����Ӧ�����κ�ˮ����д���÷�Ӧ�����ӷ���ʽ�� ��
��3��X��������W������ȼ�տ����ɻ�����R��R�ĵ���ʽ �� �����������е�����������������Ϊ ��
��4��Z���⻯����W��һ���⻯�����Ӧ������Z�ĵ��ʣ�д���仯ѧ����ʽ ��
���𰸡�
��1���ڶ����ڵ�VA ��
��2��Al��OH��3+OH��=AlO2��+2H2O
��3��![]() �����Ӽ������ۼ�
�����Ӽ������ۼ�
��4��H2S+H2O2=S��+2H2O
���������⣺Q��W��X��Y��Z��ԭ��������������Ķ�����Ԫ�أ�Q��W��Z�Ƿǽ���Ԫ�أ�W��Z������������ͬ��Z�ĺ˵������W��2������WΪOԪ�ء�ZΪSԪ�أ�X��Y�ǽ���Ԫ�أ�X��ͬ�����н�������ǿ��Ԫ�أ���X����IA�壬ԭ����������������XΪNa������Ԫ��ԭ������������֮��Ϊ21����Q��Y������������֮��Ϊ21��1��12=8������Ԫ�غ˵����֮��Ϊ55��Q��Y�ĺ˵����֮��Ϊ55��11��8��16=20����YΪ����������֪QΪNԪ�ء�YΪAl����1��NԪ�������ڱ���λ�ڵڶ����ڵ�VA �壻���Դ��ǣ��ڶ����ڵ�VA �壻��2��X��Y����������Ӧˮ����ֱ�ΪNaOH��Al��OH��3 �� ���߷�Ӧ���ӷ���ʽΪ��Al��OH��3+OH��=AlO2��+2H2O�����Դ��ǣ�Al��OH��3+OH��=AlO2��+2H2O����3��Na��������ȼ������Na2O2 �� �����ʽ�� ![]() ���ڸ����ʺ��еĻ�ѧ�������Ӽ������ۼ������Դ��ǣ�
���ڸ����ʺ��еĻ�ѧ�������Ӽ������ۼ������Դ��ǣ� ![]() �����Ӽ������ۼ�����4��H2S�л�ԭ�ԣ��� H2O2�������ԣ����߷���������ԭ��Ӧ�Ļ�ѧ����ʽ�ǣ�H2S+H2O2=S��+2H2O�����Դ��ǣ�H2S+H2O2=S��+2H2O��
�����Ӽ������ۼ�����4��H2S�л�ԭ�ԣ��� H2O2�������ԣ����߷���������ԭ��Ӧ�Ļ�ѧ����ʽ�ǣ�H2S+H2O2=S��+2H2O�����Դ��ǣ�H2S+H2O2=S��+2H2O��


 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ����ȡ����Ҫʱ�ɼ��ȣ����������ռ��������ǣ� �� 
A.ͭ��ϡ������һ������
B.�Ȼ�����Ũ�������Ȼ���
C.п��ϡ����������
D.��������ϡ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱKsp[Al(OH)3]=1��0��10-33��Ksp[Fe(OH)3]=4��0��10-38����Fe(NO3)3��Al(NO3)3�Ļ����Һ����μ���NaOH��Һ�����ɳ��������ʵ��������NaOH��Һ������Ĺ�ϵ����ͼ��ʾ�����������Fe3+��ȫ����ʱ��Al3+ǡ�ÿ�ʼ����������˵����ȷ���� �� ��

A. ԭ�����Һ��c(Fe3+):c(Al3+)=1:1
B. Fe(NO3)3��Һ�л�������Al(NO3)3���Լ��������NaOH��Һ��ȥ
C. B�����ֳ�����������ʱ�ϲ���Һ��c(Al3+):c(Fe3+)=2.5��104
D. C����Һ�е�����ֻ��NaAlO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ƴ�����ʳƷ����������׳�Ϊ(����)
A. ��ʯ�� B. ������ C. ��ʯ�� D. ʯ��ʯ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������;������ȡ������������ͭ��
��ͭ��ϡ���ᷴӦ����ͭ��Ũ���ᷴӦ����ͭ����������Ӧ��������ͭ������ͭ�ٸ����ᷴӦ��
������������ȷ���ǣ� ��
A.����;�������ĵ�ͭ���������
B.�����ĵ���������ʵ����Ǣ٣��ڣ���
C.;���۵��Ʊ�����������ϡ���ɫ��ѧ�������
D.;�����б�������ͭ�뱻��ԭ����������ʵ�������3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶�ʱ��Cu2+��Mn2+��Fe2+��Zn2+�����ֽ������ӣ�M2+���γ������������S2-���Ũ�ȵĶ���ֵlgc(S2-)��lgc(M2+)�Ĺ�ϵ��ͼ��ʾ�������й��жϲ���ȷ���� �� ��

A. ���¶��£�Ksp��MnS������1.0��10-35
B. ��Mn2+��Zn2+��ϡ��Һ�еμ�Na2S��Һ��Mn2+���п����ȳ���
C. ��c(Fe2+)=0.1mol��L-1����Һ�м���CuS��ĩ����FeS��������
D. ���¶��£��ܽ�ȣ�CuS>MnS>FeS>ZnS
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[���ʽṹ������]2016��9���Ͽ���ѧѧ���״β�����һ������п���ӵ�أ��õ����Zn��CF3SO3��2Ϊ����ʣ�������������ȱ�ݵ�ZnMn2O4Ϊ�缫���ɹ��Ļ�����ȶ��Ĵ��ʵ�����
��1��д��Mnԭ�ӻ�̬��������Ų�ʽ ��
��2��CF3SO3H��һ���л�ǿ�ᣬ�ṹʽ��ͼ1��ʾ��ͨ���� CS2��IF5��H2O2��Ϊ��Ҫԭ����ȡ��
��1molCF3SO3H�����к��е���������ĿΪ mol��
��H2O2������Oԭ�ӵ��ӻ���ʽΪ ����CS2��Ϊ�ȵ�����ķ���Ϊ ��
��IF5��ˮ��ȫˮ�����������ᣬд����ػ�ѧ����ʽ�� ��
��3����п����Ĺ����ж��֣�����һ����п�ľ�����ͼ2���þ�����S2������λ��Ϊ ��
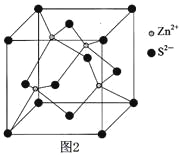
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2Zn(OH)2��ZnCO3���Ʊ�����ZnO���м��壬��п��ɰ����Ҫ�ɷ�ΪZnO��������Cu2+��Mn2+�����ӣ�Ϊԭ���Ʊ�2Zn(OH)2��ZnCO3�Ĺ����������£�

��1����(NH4)2SO4��NH3��H2O���ʵ���֮��Ϊ1��2�Ļ����Һ��ȡп��ɰʱ������[Zn(NH3)4]2+���÷�Ӧ�����ӷ���ʽ�� ����ȡ���̼���H2O2��Ŀ���� ��
��2������S2���ܽ�Cu2+������ת��Ϊ�����������ȥ����ѡ���û��ķ������ӣ���Ӧ���������Ϊ ��
��3������A�Ļ�ѧʽ�� ��
��4������3������Һ��ѭ��ʹ�ã�����Ҫ�ɷֵĻ�ѧʽ�� ��֤��2Zn(OH)2��ZnCO3����ϴ����ȫ�ķ����� ��
��5��Ϊʵ��ѭ�����������������п�����������(NH4)2S��ɳ��ӵ��� ��������ĸ��
a��Na2S b��K2S c��BaS
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com