
【题目】氯化亚铜是一种无机精细化工产品,实验室用蚀刻废液![]() 主要含
主要含![]() 、HCl等
、HCl等![]() 制备CuCl的实验流程如下.
制备CuCl的实验流程如下.

![]() 滤渣1的主要成分为 ______ ;还原时生成
滤渣1的主要成分为 ______ ;还原时生成![]() 的离子方程式为 ______ .
的离子方程式为 ______ .
![]() 加水时发生反应的离子方程式为 ______
加水时发生反应的离子方程式为 ______ ![]() 过滤时用的硅酸盐质仪器除烧杯外还有 ______
过滤时用的硅酸盐质仪器除烧杯外还有 ______ ![]() 滤液2的用途是 ______ .
滤液2的用途是 ______ .
![]() 用稀盐酸洗涤的目的是 ______ .
用稀盐酸洗涤的目的是 ______ .
【答案】铜粉 ![]()
![]() 漏斗和玻璃棒 返回到还原步骤,循环利用 减少CuCl溶解损失
漏斗和玻璃棒 返回到还原步骤,循环利用 减少CuCl溶解损失
【解析】
根据题中的流程可知,蚀刻废液![]() 主要含
主要含![]() 、HCl等
、HCl等![]() 中加入足量的铜粉及饱和氯化钠溶液,铜将
中加入足量的铜粉及饱和氯化钠溶液,铜将![]() 还原成
还原成![]() ,过滤掉未反应的铜粉,所以滤渣1为未反应的铜粉,在滤液中加足量的水,
,过滤掉未反应的铜粉,所以滤渣1为未反应的铜粉,在滤液中加足量的水,![]() 电离出氯离子得CuCl沉淀,过滤后将CuCl沉淀用稀盐酸洗涤,主要是减小CuCl在水中的溶解度,再用酒精洗涤,酒精易挥发,便于干燥,得到CuCl,滤液2中含有氯化钠和盐酸,可循环利用,据此答题。
电离出氯离子得CuCl沉淀,过滤后将CuCl沉淀用稀盐酸洗涤,主要是减小CuCl在水中的溶解度,再用酒精洗涤,酒精易挥发,便于干燥,得到CuCl,滤液2中含有氯化钠和盐酸,可循环利用,据此答题。
![]() 根据上面的分析可知,滤渣1的主要成分为铜粉,根据元素守恒和电荷守恒可知,还原时生成
根据上面的分析可知,滤渣1的主要成分为铜粉,根据元素守恒和电荷守恒可知,还原时生成![]() 的离子方程式为
的离子方程式为![]() , 故答案为:铜粉;
, 故答案为:铜粉;![]() ;
;
![]() 加水时发生反应的离子方程式为
加水时发生反应的离子方程式为![]() ,过滤时用的硅酸盐质仪器除烧杯外还有漏斗和玻璃棒,滤液2中含有氯化钠和盐酸,所以滤液2的用途是返回到还原步骤,循环利用, 故答案为:
,过滤时用的硅酸盐质仪器除烧杯外还有漏斗和玻璃棒,滤液2中含有氯化钠和盐酸,所以滤液2的用途是返回到还原步骤,循环利用, 故答案为:![]() ;漏斗和玻璃棒;返回到还原步骤,循环利用;
;漏斗和玻璃棒;返回到还原步骤,循环利用;
![]() 根据上面的分析可知,用稀盐酸洗涤的目的是减少CuCl溶解损失, 故答案为:减少CuCl溶解损失。
根据上面的分析可知,用稀盐酸洗涤的目的是减少CuCl溶解损失, 故答案为:减少CuCl溶解损失。


科目:高中化学 来源: 题型:
【题目】肼![]() 又称联氨,是一种可燃性的液体,可用作火箭燃料。
又称联氨,是一种可燃性的液体,可用作火箭燃料。
![]() 已知在101kPa时,
已知在101kPa时,![]() 时,
时,![]() 在氧气中完全燃烧生成氮气和水,放出624kJ的热量,则
在氧气中完全燃烧生成氮气和水,放出624kJ的热量,则![]() 的燃烧热的热化学方程式是_____________。
的燃烧热的热化学方程式是_____________。
![]() 下图是一个电化学过程示意图。
下图是一个电化学过程示意图。

![]() 图中甲池是_________
图中甲池是_________![]() 填“原电池”或“电解池”
填“原电池”或“电解池”![]() ,其电解质溶液为KOH溶液,则该池电极M的电极反应式是_________________________。
,其电解质溶液为KOH溶液,则该池电极M的电极反应式是_________________________。
![]() 乙池中石墨电极2的电极反应式是_________________________。 当石墨电极2上生成
乙池中石墨电极2的电极反应式是_________________________。 当石墨电极2上生成![]() 气体时
气体时![]() 标准状况下
标准状况下![]() ,转移的电子的数目为_________,则甲池理论上消耗标标准状况下的空气是________
,转移的电子的数目为_________,则甲池理论上消耗标标准状况下的空气是________![]() 假设空气中氧气体积含量为
假设空气中氧气体积含量为![]() 。
。
![]() 传统制备肼的方法,是以NaClO氧化
传统制备肼的方法,是以NaClO氧化![]() ,制得肼的稀溶液。该反应的离子方程式是_________。
,制得肼的稀溶液。该反应的离子方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列各小题:
Ⅰ.(1)理论上稀的强酸、强碱反应生成1molH2O(l)时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式__________________________。
(2)已知:乙苯催化脱氢制苯乙烯反应:![]() +H2(g)
+H2(g)
化学键 | C-H | C-C | C=C | H-H |
键能/kJmol-1 | 412 | 348 | 612 | 436 |
计算上述反应的△H=_________kJmol-1。
Ⅱ.25℃时,部分物质的电离平衡常数如表所示,请回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为_____________________________。
(2)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知BaSO4(s)![]() Ba2+(aq)+SO42﹣(aq),25℃时Ksp=1.07×10﹣10,且BaSO4的溶解度随温度升高而增大.如图所示,有T1、T2不同温度下两条BaSO4在水中的沉淀溶解平衡曲线,则下列说法不正确的是
Ba2+(aq)+SO42﹣(aq),25℃时Ksp=1.07×10﹣10,且BaSO4的溶解度随温度升高而增大.如图所示,有T1、T2不同温度下两条BaSO4在水中的沉淀溶解平衡曲线,则下列说法不正确的是
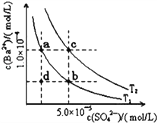
A. 温度为T1时,在T1曲线上方区域任意一点时,均有BaSO4沉淀生成
B. 蒸发溶剂可能使溶液由d点变为T1曲线上a、b之间的某一点
C. 升温可使溶液由b点变为d点
D. T2>25℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取金属镁的工艺流程可简单图示如下:

(1)步骤①的目的是将海水中的Mg2+沉淀为Mg(OH)2,若浓缩海水中c(Mg2+)=2.0 mol·L-1,Mg2+开始形成沉淀时溶液的pH约为________(已知Ksp[Mg(OH)2]=1.8×10-11,log3=0.48)
(2)步骤③的操作由蒸发浓缩,______,过滤,_______四个环节组成。
(3)步骤④是在HCl气流中加热晶体得到无水MgCl2,简要说明HCl气体的作用_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,一定量的石灰乳悬浊液中存在下列平衡:Ca(OH)2(s)![]() Ca(OH)2(aq)
Ca(OH)2(aq)![]() Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法中正确的是
Ca2+(aq)+2OH-(aq),当向此悬浊液中加入少量生石灰时,下列说法中正确的是
A. n (Ca2+)增大 B. c(Ca2+)不变
C. c(OH-)增大 D. n(OH-)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示的原电池,下列说法正确的是( )
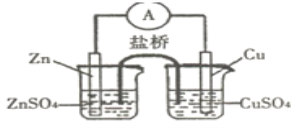
A.电子从锌电极通过电流表流向铜电极
B.盐桥中的阳离子向硫酸锌溶液中迁移
C.锌电极发生氧化反应,铜电极发生还原反应,其电极反应是2H+2e=H2↑
D.取出盐桥后,电流表仍会偏转,铜电极在反应前后质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示的实验装置和方法进行实验,能达到目的的是( )
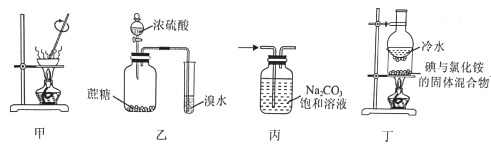
A.甲装置可将AlCl3溶液蒸干获得AlCl3晶体
B.乙装置可证明浓硫酸具有脱水性和氧化性
C.丙装置可除去CO2中的HCl
D.丁装置可将NH4Cl固体中的I2分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂用闪锌矿制备锌及颜料 A(红棕色固体)的工艺流程如下图所示。(闪锌矿的主要成分为 ZnS,同时含有 10%的 FeS 及少量 CuS)
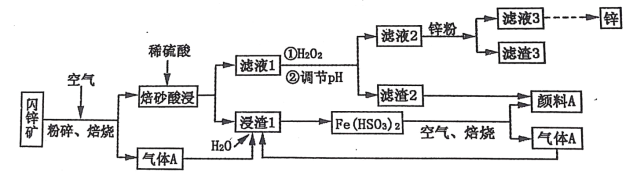
已知:①闪锌矿在焙烧时会生成副产物 ZnFeO4,ZnFeO4 不溶于水及硫酸。Fe(HSO3)2 难溶于水。②Ksp[Fe(OH)3]=1×10-39。
完成下列问题
(1)闪锌矿粉碎的目的是_______________________________________________________。
(2)“滤液 1”中选用足量的 H2O2,理由是_____________________。假设“②调节 pH"前,滤液 1 中 c(Fe3+)=1molL-1 ,则 Fe3+ 完全沉淀时的 pH 至少为____________________。(离子浓度≤ 10-6mol·L-1 规为完全除去)。
(3)“滤渣 3”的成分为__________________________________ (写化学式)。
(4)设计一种检验“颜料 A”中是否含有 Fe2+的实验方案_______________________________________________________。
(5)“气体 A”与“浸渣 1”反应的化学方程式为_______________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com