
【题目】在恒温、容积为2L的密闭容器中通入1molN2和xmolH2发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)。经过5min达到平衡时,混合气体的物质的量为3.6mol,容器内的压强变为原来的90%。试回答(请书写必要的计算步骤):
2NH3(g)。经过5min达到平衡时,混合气体的物质的量为3.6mol,容器内的压强变为原来的90%。试回答(请书写必要的计算步骤):
(1)起始时充入H2的物质的量_________;
(2)平衡时N2的浓度_______;
(3)5min内用NH3表示的化学反应速率__________。
【答案】 3mol 0.4mol/L 0.04mol/(L.min)
【解析】恒温恒容条件下,气体的压强之比等于其物质的量之比,反应达到平衡后,混合气体的物质的量为3.6mol,容器内的压强变为原来的90%,则反应前混合气体的物质的量为4mol;
(1)反应前混合气体的物质的量为4mol,为氢气和氮气的物质的量之和,氮气的物质的量为1mol,则氢气的物质的量为3mol;正确答案:3。
(2)达到平衡后,设参加反应的氮气的物质的量为x,
N2 + 3H2 2NH3 减少的物质的量
1 mol 3 mol 2mol
X 0.8mol (4-3.6)mol
1mol:2mol=x:(4-3.6)mol, x=1mol×(4-3.6)/2=0.2mol;平衡时N2的浓度(1-0.2)/2=0.4mol/L;正确答案:0.4mol/L;
(3)根据关系式可知:生成2mol NH3,减少的物质的量为2mol,现减少的物质的量为0.4mol,生成氨气0.4 mol,浓度为0.4/2=0.02 mol/L, 5min内用NH3表示的化学反应速率=0.2/5=0.04 mol/(L.min); 正确答案:0.04 mol/(L.min)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】五种短周期主族元素的部分信息如下表所示:
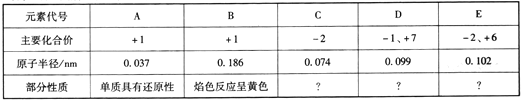
(1)E在元素周期表中的位置是____________________。
(2)在BDC溶液中滴加酚酞溶液,溶液先变红后褪色,原因是__________________(用离子方程式表示)。
(3)25℃时,pH均为10的BCA溶液和B2E溶液中,水电离出的c(OH-)之比为____________。
(4)下列事实中,能说明D的非金属性比E强的是________ (填字母)。
a.D的简单氢化物比E的稳定 b.AD的酸性比A2E的强
c.D的单质的沸点低于E的单质 d.D2与A2E能发生置换反应
(5)500℃时,向容积为1L的恒容密闭容器中充入2mol EC3气体,在催化剂作用下发生反应,经过10min恰好达到平衡,测得平衡浓度c(C2)=0.75mol·L-1。
①反应从开始到平衡时的平均反应速率v(EC2)=____________。
②EC3的平衡转化率为____________。
③其他条件不变,再向容器中充入少量EC3气体,则EC3的平衡转化率会________ (填“增大”“减小”或“不变”)。
(6)在B2E2C3溶液中滴加BAEC4溶液,会析出黄色沉淀并逸出刺激性气体,反应的离子方程式为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素①~⑩在周期表中的位置如表所示,试回答下列问题。
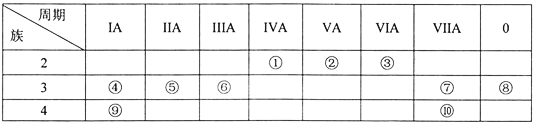
(1)上述10种元素中,化学性质最不活泼的是___(填元素符号,下同);与水反应最激烈的金属元素是___________。
(2)元素②的气态氢化物的分子式是_____;上述10种元素中,其最高价氧化物对应水化物的酸性最强的物质是_______(填化学式)。
(3)元素③与④形成的常用作供氧剂的化合物的电子式_________。
(4)①②⑤元素的原子半径由小到大的顺序为______(用元素符号表示);
请用一个化学方程式(或离子方程式)说明元素⑦和⑩非金属性的强弱:_____。
(5)④和⑥两元素的最高价氧化物对应的水化物相互反应的离子方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种气态烷烃和一种气态烯烃组成的混合气体共10g,其密度是相同条件下H2的12.5倍,该混合气通过Br2水时,Br2水增重8.4g,则组成该混合气的可能是( )
A.甲烷、乙烯
B.丙烷、乙烯
C.乙烷、丙烯
D.甲烷、丙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光刻胶是一种应用广泛的光敏材料,其合成路线如下(部分试剂和产物略去):
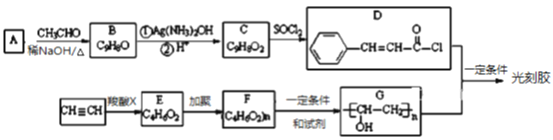
已知Ⅰ.![]() (R,R′为烃基或氢)
(R,R′为烃基或氢)
Ⅱ. ![]()
Ⅲ.![]() (R,R′为烃基)
(R,R′为烃基)
(1)写出A的结构简式_____________、C的结构简式:_____________。
(2)由B生成C的反应试剂还可以选用_____________________。
(3)由B到C的反应类型为_____________。由F到G的反应类型为_____________。
(4)D和G反应生成光刻胶的化学方程式为_________________________________________________。
(5)写出由A生成B的化学反应方程式:___________________________________________________。
(6)C的一种同分异构体满足下列条件:
①能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应;
②苯环上的一氯取代产物只有两种。写出该同分异构体的结构简式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数为z的元素R,在周期表中它位于A、B、C、D四种元素的中间,如图所示,A、B、C、D 4种元素的原子序数之和为下列数据,其中不可能是
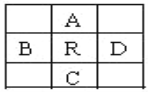
A. 4Z B. 4Z+10 C. 4Z+5 D. 4Z+14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列说法不正确的是( )
A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
B.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
C.屠呦呦提取青蒿素加入乙醚萃取,此过程属于化学变化
D.“春蚕到死丝方尽,蜡炬成灰泪始干”诗句中涉及化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》中“烧酒”条目为:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”是指
A.蒸馏B.萃取C.过滤D.升华
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.对于4FeS2+11O2═2Fe2O3+8SO2,试回答有关的问题:
(1)常选用哪些物质浓度的变化来表示该反应的速率____________;
(2)为了提高生成SO2的速率,可以采取的措施是______________;
A.增加FeS2的量 B.增大O2的浓度 C.升高温度 D.减小压强
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0﹣3分钟各物质的量的变化情况如图所示(A,B,C均为气体)
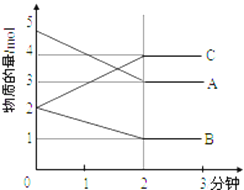
(3)该反应的化学方程式为_________________;
(4)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是_______________
A.气体总质量保持不变
B.A、B、C的浓度都相等
C.A、B、C的浓度不再发生变化
D.A、B、C的分子数之比为2:1:2
E.正反应和逆反应都已停止
F.容器内气体密度不再发生变化.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com