
【题目】下列为实验室常用仪器
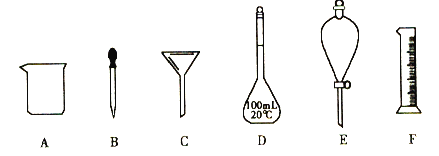
(1)下列各组混合物中,能用仪器E进行分离的是____________。
a.水和四氯化碳 b.碘和酒精 c.水中的泥沙
(2)配制100mL0.1mol·L-1NaOH溶液,所需NaOH固体的质量是_______g,实验中用到的四种仪器为_________________(填序号),还缺少的一种玻璃仪器为______________(填仪器名称)。
科目:高中化学 来源: 题型:
【题目】某校合作学习小组的同学设计实验验证钠在二氧化碳中燃烧的产物。回答下列问题:
(1)甲组同学利用下列装罝制取干燥纯净的二氧化碳。仪器X的名称是________________,装置B中盛装的试剂是_________________。

(2)乙组同学利用甲组制得的CO2并选用下列装置(可重复使用)验证钠在二氧化碳中燃烧的产物中是否含有CO。

①F中盛装的试剂是__________________。
②装置正确的连接顺序为C→_______→______→______→E→_______→_______H。
③证明燃烧的产物中含有CO的现象是_______________。
(3)丙组同学取乙组同学在G装置中所得的固体于试管中,加入足量稀盐酸,有气体产生且试管底部有黑色不溶物,则固体产物中一定有__________________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 碳酸氢钠溶液与少量澄清石灰水反应:HC![]() +Ca2++OH-CaCO3↓+H2O
+Ca2++OH-CaCO3↓+H2O
B. 氯化铵与氢氧化钠两种溶液混合加热:N![]() +OH-
+OH-![]() H2O+NH3↑
H2O+NH3↑
C. 钠和冷水反应:Na+2H2ONa++2OH-+H2↑
D. 向氯化铝溶液中滴加过量氨水:Al3++3OH-Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列说法不正确的是
A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
B.“青蒿一握,以水二升渍,绞取汁”,诗句中屠呦呦对青蒿素的提取属于化学变化
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D.“春蚕到死丝方尽,蜡炬成灰泪始干” 诗句中涉及氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.1mol 羟基所含的电子数为7NA
B.9.2 克甲苯含有的C﹣H 数目为0.8NA
C.28g 聚乙烯含有的碳原子数为2nNA
D.1mol 乙醇催化氧化生成乙醛时转移的电子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是( )
A.苯酚钠溶于醋酸溶液:C6H5O﹣+H+→C6H5OH
B.用稀硝酸除去试管内壁银:Ag+2H++NO3﹣═Ag++NO2↑+H2O
C.酯的水解反应:CH3CH2OOCCH3+H218O ![]() CH3CH2OH+CH3CO18OH
CH3CH2OH+CH3CO18OH
D.乙醛的银镜反应:CH3CHO+2Ag(NH3)2OH ![]() CH3COO﹣+NH4++2Ag↓+3NH3+H2O
CH3COO﹣+NH4++2Ag↓+3NH3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是进行化学研究的重要手段之一。请回答下列问题:
(1)实验室需要450 mL 1 mol·L-1硫酸溶液。
①配制1 mol·L-1的硫酸时,下列仪器肯定不需要的是_________(填标号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器有________________。
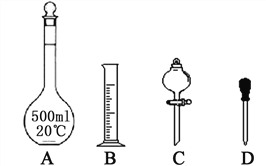
②在容量瓶的使用方法中,下列操作正确的是_______(填写序号)。
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制硫酸溶液时,用量筒量取浓硫酸后用玻璃棒引流注入容量瓶中,然后加水。
(2)如图装置中,若A中盛有品红溶液,B中盛有氢氧化钠溶液。
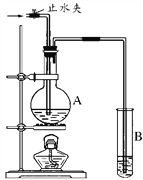
①向A中通入足量的SO2气体,然后加热,A中的现象_____________。
②向A中通入足量的Cl2气体,然后加热,A中的现象是_____________。
③若将SO2和Cl2按1:1体积比(同温同压)同时通入A中,则溶液不褪色。原因是SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是______________________。
(3)若(2)中的A中盛的是浓硫酸,加入足量的锌后,关闭止水夹并加热,进入B溶液的气体的化学式为____________;B中发生反应的离子方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成导电高分子材料PPV 的反应: ![]()
下列说法正确的是( )
A.合成PPV 的反应为加聚反应
B.PPV 与聚苯乙烯具有相同的重复结构单元
C.![]() 和苯乙烯互为同系物
和苯乙烯互为同系物
D.通过质谱法测定PPV 的平均相对分子质量,可得其聚合度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米磁性流体材料广泛应用于减震、医疗器械、声音调节等高科技领域。下图是制备纳米Fe3O4磁流体的两种流程:

(1)分析流程图中的两种流程,其中______(填“流程1”、“流程2”)所有反应不涉及氧化还原反应。步骤①反应的离子方程式为____________。
(2)步骤②保持50℃ 的方法是_____________。
(3)步骤③中加入的H2O2电子式是_______,步骤③制备Fe3O4磁流体的化学方程式为_______。
(4)流程2中FeCl3和FeCl2制备Fe3O4磁流体,理论上FeCl3和FeCl2物质的量之比为_____。己知沉淀B为四氧化三铁.步骤⑤中操作a具体的步骤是____________。
(5)利用K2Cr2O7可测定Fe3O4磁流体中的Fe2+含量。若Fe3O4磁流体与K2Cr2O7充分反应消耗了0.01mol·L -1的K2Cr2O7标准溶液100mL,则磁流体中含有Fe2+的物质的量为______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com