
【题目】实验是进行化学研究的重要手段之一。请回答下列问题:
(1)实验室需要450 mL 1 mol·L-1硫酸溶液。
①配制1 mol·L-1的硫酸时,下列仪器肯定不需要的是_________(填标号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器有________________。
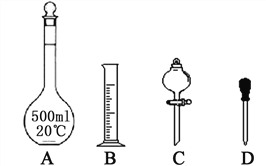
②在容量瓶的使用方法中,下列操作正确的是_______(填写序号)。
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制硫酸溶液时,用量筒量取浓硫酸后用玻璃棒引流注入容量瓶中,然后加水。
(2)如图装置中,若A中盛有品红溶液,B中盛有氢氧化钠溶液。
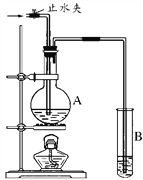
①向A中通入足量的SO2气体,然后加热,A中的现象_____________。
②向A中通入足量的Cl2气体,然后加热,A中的现象是_____________。
③若将SO2和Cl2按1:1体积比(同温同压)同时通入A中,则溶液不褪色。原因是SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是______________________。
(3)若(2)中的A中盛的是浓硫酸,加入足量的锌后,关闭止水夹并加热,进入B溶液的气体的化学式为____________;B中发生反应的离子方程式__________________________________________。
【答案】 C 烧杯、玻璃棒 a 先褪色,加热又变红 褪色,加热无明显现象 SO2+Cl2+2H2O=4H++SO42-+2Cl- SO2、H2 SO2+2OH-=SO32-+H2O或SO2+OH-=HSO3-
【解析】(1)①配制450 mL 1 mol·L-1的硫酸时需要量筒、烧杯、玻璃棒、胶头滴管和500mL容量瓶,因此肯定不需要的是分液漏斗,答案选C;所以除图中已有仪器外,配制上述溶液还需要的玻璃仪器有烧杯、玻璃棒。②a.使用容量瓶前检验是否漏水,a正确;b.容量瓶用水洗净后,不能再用待配溶液洗涤,b错误;c.配制硫酸溶液时,用量筒量取浓硫酸后先在烧杯中稀释,冷却后用玻璃棒引流注入容量瓶中,然后加水,c错误;答案选a;(2)①由于二氧化硫的漂白是不稳定的,所以向A中通入足量的SO2气体,然后加热,A中的现象是先褪色,加热又变红色。②氯气溶于水生成的次氯酸具有强氧化性,其漂白是不可逆的,所以向A中通入足量的Cl2,然后加热,A中的现象是褪色,加热无明显现象。③若将SO2和Cl2按1:1体积比(同温同压)同时通入A中,则溶液不褪色。原因是SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化生成硫酸,该反应的离子方程式是SO2+Cl2+2H2O=4H++SO42-+2Cl-。(3)若(2)中的A中盛的是浓硫酸,加入足量的锌后,关闭止水夹并加热,开始生成二氧化硫,随着反应的进行,浓硫酸变为稀硫酸,稀硫酸与锌反应生成氢气,因此进入B溶液的气体的化学式为SO2、H2;二氧化硫与氢氧化钠溶液反应,则B中发生反应的离子方程式为SO2+2OH-=SO32-+H2O或SO2+OH-=HSO3-。


科目:高中化学 来源: 题型:
【题目】利用废碱渣(主要成分为Na2CO3)处理硫酸厂尾气中的SO2,可制得无水Na2SO3(成品),其流程如图所示。
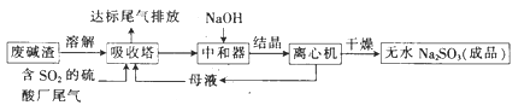
(1)某硫酸厂排放出的尾气中SO2的含量特别髙,而废碱渣的量不足,此时“吸收塔”内发生反应的离子方程式为_______________(不考虑H2O与SO2反应)。
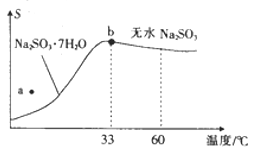
(2)亚硫酸钠的溶解度曲线如图所示,则上述流程中“结晶”的方法是___________(填“蒸发结晶”或“降温结晶”),图中a点所示分散系类别为____________(填“浊液”“胶体”或“溶液”)。
(3)仅用BaCl2、H2O2和过量稀盐酸的混合溶液难以检出“成品”中的SO32-,原因是“成品”中含有某种杂质阴离子。
①该杂质阴离子为________________(填离子符号)。
②25℃时,部分钡盐的Ksp如下表所示。
化学式 | BaSO4 | BaSO3 |
Ksp | 1.1×10-10 | 5.5×10-7 |
将得到的“成品”溶于水,测得溶液中SO32-的浓度为0.5mol L-1,为杂质阴离子浓度的10倍,向该溶液中加入等体积、0.5mol·L-1的BaCl2溶液,充分反应后c(Ba2+)=_______mol L-1。(混合时溶液体积的变化忽略不计)
(4)某同学采用如下方法检验SO32-:
![]()
①洗涤时使用的试剂最好为____________(填字母)。
a.稀HNO3 b.蒸馏水 c.稀H2SO4
②根据上述流程中的数据(w、x、y)_____________ (填“能”或“不能”)计算出成品试样中SO32-的百分含量,若能,则SO32-的百分含量为 (若不能,则此空不填);若不能,则理由是_____________(若能,则此空不填)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如果反应4P + 3KOH + 3H2O === 3KH2PO2 + PH3中转移0.6mol电子,消耗KOH的质量为( )
A. 5.6克 B. 16.8克 C. 33.6克 D. 100.8克
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为实验室常用仪器
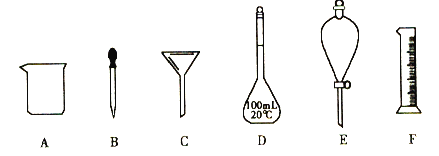
(1)下列各组混合物中,能用仪器E进行分离的是____________。
a.水和四氯化碳 b.碘和酒精 c.水中的泥沙
(2)配制100mL0.1mol·L-1NaOH溶液,所需NaOH固体的质量是_______g,实验中用到的四种仪器为_________________(填序号),还缺少的一种玻璃仪器为______________(填仪器名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验结果与图像不相符的是
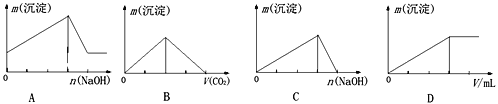
A. 向含有盐酸、氯化镁和氯化铝的溶液中逐渐加入氢氧化钠溶液直至过量
B. 向澄清石灰水中通入二氧化碳气体直至过量
C. 向氯化铝的溶液中逐渐加入氢氧化钠溶液直至过量
D. 向氯化铝的溶液中逐渐加入氨水直至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成聚丙烯腈纤维的单体是丙烯腈,它可由以下两种方法制备:
方法一:CaCO3﹣→CaO ![]() CaC2
CaC2 ![]() CH≡CH
CH≡CH ![]() CH2═CH﹣CN
CH2═CH﹣CN
方法二:CH2═CH﹣CH3+NH3+ ![]() O2
O2 ![]() CH2═CH﹣CN+3H2O
CH2═CH﹣CN+3H2O
对以上两种途径的分析中,正确的是( )
①方法二比方法一反应步骤少,能源消耗低,成本低
②方法二比方法一原料丰富,工艺简单
③方法二比方法一降低了有毒气体的使用量,减少了污染
④方法二需要的反应温度高,耗能大.
A.①②③
B.①③④
C.②③④
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)
选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
A | CO2(HCl) | 饱和碳酸钠溶液 | 洗气 |
B | CO2(CO) | O2 | 点燃 |
C | CuSO4(FeSO4) | Cu | 过滤 |
D | NaCl(Na2CO3) | 盐酸 | 蒸发结晶 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
A. 标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA
B. 某密闭容器盛0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA
C. 1 mol Na与足量O2在一定条件下完全反应时转移电子数为NA
D. 1 mol·L-1Na2SO4溶液中,Na+和SO![]() 离子数的总和一定为3NA
离子数的总和一定为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图装置进行实验,可证明碳和浓硫酸反应放出气体SO2和CO2。
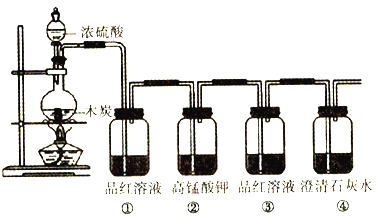
(1)木炭与浓H2SO4反应的化学方程式是_________________________________________,该反应的氧化剂为_______________,当转移2mol电子时,生成标准状况下的SO2和CO2共_______L。
(2)洗气瓶①、②中溶液褪色,体现二氧化硫的性质依次为_________(填序号)。
a.氧化性、还原性 b.漂白性、还原性 c.漂白性、氧化性 d.还原性、漂白性
(3)证明二氧化碳存在的现象为_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com