
【题目】将0.4 g NaOH和1.06 g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )
A.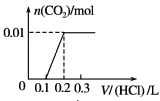 B.
B.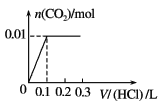
C.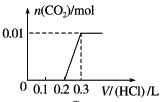 D.
D.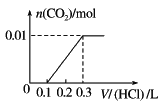
【答案】C
【解析】
NaOH和Na2CO3的混合溶液中,加入盐酸,H+先和OH-反应,再和CO32-反应,但是CO32-与H+反应先生成HCO3-,HCO3-与H+反应生成CO2和H2O。
NaOH和Na2CO3的混合溶液中,加入盐酸,H+先和OH-反应,再和CO32-反应;先后发生的反应的离子方程式为H++OH-=H2O,H++CO32-=HCO3-,HCO3-+H+=CO2↑+H2O,只有最后一个反应,有气体生成。
0.4g NaOH,其物质的量为0.01mol,消耗的HCl的物质的量为0.1mol,体积为![]() ;1.06 g Na2CO3,其物质的量为0.01mol,CO32-与H+反应先生成HCO3-,消耗的HCl的物质的量为0.01mol,体积为
;1.06 g Na2CO3,其物质的量为0.01mol,CO32-与H+反应先生成HCO3-,消耗的HCl的物质的量为0.01mol,体积为![]() ;HCO3-与H+反应生成CO2和H2O,消耗的HCl的物质的量为0.01mol,体积为
;HCO3-与H+反应生成CO2和H2O,消耗的HCl的物质的量为0.01mol,体积为![]() ,同时生成0.01molCO2;只有最后一个反应,有气体生成,因此开始消耗了0.2L盐酸溶液,没有气体生成,随后消耗0.1L盐酸溶液,生成0.01molCO2,图像C符合;
,同时生成0.01molCO2;只有最后一个反应,有气体生成,因此开始消耗了0.2L盐酸溶液,没有气体生成,随后消耗0.1L盐酸溶液,生成0.01molCO2,图像C符合;
答案选C。


科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是
A.5.6g铁在足量氯气中燃烧,铁失去电子数为0.2NA
B.常温常压下,32gO2和O3的混合气体所含原子数为2NA
C.9g重水(2H216O)中含有的电子数为5NA
D.0.5 mol/L MgCl2溶液中,含有的Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A.常温常压下,8gO2含有8NA个质子
B.分子总数为NA的CO2和NO2混合气体中含有的氧原子数为2NA
C.标准状况下,22.4L盐酸含有NA个HC1分子
D.分子总数为NA的CO、N2混合气体体积约为22.4L,质量为28g
查看答案和解析>>
科目:高中化学 来源: 题型:
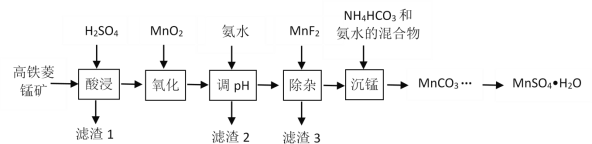
【题目】一水硫酸锰(MnSO4H2O)是一种重要的化工中间体,工业上可由高铁菱锰矿(主要成分为MnCO3,含有FeCO3、Al2O3、MgO、CaO、SiO2等杂质)制备,部分工艺流程如下:
相关金属离子[c(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的 pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 |
(1)“酸浸”时高铁菱锰矿需要粉碎,并进行充分搅拌,为提高锰的浸出率还可采取的措施有_________。(写出其中一种)
(2)“氧化”时发生反应的化学方程式为________。
(3)“调pH”范围至5~6,得到滤渣2的主要成分除MnO2外还有_________。
(4)“除杂”过程中加入MnF2的目的是_________。已知:Ksp(MgF2)=5.16×10-11,Ksp(CaF2)=5.3×10-9。
(5)“沉锰”过程中发生反应的离子方程式为_________。
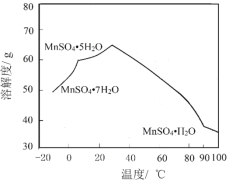
(6)MnSO4在水中的溶解度与温度关系如图。由MnCO3获得较纯净的MnSO4H2O 晶体的方法是:将MnCO3溶于_________,控制温度为_________以上结晶,得到MnSO4H2O晶体,洗涤、烘干。晶体烘干时温度不能过高的原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在室温下,下列各组离子一定能大量共存的是( )
A.滴入石蕊试液显红色的溶液:K+、Mg2+、AlO2、SO32
B.1.0mol·L1的KNO3溶液:H+、Fe2+、Cl、SO42
C.在![]() =1×1012的溶液中:NH4+、Fe2+、Cl-、NO3
=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3
D.通入足量CO2的溶液:Ca2+、Cl、K+、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 向50mL 1mol·L-1的盐酸中加入烧碱,水的KW不变
B. NH4Cl和NH3·H2O混合液中,二者对对方的平衡都起了抑制作用
C. 有两种弱酸HX和HY且酸性HX>HY,则体积和浓度相同的NaX和NaY溶液中有c(Y-)>c(X-)>c(OH-)>c(H+)
D. 常温0.1mol·L-1HA溶液中c(OH-)/ c(H+)=10-8,则0.01mol·L-1 HA溶液中c(H+)=1×10-4mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由重水D2O组成的水,D2O的离子积为1.6×10-15,可用pH一样定义规定pD= -lg{c(D+)},下列关于pD的叙述,正确的是( )
A. D2O呈中性,pD=7
B. 含0.01mol NaOD的D2O溶液1L,pD=12
C. 用D2O溶解0.1mol DCl成1L溶液,pD=2
D. 在100mL 0.25mol/L DCl溶液中加入50mL 0.2mol/L的NaOD的D2O溶液,pD=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A.7.2g CaO2固体中阴阳离子总数为0.3NA
B.密闭容器中2 mol NO与1mol O2充分反应,产物的分子数目为2NA
C.在一定条件下,6.4g铜与过量的硫反应,转移的电子数目为0.2NA
D.10g质量分数为46%的乙醇溶液中O-H键数目为0.7NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知C(s、金刚石)+O2(g)==CO2(g);ΔH= -395.4kJ/mol,C(s、石墨)+O2(g)==CO2(g);ΔH= -393.5kJ/mol。
①石墨和金刚石相比,石墨的稳定性______金刚石的稳定性。
②石墨中C-C键键能______金刚石中C-C键键能。(均填“大于”、“小于”或“等于”)。
(2)已知H—H键的键能为436 kJ·mol-1,Cl—Cl键的键能为243 kJ·mol-1,H—Cl键的键能为431 kJ·mol-1,则H2(g) +Cl2(g)=2HCl(g)的反应热为______。
(3)已知下列反应的反应热:
CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=-247.4 kJ·mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com