
【题目】小强同学利用图甲所示的裝置测定空气中氧气的含量,其中燃烧匙内的白磷用电加热装置点燃,瓶內气压用气体压强传感器测定,其变化如图乙所示,回答相关问题。
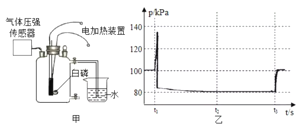
(1)下列关于图甲实验的说法正确的是(________)
A.实验前先检査装置气密性,再装入少量白磷
B.红磷燃烧,产生大量白雾,放热
C.甲装置密闭,可以减小空气污染
D.本实验可以证明空气含有N2、O2、CO2和稀有气体
(2)图乙中,t3时刻瓶内气压又显著增加,这是因为进行了一个实验操作,即___。
(3)小强同学对实验装置进行了改进:选用容积为45mL的试管做反应容器进行实验,如图丙所示。
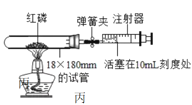
①实验前检查装置的气密性,具体操作为:组装好装置,打开弹簧夹,将活塞往前轻轻推一段距离,松手后,观察到___,则装置气密性良好。
②如果实验一切正常,则实验结束后打开弹簧夹,注射器活塞将从10mL刻度处慢慢前移到约___mL刻度处才停止。
【答案】C 冷却至室温,打开止水夹 活塞回到原位置 1
【解析】
(1)A.实验前先检查装置气密性,再装入足量红磷,确保氧气完全反应,故A不正确;
B.白磷燃烧,产生大量白烟,放热,故B不正确;
C.甲装置密闭,可以减小空气污染,故C正确;
D.本实验不能证明空气含有N2、CO2和稀有气体,故D不正确;
故答案为:C;
(2)乙中,t3时刻瓶内气压又显著增加,是因为进行了一个实验操作,即打开止水夹,水进入容器,故答案为:冷却至室温,打开止水夹;
(3)①组装好装置,打开弹簧夹,将活塞往前轻轻推一段距离,松手后,观察到活塞回到原位置,则装置气密性良好,故答案为:活塞回到原位置。
②注射器活塞将从10mL刻度处慢慢前移到约为:10mL-45mL×![]() =1mL刻度处才停止,故答案为1。
=1mL刻度处才停止,故答案为1。


科目:高中化学 来源: 题型:
【题目】实验室模拟合成氨和氨催化氧化的流程如图:

已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从图中选择制取气体的合适装置:氮气___、氢气___。
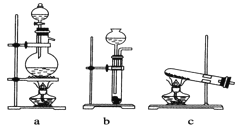
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有两个作用,分别是:___、___。

(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是___,锥形瓶中还可观察到的现象是___。
(4)写出乙装置中氨氧化的化学方程式:___。
(5)反应结束后锥形瓶内的溶液中除含有H+、OH-外,还含有___、___离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式和名称:
①1-溴丁烷与氢氧化钠乙醇溶液共热:_________________________________________________
②2-甲基-1,3-丁二烯与等物质的量的单质溴在60℃时发生1,4-加成反应:_________________
③甲苯制备TNT的反应:____________________________________________________
④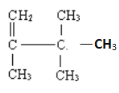 (用系统命名法命名) ____________________________________________
(用系统命名法命名) ____________________________________________
⑤ 2,6﹣二甲基﹣4﹣乙基辛烷(写出结构简式)_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3-甲基-1-溴丁烷和3-甲基-2-溴丁烷分别与NaOH的乙醇溶液共热,关于两反应的说法正确的是( )
A.产物相同,反应类型相同B.产物不同,反应类型相同
C.碳氢键断裂的位置相同D.碳溴键断裂的位置相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对教材中探究分子性质的实验(图1)进行了改进,如图2所示,试管丙中有一张每隔1cm滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的敞口小药瓶固定在橡皮塞上。关于图1图2中的实验有以下说法,其中正确的是( )
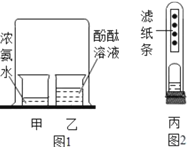
①图2比图1的实验减少了大气污染、更节约
②图1和图2的实验均能证明分子在不断运动
③图2中观察到的现象是滤纸条上的酚酞试液自上而下依次变红
④若另取与丙相同的装置浸入10℃的冷水中,则不能得出结论
A.①②B.①②④C.①②③④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下图两种化合物的结构或性质描述正确的是( )
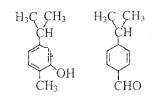
A.是同分异构体
B.分子中共平面的碳原子数一定相同
C.均能与溴水反应,不能使酸性高锰酸钾褪色
D.可用红外光谱区分,但不能用核磁共振氢谱区分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】漂白粉是常见的消毒剂,实验室可利用如图所示装置制取:
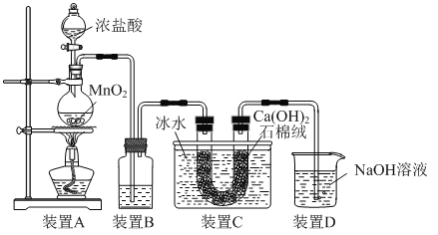
(1)装置A中所发生反应的化学方程式为_____。
(2)为除去挥发出的HCl,装置B中应装有_____。
(3)装置C中所发生反应的化学方程式为_____。
(4)装置D的作用是_____。
(5)有效氯含量是衡量次氯酸盐氧化能力的重要指标。次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量表示:Cl—+ClO—+2H+=Cl2+H2O[有效氯含量=![]() ×100%]。为测定装置C中所得漂白粉的有效氯含量,进行如下实验:准确称取装置C中所得漂白粉1.775g,将其与浓盐酸反应,所得Cl2在标准状况下的体积为0.112L。计算漂白粉的有效氯含量,并写出计算过程_____。
×100%]。为测定装置C中所得漂白粉的有效氯含量,进行如下实验:准确称取装置C中所得漂白粉1.775g,将其与浓盐酸反应,所得Cl2在标准状况下的体积为0.112L。计算漂白粉的有效氯含量,并写出计算过程_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化碘(IC13)在药物合成中用途非常广泛。已知ICl3熔点33℃,沸点73℃,有吸湿性,遇水易水解。某小组同学用下列装置制取ICl3(部分夹持和加热装置省略)。
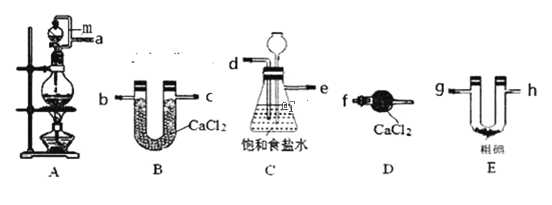
(1)按照气流方向连接接口顺序为a→___。装置A中导管m的作用是___。
(2)烧瓶中发生反应的离子方程式___,若移除酒精灯为了使反应能顺利进行烧瓶中可以放___。
(3)装置C用于除杂,同时作为安全瓶,能监测实验进行时后续装置是否发生堵塞,若发生堵塞C中的现象为___。
(4)氯气与单质碘需在温度稍低于70℃下反应,则装置E适宜的加热方式为___。装置E中发生反应的化学方程式为___。
(5)该装置存在的明显缺陷是___。
(6)粗碘的制备流程为:

操作Y用到的玻璃仪器有烧杯、___,操作Z的名称为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1—丙烯酯: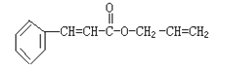 可简化为
可简化为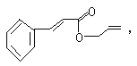 杀虫剂“阿乐丹”的结构表示为
杀虫剂“阿乐丹”的结构表示为 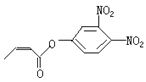 ,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
A.遇FeCl3溶液均显紫色B.均能发生银镜反应
C.均能与溴水发生反应D.均能与NaOH溶液发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com