
【题目】下列关于反应速率的说法中,错误的是( )
A.反应速率用于衡量化学反应的快慢
B.决定反应速率的主要因素是反应物的性质
C.可逆反应达到化学平衡时,正、逆反应速率都为零
D.化学反应中,纯液体物质不能计算其速率
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】下列关于![]() 键和
键和![]() 键的理解不正确的是
键的理解不正确的是![]()
A. ![]() 键可以绕键轴旋转,
键可以绕键轴旋转,![]() 键不能绕键轴旋转
键不能绕键轴旋转
B. ![]() 分子中的
分子中的![]() 键是
键是![]()
![]() 键,HClO分子中的
键,HClO分子中的![]() 键都是
键都是![]()
![]() 键
键
C. ![]() 分子和
分子和![]() 中都是含有5个
中都是含有5个![]() 键
键
D. ![]() 键以“头碰头”方式重叠,
键以“头碰头”方式重叠,![]() 键以“肩并肩”方式重叠
键以“肩并肩”方式重叠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅的单质、氧化物、盐在现代工业中有着重要用途。
I.(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4。Pb3O4与HNO3发生非氧化还原反应生成一种盐和一种铅氧化物,其反应的化学方程式为_____________________________。
II.以含铅废料(主要含Pb、PbO、PbO2、PbSO4)为原料制务高纯PbO,其主要流程如下:
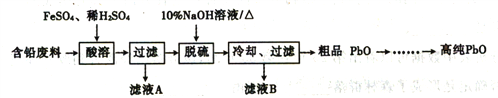
(2)“酸溶”时,在Fe2+催化下,Pb和PbO2反应生成1molPbSO4时转移电子的物质的量为____mol。
(3)已知:PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)=NaHPbO2(aq),其溶解度曲线如图所示:
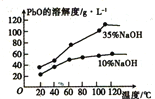
结合上述信息,完成由粗品PbO(所含杂质不溶于NaOH溶液)得到高纯PbO的操作:将粗品PbO溶解在一定量_________(填“35%”或“10%”)的NaOH溶液中,加热至110℃,充分溶解后,___________(填“趁热过滤”或“蒸发浓缩”),将滤液冷却结晶,过滤、洗涤并干燥得到高纯PbO固体。
(4)工业上利用硫化氢除去滤液A中少量的Pb2+,发生的反应为Pb2++H2S![]() PbS↓+2H+,该反应的平衡常数为_____________。(H2S的Ka1=1.5×10-7,Ka2=7.0×10-15,PbS的Ksp=8.4×10-28)
PbS↓+2H+,该反应的平衡常数为_____________。(H2S的Ka1=1.5×10-7,Ka2=7.0×10-15,PbS的Ksp=8.4×10-28)
(5)将粗品PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示:

①阴极的电极反应式为________________________;
②当有2.07gPb生成时,通过质子交换膜的n(H+)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素关于金属性或非金属性的强弱比较错误的一组是( )
A.金属性:K>NaB.金属性:B>Al
C.非金属性:Cl>PD.非金属性,F>O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 用惰性电极电解CuSO4溶液:2Cu2++4OH-![]() 2Cu+O2↑+2H2O
2Cu+O2↑+2H2O
B. 在Na2SiO3溶液中加入盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
C. 在稀硝酸中加入过量的铁屑: Fe+4H++NO3-=Fe3++NO↑+2H2O
D. 在NaHCO3溶液中加入过量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法正确的是

A. 离子半径的大小顺序:d<e<f
B. 与x形成简单化合物的沸点:y>z>d
C. 除去实验后试管中残留的g单质,可用热的氢氧化钠溶液
D. g、h的氧化物对应的水化物的酸性:h>g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于数以千万计的化学物质和如此丰富的化学变化,分类法的作用几乎是无可替代的。如:纯净物根据其组成和性质可进行如下分类。
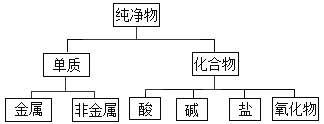
(1)如图所示的分类方法属于_______________。
(2)某化学兴趣小组对下列四组物质进行研究:
A.HCl、H2SO4、H2CO3、HNO3
B.Na2CO3、NaNO3、AgNO3、Ba(NO3)2
C.FeCl3溶液、蒸馏水、CaCO3悬浊液、Fe(OH)3胶体
D.NaOH、KOH、Ba(OH)2、Fe2O3
①填写下列空白:
A组 | B组 | C组 | D组 | |
分类标准 | 含氧酸 | ________ | 分散系 | ________ |
不属于该类别的物质 | ________ | Na2CO3 | ________ | Fe2O3 |
②写出①表中发生反应的化学方程式:
A+ B→气体__________________________;A+D__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com