
【题目】下列关于金属冶炼的说法正确的是
A.由于铝的金属性强,故工业上采用电解熔融AlCl3的方法生产单质铝
B.将钠投入氯化镁饱和溶液中,可置换出镁单质
C.根据金属的活泼性不同,采用不同的金属冶炼方法
D.铝热反应需要在高温下进行,是一个典型的吸热反应
科目:高中化学 来源: 题型:
【题目】某学生的实验报告所列出的下列数据中合理的是( )
A. 用10mL量筒量取7.13mL稀盐酸
B. 用pH计测得某稀盐酸的pH为1.54
C. 用碱式滴定管量取烧碱溶液20.3 mL
D. 用托盘天平称得某物质的质量为13.15g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL、0.1mol/L的NaOH溶液中加入0.1mol/L的HA溶液,溶液pH的变化曲线如图所示。下列说法正确的是( )
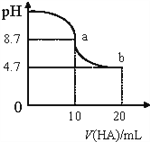
A. pH=7时,c(Na+)= c(A-)+c(HA)
B. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
C. b点所示溶液中:c(A-)>c(HA)
D. a、b两点所示溶液中水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有以下6个反应(反应条件略):
A.2Na+2H2O ═2NaOH+H2↑ B.CH4+2O2 ![]() CO2+2H2O
CO2+2H2O
C.KClO3![]() 2KCl+3O2↑ D.CaCO3+2HCl═CaCl2+H2O+CO2↑
2KCl+3O2↑ D.CaCO3+2HCl═CaCl2+H2O+CO2↑
E.Na2O+CO2 ═Na2CO3 F.CO2+C![]() 2CO
2CO
既属于化合反应又属于氧化还原反应的有__________(填编号,下同),不属于氧化还原反应的有__________.
(2)根据反应:①2Fe3++2I-===2Fe2++I2,②Br2+2Fe2+===2Fe3++2Br-,③ Br2+2I-===I2+2Br-,回答下列问题。
①试判断离子的还原性由强到弱的顺序是________
A.Br-、Fe2+、I- B.I-、Fe2+、Br- C.Br-、I-、Fe2+ D.Fe2+、I-、Br-
②某溶液中含有Br-、Fe2+、I-,为了氧化I-而不影响Br-和Fe2+,选用的氧化剂是__________;
③I2与Br-能否发生反应________
A.能 B.不能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,探究铜与稀HNO3,反应过程如下:
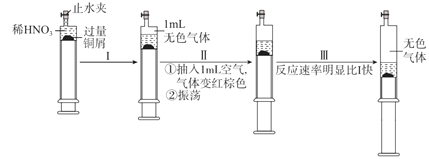
下列说法不正确的是
A. 过程I中生成无色气体的离子方程式是3Cu+2 NO3-+8H+ =3Cu2++2NO↑+4H2O
B. 步骤III反应速率比I快的原因是NO2溶于水,使c(HNO3)增大
C. 由实验可知,NO2对该反应具有催化作用
D. 当活塞不再移动时,再抽入空气,铜可以继续溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应KMn04+ HCl—KC1+ MnCl2+Cl2+ H20(未配平),若有0.1 mol KMn04参加反应,下列说法正确的是 ( )
A. 转移0.5 mol电子 B. 生成0.5 mol Cl2
C. 参加反应的HC1为1.6 mol D. Cl2是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0. 10 mol·L-1的Na2CO3溶液中逐滴加入稀盐酸,加入的HCl与原溶液中Na2CO3的物质的量之比f[f=![]() ]与混合液pH的关系如图所示。下列说法正确的是
]与混合液pH的关系如图所示。下列说法正确的是
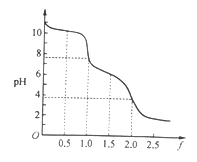
A. f=0时,溶液中:c(Na+)=2c(CO32-)
B. f=0.5时,溶液中:c(HCO3-)>c(CO32-)
C. f= 1时,溶液中:c(Na+) + c(H+) = 2c(CO32-) + c(HCO3-)+c(OH-)
D. f=2时,溶液中:1/2c(Na+)=c(CO32-)+c( HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表前四周期的一部分,下列有关R、W、X、 Y、Z五种元素的叙述中,正确的是( )
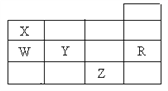
A. 通常情况下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. W的电负性比X的的电负性大
D. 第一电离能:R>W>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质X的结构简式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体。下列关于物质X的说法正确的是
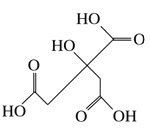
A.X分子式为C6H7O7
B.1 mol物质X可以和3 mol氢气发生加成
C.X分子内所有原子均在同一平面内
D.足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体物质的量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com