
【题目】现有A、B、C、D四种气体,A是密度最小的气体,B在通常情况下呈黄绿色,把四种气体分别通入酸性硝酸银溶液中,通入B、D气体时立即出现白色沉淀,纯净的A可以在B中安静地燃烧,发出苍白色的火焰并生成D.把无色无刺激气味气体C通入澄清石灰水时变浑浊.
(1)A、B、C、D的分子式分别为:ABCD .
(2)写出下列各反应的化学方程式: A与B;B与水;B与NaOH溶液;C与澄清石灰水 .
【答案】
(1)H2;Cl2;CO2;HCl
(2)H2+Cl2 ![]() 2HCl;Cl2+H2O?HCl+HClO;Cl2+2NaOH═NaCl+NaClO;CO2+Ca(OH)2═CaCO3↓+H2O
2HCl;Cl2+H2O?HCl+HClO;Cl2+2NaOH═NaCl+NaClO;CO2+Ca(OH)2═CaCO3↓+H2O
【解析】解:A是密度最小的气体,应为H2 , B在通常情况下呈黄绿色,应为Cl2 , 纯净的A可以在B中安静地燃烧,发出苍白色的火焰并生成D,生成HCl,则D为HCl,把无色无刺激气味气体C通入澄清石灰水时变浑浊,应为CO2 , (1)由以上分析可知A为H2 , B为Cl2 , C为CO2 , D为HCl,所以答案是:H2;Cl2;CO2;HCl;(2)氢气在点燃条件下与氯气反应生成氯化氢,方程式为H2+Cl2 ![]() 2HCl,氯气与水反应生成盐酸和次氯酸,反应的方程式为Cl2+H2OHCl+HClO, 氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的方程式为Cl2+2NaOH═NaCl+NaClO,二氧化碳与澄清石灰水反应生成碳酸钙和水,反应的方程式为,
2HCl,氯气与水反应生成盐酸和次氯酸,反应的方程式为Cl2+H2OHCl+HClO, 氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的方程式为Cl2+2NaOH═NaCl+NaClO,二氧化碳与澄清石灰水反应生成碳酸钙和水,反应的方程式为,
所以答案是:H2+Cl2 ![]() 2HCl;Cl2+H2OHCl+HClO;Cl2+2NaOH═NaCl+NaClO;CO2+Ca(OH)2═CaCO3↓+H2O.
2HCl;Cl2+H2OHCl+HClO;Cl2+2NaOH═NaCl+NaClO;CO2+Ca(OH)2═CaCO3↓+H2O.


科目:高中化学 来源: 题型:
【题目】1mol CH2=CH2与Cl2完全发生加成反应后,再与Cl2彻底取代,两过程共消耗Cl2的物质的量为( )
A. 2mol B. 4mol C. 5mol D. 6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A. 0.1 mol/L Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S)
B. 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c (Na+)>c(CO32-)>c(HCO3-)>c(OH-) >c(H+)
C. 常温下,pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):①>②>③
D. 将CH3COONa溶液从20℃升温至30℃,溶液中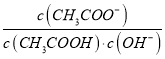 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学通过实验研究钠及其化合物的有关性质,请回答相关问题.
(1)实验室中少量的钠通常保存在 中,在实验室中取用钠的仪器是 .
(2)若将钠在空气中加热,钠会燃烧发出黄色火焰,同时生成 色的固体,写出该产物与H2O反应的化学方程式: .
(3)将金属钠投入水中,发生反应的离子方程式为
(4)该同学在实验室欲配制500mL0.1mol/L NaOH溶液. ①配制溶液时肯定不需要如图所示仪器中的(填字母),配制上述溶液还需要用到的玻璃仪器是(填仪器名称).
②根据计算,该同学应用托盘天平称取NaOH的质量为 .
③该同学将所配制的NaOH溶液进行测定,发现浓度大于0.1mol/L.下列操作会引起所配浓度偏大的是 .
A.烧杯未进行洗涤
B.配制前,容量瓶中有少量蒸馏水
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
D.往容量瓶转移时,有少量液体溅出
E.在容量瓶中定容时俯视容量瓶刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.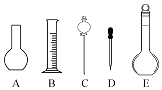
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学计量在化学中占有重要地位.根据计算填空:
(1)1.204×1022个NH3分子的物质的量为 , 在标准状况下的体积为mL.
(2)含0.4mol Fe3+的Fe2(S04)3中含SO42﹣的物质的量为 .
(3)已知8gX与10gY恰好完全反应生成0.02mol Z和15.88g W,则Z的摩尔质量为 .
(4)某混合溶液中只含有下列几种离子(不考虑水的电离):Na+、Mg2+、Cl﹣、SO42﹣ , 若Na+、Mg2+、Cl﹣的物质的量浓度依次为0.2mol/L、0.25mol/L、0.5mol/L,则(SO42﹣)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】17克NH3共有mol原子,0.1molH2S共有个氢原子;同质量的NH3和H2S中分子个数比为 . 在标准状况下,35.5g氯气的体积是 L,将其与氢气完全化合,需氢气的物质的量是mol,将生成的气体配制成1L溶液,溶质的物质的量浓度是molL﹣1 , 将此溶液取出20mL加蒸馏水制成200mL溶液,此冲稀后溶液中溶质的物质的量浓度是molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.标准状况下,22.4 L水中含有6.02×1023个水分子
B.32 g氧气所含的原子数目为2×6.02×1023
C.常温常压下,0.5×6.02×1023个一氧化碳分子所占的体积是11.2 L
D.1 molCaCl2溶于水配成1 L溶液,所得溶液中Cl﹣的物质的量浓度为1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题: 
(1)该注射液中葡萄糖的质量分数为;
(2)该注射液中葡萄糖的物质的量浓度为 . (保留两位小数)
(3)检测人的血液中葡萄糖(简称血糖,相对分子质量为180)的含量,参考指标常以两种计量单位表示,即“mmol/L”和“mg/dL”(1L=10dL).以“mmol/L”表示时,人的血糖正常值在3.61~6.11mmol/L之间.如果以“mg/dL”表示,血糖正常值范围是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池在通讯,交通及日常生活中有着广泛的应用。
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为Cd+2NiO(OH)+2H2O![]() 2Ni(OH)2+Cd(OH)2。已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是__________。
2Ni(OH)2+Cd(OH)2。已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是__________。
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
A.①③ B.②④ C.①④ D.②③
(2)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重。这是因为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com