
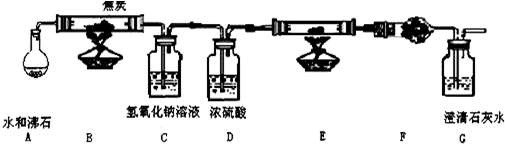
| ||
| ||
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
| A、一定温度下,弱酸的电离常数越大,酸性越强 |
| B、醋酸的电离常数K.和醋酸钠的水解常数之间的关系为:Ka?Kh=Kw |
| C、平衡常数只受温度影响,与反应物或生成物的浓度变化无关 |
| D、合成氨的反应,正反应的平衡常数和逆反应的平衡常数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
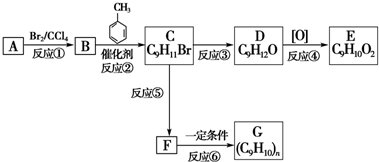
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:
| 相关信息 | |
| W | W原子基态时最外层电子数是其内层电子数的2倍 |
| X | X原子基态时2p原子轨道上有3个未成对电子 |
| Y | Y的基态原子最外层电子排布式为:3s1 |
| Z | Z的原子序数为26 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

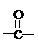 的异构体的数目有
的异构体的数目有查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 金属是一种重要的材料,人类的生活和生产都离不开金属.如图表示了金属活动性顺序表中的铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.
金属是一种重要的材料,人类的生活和生产都离不开金属.如图表示了金属活动性顺序表中的铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com