
| A、所有酸中,二氧化硅只与氢氟酸反应,可用石英制造耐酸容器 |
| B、工业上金属Mg、Al都是用电解其熔融的氯化物制得的 |
| C、二氧化氯具有氧化性,可用于自来水的杀菌消毒 |
| D、若铁制品表面的钢镀层有破损,会加快铁制品腐蚀 |


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
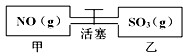 如图,容积相等的甲乙两个容器,通过活塞相连,分别充入NO和SO3且使气体密度相等.打开活塞使气体充分混合,发生反应:SO3(g)+NO(g)?SO2(g)+NO2(g)并达到平衡.反应过程中两容器的温度恒定且相等.则打开活塞前后,容器甲中保持不变的是( )
如图,容积相等的甲乙两个容器,通过活塞相连,分别充入NO和SO3且使气体密度相等.打开活塞使气体充分混合,发生反应:SO3(g)+NO(g)?SO2(g)+NO2(g)并达到平衡.反应过程中两容器的温度恒定且相等.则打开活塞前后,容器甲中保持不变的是( )| A、气体的密度 |
| B、气体分子数 |
| C、气体压强 |
| D、气体平均摩尔质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶刚用蒸馏水洗净,没有烘干 |
| B、没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中 |
| C、定容时滴加蒸馏水先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切 |
| D、定容时仰视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、② | B、④ | C、⑥ | D、⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
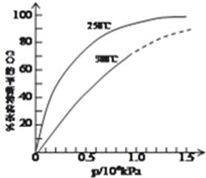 在容积可变的密闭容器中,由CO和H2合成甲醇CO(g)+2H2(g)═CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示.
在容积可变的密闭容器中,由CO和H2合成甲醇CO(g)+2H2(g)═CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
A、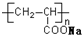 表示一种吸水性高分子树脂 表示一种吸水性高分子树脂 |
| B、用于现代建筑的钢筋混凝土不属于复合材料 |
| C、pH=2的盐酸和NH4Cl溶液中,水电离出的c(H+)相等 |
| D、常温时铝遇浓硝酸钝化,是由于铝元素有很强的金属性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com