
【题目】请写出相应化学方程式,并写出前三个反应的反应类型。
(1)乙烯水化法制乙醇:_______________;反应类型:__________________________。
(2)溴乙烷在氢氧化钠醇溶液中加热:_______________;反应类型:__________________________。
(3)苯与液溴在一定条件下反应:___________________________(注明条件);反应类型:__________________________。
(4)苯酚钠与少量二氧化碳的反应:_________________。
(5)乙醛与银氨溶液反应制银镜:______________________。
【答案】CH2===CH2+H2O![]() CH3CH2OH 加成反应 CH3CH2Br+NaOH
CH3CH2OH 加成反应 CH3CH2Br+NaOH![]() CH2===CH2↑+NaBr+H2O 消去反应
CH2===CH2↑+NaBr+H2O 消去反应 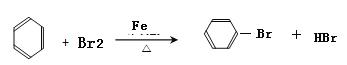 取代反应 C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 CH3CHO+2Ag(NH3)2OH
取代反应 C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H2O
CH3COONH4+2Ag↓+3NH3+H2O
【解析】
(1)乙烯不饱和的C=C双键,其中1个C-C断裂结合水提供的-H、-OH,发生加成反应;
(2)CH3CH2Br在NaOH的乙醇溶液中加热发生消去反应,生成乙烯;
(3)苯与液溴在一定条件下发生取代反应生成溴苯;
(4)碳酸的酸性强于苯酚,苯酚钠与少量二氧化碳的反应生成碳酸氢钠和苯酚;
(5)乙醛与银氨溶液反应制银镜,还生成乙酸铵、氨气和水。
(1)CH2=CH2中含有不饱和的C=C双键,能够在催化剂存在条件下与水发生加成反应生成乙醇,反应的化学方程式为:CH2═CH2+H2O![]() CH3CH2OH;
CH3CH2OH;
(2)CH3CH2Br在NaOH的乙醇溶液中加热发生消去反应,生成乙烯,反应的化学方程式为:CH3CH2Br+NaOH![]() CH2===CH2↑+NaBr+H2O;
CH2===CH2↑+NaBr+H2O;
(3)苯与液溴在一定条件下发生取代反应生成溴苯,反应的化学方程式为: ;
;
(4)碳酸的酸性强于苯酚,苯酚钠与少量二氧化碳的反应生成碳酸氢钠和苯酚,反应的化学方程式为:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3;
(5)乙醛与银氨溶液反应制银镜,还生成乙酸铵、氨气和水,反应的化学方程式为:CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H2O。
CH3COONH4+2Ag↓+3NH3+H2O。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】用如图所示装置进行实验,下列对实验现象的解释不合理的是

选项 | ①试剂 | ①中现象 | 解释 |
A | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
B | Na2SiO3溶液 | 产生胶状沉淀 | 酸性: H2SO3 >H2SiO3 |
C | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
D | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成 白色BaSO3沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥E、C同主族,且E比C多两个电子层,E单质可与冷水反应生成氢气。
试回答:
(1)写出元素C、E的名称:C______;E______。
(2)画出A的原子结构示意图______,B的离子结构示意图______,D的单质分子的电子式______。
(3)写出B2A3分别与盐酸和氢氧化钠溶液反应的离子方程式:
____________________;___________________。
(4)比较B、C、E三种元素形成的简单离子半径的大小和氧化性的强弱(用离子符号表示):离子半径:_____________;氧化性:____________。
(5)写出E与冷水反应的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是 ( )
A.将 CO2 通入 CaCl2 溶液:CO2+H2O+Ca2+=CaCO3↓+2H+
B.往氢氧化钠溶液中通入过量 SO2:OH- + SO2 =![]()
C.向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+=Fe2++2H2O
D.向 Ba(OH)2 溶液中滴加NaHSO4 溶液至中性:Ba2++OH-+H++![]() ═BaSO4↓+H2O
═BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO、CO、![]() 是大气污染物但又有着重要用途。
是大气污染物但又有着重要用途。
已知:![]()
![]()
![]()
![]()
![]()
![]()
(1)某反应的平衡常数表达式为 ,此反应的热化学方程式为:______。
,此反应的热化学方程式为:______。
(2)向绝热恒容密闭容器中充入等量的NO和CO进行反应,能判断反应已达到化学平衡状态的是______(填序号)。
a.容器中的压强保持不变 b.![]()
c.气体的平均相对分子质量保持34.2不变 d.该反应平衡常数保持不变
e.NO和CO的体积比保持不变
Ⅱ.(3)甲烷转化为![]() 和CO的反应为:
和CO的反应为:![]()
![]()

①一定条件下,![]() 的平衡转化率与温度、压强的关系如图所示。则
的平衡转化率与温度、压强的关系如图所示。则![]() ______
______![]() (填“<”“>”或“=”);
(填“<”“>”或“=”);
A、B、C三点处对应的平衡常数(![]() 、
、![]() 、
、![]() ),由大到小的顺序为______。
),由大到小的顺序为______。
②将![]() 和
和![]() 按等物质的量混合,一定条件下反应达到平衡,
按等物质的量混合,一定条件下反应达到平衡,![]() 转化率为50%。则反应前与平衡后,混合气体的平均相对分子质量之比为______。
转化率为50%。则反应前与平衡后,混合气体的平均相对分子质量之比为______。
Ⅲ.含![]() 的烟气可用
的烟气可用![]() 溶液吸收。
溶液吸收。
(4)已知![]() 时由
时由![]() ,和
,和![]() 形成的混合溶液恰好呈中性,此时溶液中离子浓度大小顺序为______。(已知
形成的混合溶液恰好呈中性,此时溶液中离子浓度大小顺序为______。(已知![]() 时,
时,![]() 的电离平衡常数
的电离平衡常数![]() ,
,![]() )
)
(5)可将吸收液送至电解槽再生后循环使用。再生电解槽如图所示。a电极上含硫微粒放电的反应式为______(任写一个)。离子交换膜______(填标号)为阴离子交换膜。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有水参加的反应中,属于氧化还原反应但水既不是氧化剂也不是还原剂的是( )
A.2Na2O2+2H2O=4NaOH+O2↑ B.Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
C.Na2O+H2O=2NaOH D.2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物A~H的转换关系如下所示:

请回答下列问题:
(1)链烃A有支链且只有一个官能团,其相对分子质量在65~75之间,1 mol A完全燃烧消耗7 mol氧气,则A的结构简式是____________________________。
(2)在特定催化剂作用下,A与等物质的量的H2反应生成E。E______(填“存在”或“不存在”)顺反异构,由E转化为F的化学方程式为______________________________。
(3)G与金属钠反应能放出气体,由F转化为G的反应条件是__________________;由G生成H的化学方程式是__________________。
(4)B是A的一种同分异构体,它的一氯代物只有一种(不考虑立体异构),则B的结构简式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1980年Smith Kline & French(英国)开发了一种叫盐酸卡布特罗的有机物,它是一种用于治疗支气管的药物,其合成路线如下:

已知:① ![]() ②
② ![]()
(1)下列说法不正确的是_____________。
A. 化合物A能使酸性高锰酸钾溶液褪色 B. 试剂X能够和盐酸反应
C. 1mol化合物G最多能和4mol氢氧化钠溶液反应 D. 反应⑤的反应类型为加成反应
(2)化合物G的结构简式________。
(3)写出④的化学方程式________。
(4)已知:①苯环上有甲基或乙基时,新取代基主要在邻位或对位;
②苯环上有羧基或酯基时,新取代基主要在间位。
结合上述合成路线,请设计以乙苯、ClCH2OH、(CH3)2NH为原料合成 ![]() 的合成路线(用流程图表示,无机试剂任选),示例如下:
的合成路线(用流程图表示,无机试剂任选),示例如下:
![]() ________
________
(5)写出同时满足下列条件的X的所有同分异构体的结构简式________。
①有苯环;②核磁共振氢谱有4个峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的,如下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化。则下列说法正确的是

A. 通常情况下,NO比N2稳定
B. 通常情况下,N2(g)和O2(g)混合能直接生成NO
C. 1molN2(g)和1molO2(g)具有的总能量小于2mol NO(g)具有的总能量
D. 1molN2(g)和1molO2(g)反应放出的能量为180kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com