
【题目】已知乙烯能发生以下转化:

(1)乙烯的结构式为: 。
(2)B中官能团的电子式: ;D中官能团的名称: 。
(3)写出反应的化学方程式及反应类型:
② ;反应类型: ;
③ ;反应类型: ;
④ ;反应类型: 。
【答案】(1)![]() (2)
(2)![]() 羧基
羧基
(3)②2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化反应
2CH3CHO+2H2O 氧化反应
③ ![]() ; 加聚反应
; 加聚反应
④![]() 酯化反应(取代反应)
酯化反应(取代反应)
【解析】
试题分析:(1)乙烯分子中C原子之间形成2对共用电子对,每个C原子在与2个H原子形成2对共用电子对,乙烯的结构式为![]() ;(2)乙烯与水发生加成反应产生的B是乙醇,B中官能团是羟基,电子式是:
;(2)乙烯与水发生加成反应产生的B是乙醇,B中官能团是羟基,电子式是:![]() ;乙醇与乙酸在浓硫酸存在时,在加热条件下发生酯化反应产生乙酸乙酯,所以D是乙酸,D中官能团的名称羧基;(3)乙醇在Cu作催化剂时,在加热条件下发生氧化反应产生C是乙醛,反应的化学方程式是:2CH3CH2OH+O2
;乙醇与乙酸在浓硫酸存在时,在加热条件下发生酯化反应产生乙酸乙酯,所以D是乙酸,D中官能团的名称羧基;(3)乙醇在Cu作催化剂时,在加热条件下发生氧化反应产生C是乙醛,反应的化学方程式是:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;③在催化剂存在时,在加热条件下发生加聚反应,产生聚乙烯,反应的化学方程式是:
2CH3CHO+2H2O;③在催化剂存在时,在加热条件下发生加聚反应,产生聚乙烯,反应的化学方程式是:![]() ;④乙醇与乙酸在浓硫酸存在时,在加热条件下发生酯化反应(也是取代反应),产生乙酸乙酯和水,反应的化学方程式是:
;④乙醇与乙酸在浓硫酸存在时,在加热条件下发生酯化反应(也是取代反应),产生乙酸乙酯和水,反应的化学方程式是:![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】离子化合物①NaCl、②CaO、③NaF、④MgO中,晶格能从小到大顺序正确的是( )
A.①②③④ B.①③②④ C.③①④② D.④②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在酸性溶液中能大量共存的是
A、Na+、Fe2+、NO3-、SCN— B、Ca2+、K+、Cl—、NO3—
C、Al3+、K+、OH—、NO3— D、Na+、Ca2+、SiO32—、Cl—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贵州凤岗的“富锌富硒”茶已享誉全国,因富含硒元素,有延年益寿、抗衰老等作用。但研究表明单质硒可能成为环境污染物,通过与浓盐酸、浓H2SO4反应可回收Se。在回收过程中涉及到如下两个化学反应:①SeO2+4KI+4HCl=Se+2I2+4KCl+2H2O;②Se+2H2SO4(浓)=2SO2![]() + SeO2+2H2O。下列叙述正确的是( )
+ SeO2+2H2O。下列叙述正确的是( )
A. 反应①中Se是氧化产物,I2是还原产物
B. 反应②中浓H2SO4是氧化剂,SeO2是还原产物
C. 反应①中每有1.0mol I2生成,转移电子数目为4 NA
D. SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)> SeO2> I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的浓硫酸跟过量的锌充分反应,产生的气体可能有
① SO2 ② SO3 ③ H2S ④ H2
A.①②③ B.①③④ C.①②④ D.只有①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水的综合利用包括很多方面,下图是从海水中通过一系列工艺流程提取产品的流程图。
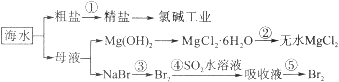
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-等离子。
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。回答下列问题:
(1)海水pH约为8的原因主要是天然海水含上述离子中的_________。
(2)除去粗盐溶液中的杂质(Mg2+、SO42-、Ca2+),加入药品的顺序可以为__________(填序号)
①NaOH溶液 ②BaCl2溶液 ③过滤后加盐酸 ④Na2CO3溶液
(3)过程②中由MgCl2·6H2O制得无水MgCl2,应如何操作____________________。
(4)从能量角度来看,氯碱工业中的电解饱和食盐水是一个将__________转化为_________的过程。采用石墨阳极,不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为_____________
(5)从第③步到第④步的目的是____________________。采用“空气吹出法”从浓海水中吹出Br2,并用SO2吸收。主要反应的化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去)。下列推断不正确的是( )
![]()
A.若D是一种强碱,则A、B、C均可与X反应生成D
B.若D为NaCl,且A可与C反应生成B,则E可能是CO2
C.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的化工原料,可进行如下转化,其中C是食醋的主要成分。(部分反应物、生成物和反应条件已略去)
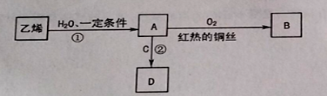
请回答下列问题。
(1)反应①的化学方程式是____________________________。
(2)B的结构简式是______________ ,C中官能团的名称是______________。
(3)反应②的化学方程式是_____________,反应类型是______________,反应后可用______________除去D中混有的C。
(4)鉴别乙烯和甲烷的方法是______________,若观察到______________,则证明气体是乙烯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰的单质及其化合物在生产、生活中有广泛应用。
(1)碱性锌锰电池广泛应用于日常生活。电池的总反应式为:Zn(s)+2MnO2(s)+2H2O(l)===Zn(OH)2(s)+2MnOOH(s)。该电池的正极反应式为 。
(2)某学习小组拟以废旧干电池为原料制取锰,简易流程如下:
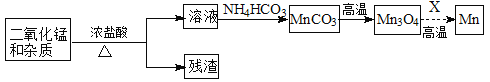
①加入浓盐酸溶解废旧电池内黑色物质过程中保持通风,其原因是 。
②从产品纯度、环保等角度考虑,X宜选择 (填代号)。
A.焦炭 B.铝 C.氢气 D.一氧化碳
③写出碳酸锰在空气中灼烧生成四氧化三锰的化学方程式 。
(3)电解硫酸锰溶液法制锰又叫湿法冶锰。以菱锰矿(主要成份是MnCO3,主要杂质是Fe2+、Co2+、Ni2+)为原料制备锰的工艺流程如下:
![]()
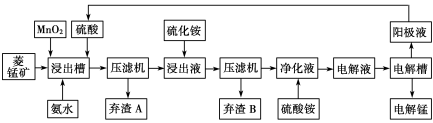
已知:NiS 、CoS均难溶于水。部分氢氧化物的pH如下表:(若某离子浓度小于等于105mol·L1,则认为完全沉淀)
物质 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 | Fe(OH)3 |
开始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 | 2.7 |
完全沉淀pH | 9.7 | 8.4 | 8.5 | 9.8 | 3.8 |
①浸出槽内MnO2的作用是(用离子方程式表示) 。
②加入氨水调节浸出槽中溶液的pH范围为 。
③电解槽阴极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com