
【题目】锰的单质及其化合物在生产、生活中有广泛应用。
(1)碱性锌锰电池广泛应用于日常生活。电池的总反应式为:Zn(s)+2MnO2(s)+2H2O(l)===Zn(OH)2(s)+2MnOOH(s)。该电池的正极反应式为 。
(2)某学习小组拟以废旧干电池为原料制取锰,简易流程如下:
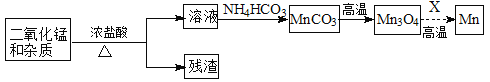
①加入浓盐酸溶解废旧电池内黑色物质过程中保持通风,其原因是 。
②从产品纯度、环保等角度考虑,X宜选择 (填代号)。
A.焦炭 B.铝 C.氢气 D.一氧化碳
③写出碳酸锰在空气中灼烧生成四氧化三锰的化学方程式 。
(3)电解硫酸锰溶液法制锰又叫湿法冶锰。以菱锰矿(主要成份是MnCO3,主要杂质是Fe2+、Co2+、Ni2+)为原料制备锰的工艺流程如下:
![]()
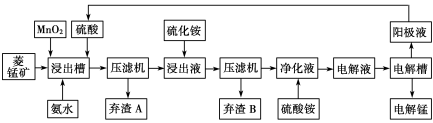
已知:NiS 、CoS均难溶于水。部分氢氧化物的pH如下表:(若某离子浓度小于等于105mol·L1,则认为完全沉淀)
物质 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 | Fe(OH)3 |
开始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 | 2.7 |
完全沉淀pH | 9.7 | 8.4 | 8.5 | 9.8 | 3.8 |
①浸出槽内MnO2的作用是(用离子方程式表示) 。
②加入氨水调节浸出槽中溶液的pH范围为 。
③电解槽阴极的电极反应式为 。
【答案】(1)MnO2+H2O+e=MnOOH+OH;(2)①二氧化锰与浓盐酸反应会产生有毒的氯气;② C; ③ 6MnCO3+O2![]() 2Mn3O4+6CO2;(3)①MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;②3.8≤pH<8.3;③Mn2++2e=Mn。
2Mn3O4+6CO2;(3)①MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;②3.8≤pH<8.3;③Mn2++2e=Mn。
【解析】
试题分析:(1)正极上得到电子,化合价降低,发生还原反应,Mn的化合价降低,MnO2在正极上得电子,根据总电极反应式为:MnO2+H2O+e-=MnOOH+OH-;(2)①废电池中含有MnO2,MnO2和浓盐酸反应产生Cl2,MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,氯气有毒,因此注意通风;②A、用焦炭,得到Mn含有焦炭,且容易产生温室气体,故错误;B、Mn中可能含有未反应铝,产品不纯,故错误;C、用氢气得到的是水,对环境无污染,故正确;D、CO有毒,未反应的CO污染空气,故错误;③MnCO3中Mn为+2价,Mn3O4中Mn为+8/3价,化合价升高,氧气参与反应,反应方程式为6MnCO3+O2
MnCl2+Cl2↑+2H2O,氯气有毒,因此注意通风;②A、用焦炭,得到Mn含有焦炭,且容易产生温室气体,故错误;B、Mn中可能含有未反应铝,产品不纯,故错误;C、用氢气得到的是水,对环境无污染,故正确;D、CO有毒,未反应的CO污染空气,故错误;③MnCO3中Mn为+2价,Mn3O4中Mn为+8/3价,化合价升高,氧气参与反应,反应方程式为6MnCO3+O2![]() 2Mn3O4+6CO2;(3)①根据流程图以及信息,弃渣A为Fe(OH)3,MnO2的作用是把Fe2+氧化成Fe3+,然后调节pH除去Fe3+,因为Fe(OH)3全部变为沉淀的时,Mn元素没有沉淀,如果是Fe(H)2完全沉淀,则Mn一部分全化成沉淀,MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;②氨水调节pH,使Fe3+变成Fe(OH)3,减少Mn的损耗,因此pH的范围是3.8≤pH<8.3;③阴极是得电子的,Mn2++2e-=Mn。
2Mn3O4+6CO2;(3)①根据流程图以及信息,弃渣A为Fe(OH)3,MnO2的作用是把Fe2+氧化成Fe3+,然后调节pH除去Fe3+,因为Fe(OH)3全部变为沉淀的时,Mn元素没有沉淀,如果是Fe(H)2完全沉淀,则Mn一部分全化成沉淀,MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;②氨水调节pH,使Fe3+变成Fe(OH)3,减少Mn的损耗,因此pH的范围是3.8≤pH<8.3;③阴极是得电子的,Mn2++2e-=Mn。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知乙烯能发生以下转化:

(1)乙烯的结构式为: 。
(2)B中官能团的电子式: ;D中官能团的名称: 。
(3)写出反应的化学方程式及反应类型:
② ;反应类型: ;
③ ;反应类型: ;
④ ;反应类型: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而会发生引发中毒的事故。
(1)两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式: 。
(3)常温下,0.1mol/L的NaClO溶液的PH=9.7,原因 。常温下HClO的电离平衡常数为 。洁厕液与84消毒液混合后会生成有毒的氯气。写出该反应的离子方程式 。
(4)高铁酸钾是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:
①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为 。
②Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH=K2FeO4+2NaOH;K2FeO4在水溶液中易水解:4FeO42-+10H2O![]() 4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号)
4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号)
a.水 b.NH4Cl、异丙醇 c.Fe(NO3)3、异丙醇 d.CH3COONa、异丙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3 → Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平,不考虑 2NO2 ![]() N2O4)。
N2O4)。
(1)硝酸在该反应中体现的性质有_________________ _。
(2)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出并配平该反应的离子方程式
_________ 。
(3)0.004molCu被硝酸完全溶解后,Cu失去的电子数是____________,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是____________,在标准状况下若将收集NO和NO2的集气瓶倒立于水中,通入一定量的氧气充分反应后发现无气体剩余,则通入O2的体积为________ mL;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
化合物F是一种抗心肌缺血药物的中间体,可以通过以下方法合成:
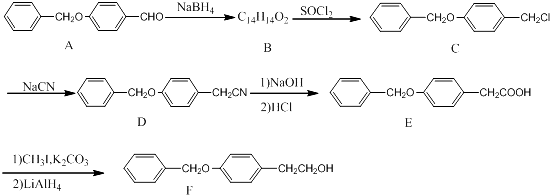
(1)化合物C中的官能团为 (填官能团的名称)。
(2)化合物B的结构简式为 ; 由A→B的反应类型是: 。
(3)同时满足下列条件的A的同分异构体有 种。试写出一种分子中只含有6种等效氢的结构简式: 。
①分子含有2个独立苯环,无其他环状结构 ②能发生银镜反应和水解反应
③不能和FeCl3发生显色反应,但水解产物分子中含有甲基
(4)已知:RCH2CN![]() RCH2CH2NH2,请写出以
RCH2CH2NH2,请写出以![]() 为原料制备化合物X(
为原料制备化合物X(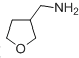 )(结构简式见图)的合成路线流程图(无机试剂可任选): 。
)(结构简式见图)的合成路线流程图(无机试剂可任选): 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物通过化合反应生成,向其水溶液中加入足量Na2O2,最终有白色沉淀产生。下列化合物中符合上述条件的是
A.Ca(HCO3)2 B.Na2S C.FeI2 D.AlCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容器中发生一个化学反应,反应过程中存在H2O、ClO﹣、CN﹣、HCO3﹣、N2、Cl﹣六种物质,在反应过程中测得ClO﹣和N2的物质的量随时间变化的曲线如图所示.下列有关判断中正确的是( )
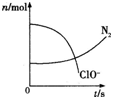
A.还原剂是CN﹣,氧化产物只有N2
B.氧化剂是ClO﹣,还原产物是HCO3﹣
C.配平后氧化剂与还原剂的计量系数之比为5:2
D.标准状况下若生成2.24LN2,则转移电子0.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应。已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g。下列说法正确的是( )

A.反应③最多能产生0.05molO2
B.反应①的离子方程式为Na+2H2O=Na++2OH-+H2↑
C.①、②、③都属于氧化还原反应
D.①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com