
【题目】[化学—选修3:物质结构与性质]
元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
Ⅰ.第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。
镓(31Ga)的基态电子排布式是 ;
31Ga的第一电离能却明显低于30Zn,原因是 ;
Ⅱ.第四周期过渡元素的明显特征是形成多种多样的配合物。
(1)CO和NH3可以和很多过渡金属形成配合物。CO与N2互为等电子体,CO分子中C原子上有一孤电子对,C、O原子都符合8电子稳定结构,则CO的结构式可表示为 。NH3 分子中N原子的杂化方式为 杂化,NH3分子的空间立体构型是 。
(2)向盛有硫酸铜水溶液的试管中加氨水,首先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加乙醇,析出深蓝色晶体。蓝色沉淀先溶解,后析出的原因是: (用相关的离子方程式和简单的文字说明加以解释)
(3)图甲所示的二维平面晶体示意图中表示化学式为AX3的是________。
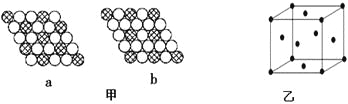
(4)图乙为一个金属铜的晶胞,此晶胞立方体的边长为acm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则阿伏加德罗常数可表示为 mol-1(用含a、ρ的代数式表示)。
【答案】Ⅰ.31Ga的电子排布式是:1s22s22p63s23p63d104s24p1(2分)
30Zn的4s能级处于全充满状态,较稳定(2分)
Ⅱ.(1)![]() (只写三键没标明配位键给2分)(2分) sp3(1分)三角锥型(1分)
(只写三键没标明配位键给2分)(2分) sp3(1分)三角锥型(1分)
(2)蓝色沉淀与氨水可发生如下反应:
Cu(OH)2+4NH3H2O=[Cu(NH3)4]2++4H2O+2OH-,生成的[Cu(NH3)4]SO4在极性较小的乙醇中溶解度较小而析出 (3分)
(3)b (2分)
(4)![]() mol-1(2分)
mol-1(2分)
【解析】试题分析:I、根据核外电子的排布规律,31号元素的核外电子排布式为1s22s22p63s23p63d104s24p1;30Zn的最外层电子排布是4s2,属于全充满状态,比较稳定,所以30Zn的第一电离能较大;
II、(1)CO与N2互为等电子体,氮气 的结构中有三键,所以CO分子中也有三键结构,CO分子中C原子上有一孤电子对,说明C原子提供2个电子,O原子提供4个电子,其中有1对电子与C原子的2p轨道形成配位键,所以CO的结构式是![]() ;氨气分子中的N原子的价层电子对数是4,有1对孤对电子,所以氨气的空间构型是三角锥型,为sp3杂化;
;氨气分子中的N原子的价层电子对数是4,有1对孤对电子,所以氨气的空间构型是三角锥型,为sp3杂化;
(2)蓝色沉淀是氢氧化铜沉淀,氢氧化铜与氨水反应生成四氨合铜离子,Cu(OH)2+4NH3H2O=[Cu(NH3)4]2++4H2O+2OH-,生成的深蓝色[Cu(NH3)4]SO4在极性较小的乙醇中溶解度较小而析出;
(3)a图中6个X原子构成一个正六边形,每个X原子被3个正六边形共有,正六边形的中心有1个A原子,所以每个正六边形中的X的原子的个数实际是6×1/3=2,则a图表示的化学式是AX2;b图中6个X原子构成一个正六边形,每个X原子被2个正六边形共有,正六边形的中心有1个A原子,所以每个正六边形中的X的原子的个数实际是6×1/2=3,则b图表示的化学式是AX3,答案选b;
(4)铜的晶胞中Cu原子分别位于面心和顶点,所以晶胞中Cu的个数实际是6×1/2+8×1/8=4,所以晶胞密度ρg/cm3=64g/mol/NA×4/a3cm3,则NA=![]() mol-1
mol-1


科目:高中化学 来源: 题型:
【题目】高中化学教材介绍了部分常见的金属与非金属元素及其化合物的相关知识,试回答下列问题
(1)实验室制取纯净氯气的实验中,除了二氧化锰、浓盐酸和浓硫酸,还需要___________、________(填写试剂或溶液名称)
(2)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式:____________________
(3)图中三根曲线表示锌、铝、铁分别与稀硫酸反应时金属质量与H2体积的关系,其中能表示铝的是 (填“a”“b”或“c”)。
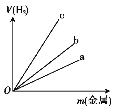
(4)氧元素的氢化物除H2O外,还有H2O2;碳元素的氢化物除CH4外,还有C2H6等;氮元素的氢化物除NH3外,还有含2个氮原子的分子的化学式为 ,该氢化物与足量盐酸反应的化学反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某烃A的质谱和核磁共振氢谱如下两个图:

(1)A的结构简式___________________________。
(2)A的二氯代物种类数_____________________。
(3)请写出A的一氯代物消去的方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H+(aq)+OH-(aq)=H2O(l) △H =a,则a可能等于
A. -57.3mol/L B. -57.3kJ/mol C. +57.3J/mol D. -57.3J/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是 ( )
待测气体 | 部分电极反应产物 |
NO2 | NO |
Cl2 | HCl |
CO | CO2 |
H2S | H2SO4 |

A. 上述气体检测时,敏感电极均作电池正极
B. 检测H2S气体时,对电极充入空气,该电极上的电极反应式为O2 + 2H2O+ 4e- = 4OH-
C. 检测Cl2气体时,敏感电极的电极反应为:Cl2 + 2e-= 2Cl-
D. 检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(s) +nB(g) ![]() pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图。根据图中曲线分析,判断下列叙述中正确的是
pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图。根据图中曲线分析,判断下列叙述中正确的是
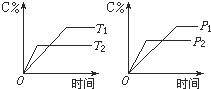
A.到达平衡后,若使用催化剂,C的质量分数增大
B.平衡后,若升高温度,平衡则向逆反应方向移动
C.平衡后,增大A的量,有利于平衡向正反应方向移动
D.方程式中一定m+n<p+q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2(g)![]() 2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是( )
2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦ C. ①③④⑤ D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com