
【题目】锌-空气电池(原理如图)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时下列说法正确的是

A. 氧气在石墨电极上发生氧化反应
B. 该电池的负极反应为Zn+H2O-2e- = ZnO+2H+
C. 该电池充电时应将Zn电极与电源负极相连
D. 该电池放电时OH-向石墨电极移动
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分:
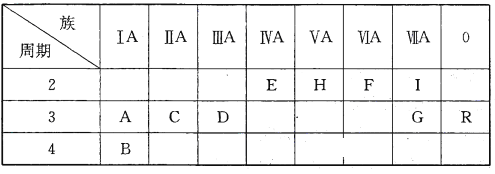
根据要求回答下列问题:
(1)十种元素中化学性质最不活泼的元素是__________________(填元素符号,下同),形成化合物种类最多的元素是_____________________。
(2)A、C、D三种元素的最高价氧化物对应的水化物,其中碱性最强的是______________(填化学式,下同),E、H、G三种元素的最高价氧化物对应的水化物中酸性最强的是______________。
(3)I元素跟A元素形成化合物的电子式是______________。高温灼烧该化合物时,火焰呈______________色。
(4)分别写出B、G两种单质和水反应的离子方程式_____________、________________。
(5)元素A和F能形成两种化合物,写出其中较稳定的化合物与CO2反应生成氧气的化学方程式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究![]() 和
和![]() 的反应规律。实验操作及现象如下:
的反应规律。实验操作及现象如下:
实验及试剂 | 编号 | 无色 | 试管中溶液颜色 | 淀粉KI试剂颜色 |
| 1 | 0.5mL | 浅黄色 | 无色 |
2 | 0.20mL | 深黄色 | 无色 | |
3 | 0.25mL | 浅黄色 | 蓝色 | |
4 | 0.30mL | 无色 | 蓝色 |
(1)取实验2后的溶液,进行如下实验:

经康康同学检验,上述白色沉淀是![]() 。写出加入0.20mL
。写出加入0.20mL ![]() 后,溶液中
后,溶液中![]() 和
和![]() 发生反应的离子方程式:____________。
发生反应的离子方程式:____________。
(2)查阅资料:一定条件下,![]() 和
和![]() 都可以被氧化成
都可以被氧化成![]() 。
。
作出假设:![]() 溶液用量增加导致溶液褪色的原因是过量的
溶液用量增加导致溶液褪色的原因是过量的![]() 溶液与(1)中的反应产物继续反应,同时生成
溶液与(1)中的反应产物继续反应,同时生成![]() 。进行实验:
。进行实验:
①取少量实验4中的无色溶液进行以下实验,进一步佐证其中含有![]() 。
。

其中试剂X可以是_________(填字母序号)。
a 碘水 b ![]() 溶液 c
溶液 c ![]() 溶液 d
溶液 d ![]() 溶液
溶液
②李政同学提出,仅通过润湿淀粉![]() 试纸变蓝的现象不能说明生成
试纸变蓝的现象不能说明生成![]() ,理由是_______,便补充了如下实验:将实验4中的湿润淀粉
,理由是_______,便补充了如下实验:将实验4中的湿润淀粉![]() 试纸替换为________,在滴加
试纸替换为________,在滴加![]() 溶液后,发现________,进一步佐证实验4中生成了
溶液后,发现________,进一步佐证实验4中生成了![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物的结构简式为 ,下列有关该化合物的叙述不正确的是
,下列有关该化合物的叙述不正确的是
A.该有机物的分子式为C11H12O2
B.1mol该物质最多能与4molH2发生反应
C.该有机物分子中所有原子一定在同一个平面上
D.该有机物一定条件下,可以发生取代、加成、氧化、酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中说法不正确的是( )
A.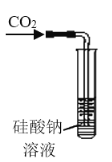 可用来证明碳的非金属性比硅强
可用来证明碳的非金属性比硅强
B.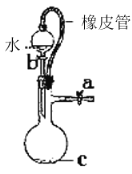 橡皮管的作用是能使水顺利流下
橡皮管的作用是能使水顺利流下
C. 用图示的方法不能检查此装置的气密性
用图示的方法不能检查此装置的气密性
D. 先从①口进气集满CO2,再从②口进气,可收集NO
先从①口进气集满CO2,再从②口进气,可收集NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将15.2 g 铜和镁组成的混合物加入250 mL4.0 mol L-1的稀硝酸中,固体完全溶解,生成的气体只有NO。向所得溶液中加入1.0 L NaOH溶液,此时金属离子恰好沉淀完全,沉淀质量为25.4 g,下列说法不正确的是
A. 原固体混合物中,Cu和Mg的物质的量之比为2:1
B. 氢氧化钠溶液的浓度为0.8 mol·L-1
C. 固体溶解后的溶液中硝酸的物质的量为0.1mol
D. 生成的NO气体在标况下的体积为4.48L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质) 制取七水合硫酸亚铁(FeSO4·7H2O) ,流程如下:
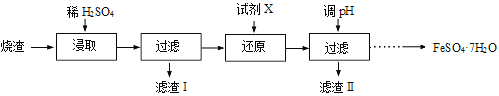
(1)浸取时,溶液中的Fe2+易被空气中的O2氧化,其离子方程式为 。能提高烧渣浸取速率的措施有 (填字母)。
A.将烧渣粉碎 B.降低硫酸的浓度 C.适当升高温度
(2)还原时,试剂X的用量与溶液pH的变化如图所示,则试剂X可能是 (填字母)。
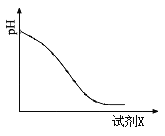
A.Fe粉 B.SO2 C.NaI
还原结束时,溶液中的主要阴离子有 。
(3)滤渣Ⅱ主要成分的化学式为 ;由分离出滤渣Ⅱ后的溶液得到产品,进行的操作是 、 过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列表述中正确的是( )

A.反应的化学方程式为2X=3Y+Z
B.t时,正、逆反应都不再继续进行,反应达到化学平衡
C.若t=4,则0~t X的化学反应速率为0.1mol/(L·min)
D.温度、体积不变,t时刻充入1mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式:
(1)28 g CO还原Fe2O3生成单质铁,放出8.3 kJ热量____________________。
(2)1 mol氨气和1 mol氯化氢气体化合生成氯化铵固体,放出176 kJ热量_________。
(3)N2和O2化合生成184 g NO2气体,吸收135.4 kJ热量___________________________。
(4)1 g H2燃烧生成液态水,放出142.9 kJ热量________________________。
(5)5.2 g气态乙炔(C2H2)完全燃烧生成液态水和气态CO2,放出260 kJ热量________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com