
����Ŀ����Ȳ���ڴ��������¿ɷ���ż����Ӧ����Ϊ Glaser ��Ӧ��2R��C��C��H![]() R��C��C��C��C��R+H2 �÷�Ӧ���о����ͷ�����ϡ������ӻ�ѧ�ȷ��������Ҫ��ֵ������������ Glaser ��Ӧ�Ʊ������� E ��һ�ֺϳ�· �ߣ�
R��C��C��C��C��R+H2 �÷�Ӧ���о����ͷ�����ϡ������ӻ�ѧ�ȷ��������Ҫ��ֵ������������ Glaser ��Ӧ�Ʊ������� E ��һ�ֺϳ�· �ߣ�
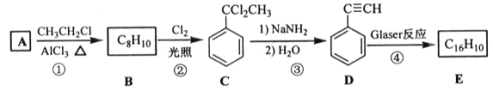
�ش��������⣺
��1��B ��һ��ȡ���������Ϊ_______��
��2���ٺ͢۵ķ�Ӧ���ͷֱ�Ϊ_______��_______��
��3��1 mol E �ڴ����������������� H2 ��Ӧ�Ļ�ѧ����ʽΪ_______��
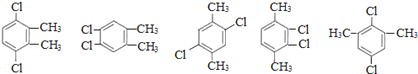
��4�����㻯���� F �� C ��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ 3:1��д������ 2 �ֵĽṹ ��ʽ_____��
��5���ÿα���ѧ֪ʶд����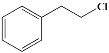 Ϊԭ�ϣ��������Լ���ѡ���Ʊ������� D �ĺϳ�·��_____��
Ϊԭ�ϣ��������Լ���ѡ���Ʊ������� D �ĺϳ�·��_____��
���ϳ�·�߳��õı�ʾ��ʽΪ��![]() ��
��
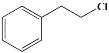
���𰸡�5 ȡ�� ��ȥ ![]() +10H2
+10H2![]()
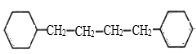
 (�����)
(�����) 
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
��������
��B�ķ���ʽ��C�Ľṹ��ʽ��֪B�Ľṹ��ʽΪ![]() ����A�������鷢��ȡ����Ӧ����B����AΪ
����A�������鷢��ȡ����Ӧ����B����AΪ![]() ���Ա�C��D�Ľṹ��ʽ��֪C��ȥ2����HCl��ͬʱ�γ�DΪ����Ȳ���÷�Ӧ������ȥ��Ӧ��D������Ϣ�е�ż����Ӧ����EΪ
���Ա�C��D�Ľṹ��ʽ��֪C��ȥ2����HCl��ͬʱ�γ�DΪ����Ȳ���÷�Ӧ������ȥ��Ӧ��D������Ϣ�е�ż����Ӧ����EΪ![]() ���ݴ˷������
���ݴ˷������
��1��B�Ľṹ��ʽΪ![]() ���ṹ�к���5�ֲ�ͬ����ԭ�ӣ���һ��ȡ���������Ϊ5�֣�
���ṹ�к���5�ֲ�ͬ����ԭ�ӣ���һ��ȡ���������Ϊ5�֣�
��2�����ݷ�������ΪA�������鷢��ȡ����Ӧ����B����Ӧ����Ϊȡ����Ӧ����Ӧ�۶Ա�C��D�Ľṹ��ʽ��֪C��ȥ2����HCl��ͬʱ�γ�DΪ����Ȳ���÷�Ӧ������ȥ��Ӧ��
��3��E�Ľṹ��ʽΪ![]() ��̼̼�����ͱ�����һ�������¶��������������ӳɷ�Ӧ��1 mol E �ڴ�������������10molH2 �����ӳɣ���Ӧ�Ļ�ѧ����ʽΪ
��̼̼�����ͱ�����һ�������¶��������������ӳɷ�Ӧ��1 mol E �ڴ�������������10molH2 �����ӳɣ���Ӧ�Ļ�ѧ����ʽΪ![]() +10H2
+10H2![]()
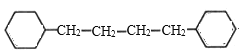 ��
��
��4�����㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3��1�����ܵĽṹ��ʽΪ�� ����5�֣���д���֡�
����5�֣���д���֡�
��5���� Ϊԭ�ϣ��������Լ���ѡ���Ʊ������� D ������
Ϊԭ�ϣ��������Լ���ѡ���Ʊ������� D ������ ������������Һ���������·���ˮ������
������������Һ���������·���ˮ������![]() ��
��![]() ��Ũ���ᡢ���������·�����ȥ��Ӧ����
��Ũ���ᡢ���������·�����ȥ��Ӧ����![]() ��Ȼ�����巢���ӳɷ�Ӧ����
��Ȼ�����巢���ӳɷ�Ӧ����![]() ��������������ƴ���Һ�����������·�����ȥ��Ӧ����
��������������ƴ���Һ�����������·�����ȥ��Ӧ����![]() ���ϳ�·������ͼΪ��
���ϳ�·������ͼΪ��
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���屽�ķе�Ϊ156�棬���ķе�Ϊ80�档ʵ�����ñ���Һ����ȡ�屽����֤��Ӧ���͵�ʵ��װ����ͼ��
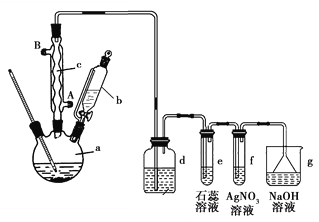
������Ҫ��ش����⣺
(1)�����ܵĽ�ˮ��Ϊ______(����A������B��)�������ܵ����ã�__________��
(2)d��ʢ�ŵ��Լ���_____________
(3)��ͬѧ��Ϊ������ķ�ӦΪ�ӳɷ�Ӧ������ȡ����Ӧ������ݸ�ʵ��װ���ص��ʵ�������жϷ�Ӧ�����͡�
�ٷ�Ӧ���ͣ�_______________(�����ӳɷ�Ӧ������ȡ����Ӧ��)��
�������ó���һ���۵�ʵ������____________________________________��
(4)�����ᴿ��
�ٷ�Ӧ��aƿ�е��屽������������Ժ�ɫ���ᴿ�屽�Ĺ����У���ȥ�屽�е���ɼ���___________��Һ������ͨ��____________(����뷽��)�����ᴿ��
�ڱ����廹���ܷ�������Ӧ���ɶԶ��屽(�е�220��)���ڶ��屽(�е�224�棬�������پ�____________(����뷽��)���ɵõ��ϴ������屽���ù�����Ϊ�����Ⱦ��Ⱥ����ڿ����¶ȣ��ɲ���_____________(����ˮԡ��������ԡ��)���ȡ�
(5)������𣺳�ַ�Ӧ��������ƿ�еĴֲ�Ʒ��ˮϴ����Һ��õ�ˮϴҺ��Ϊ��֤ˮϴҺ���Ƿ����Fe3+����ѡ�õ��Լ���_________(����ĸ)
A.NaOH��Һ B.AgNO3��Һ C.KSCN��Һ D.������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�������о�
![]() ��
��![]() ��һ�������¿��Ժϳɼ״���
��һ�������¿��Ժϳɼ״���![]() ���������Ϊ1L�ĺ����ܱ�����
���������Ϊ1L�ĺ����ܱ�����![]() ͼ��
ͼ��![]() ��ͨ��1molCO��
��ͨ��1molCO��![]() ���ⶨ��ͬʱ�䡢��ͬ�¶�
���ⶨ��ͬʱ�䡢��ͬ�¶�![]() ��������CO�����ʵ����������
��������CO�����ʵ����������

0min | 10min | 20min | 30min | 40min | |
| 1mol |
|
|
|
|
| 1mol |
|
| a | a |
��ش�
![]() ______
______![]() ����
����![]() ������
������![]() ������
������![]() ��
��![]() ��������______����֪
��������______����֪![]() ʱ����20minʱ������ѹǿ���ٸı䣬��ʱ
ʱ����20minʱ������ѹǿ���ٸı䣬��ʱ![]() ��ת����Ϊ______�����¶��µĻ�ѧƽ�ⳣ��Ϊ______��
��ת����Ϊ______�����¶��µĻ�ѧƽ�ⳣ��Ϊ______��
![]() ����1molCO��
����1molCO��![]() ͨ��ԭ���Ϊ1L�ĺ�ѹ�ܱ�����
ͨ��ԭ���Ϊ1L�ĺ�ѹ�ܱ�����![]() ͼ3��
ͼ3��![]() �У���
�У���![]() �´ﵽƽ�⣬��ʱ��Ӧ��ƽ�ⳣ��Ϊ______��������������ͨ��
�´ﵽƽ�⣬��ʱ��Ӧ��ƽ�ⳣ��Ϊ______��������������ͨ��![]() �����´ﵽƽ���
�����´ﵽƽ���![]() ����ϵ�еİٷֺ���______
����ϵ�еİٷֺ���______![]() ���������������С������������
���������������������������![]() ��
��
![]() һ��������Ҳ����NaOH��Һ��CO��Ӧ���ɼ����ƣ���һ����Ӧ���ɼ���������CO��Ⱦ�������½�amol��COͨ��
һ��������Ҳ����NaOH��Һ��CO��Ӧ���ɼ����ƣ���һ����Ӧ���ɼ���������CO��Ⱦ�������½�amol��COͨ��![]() NaOH��Һ�У�ǡ����ȫ��Ӧ���ɼ����ƺͺ���������Ļ����Һ
NaOH��Һ�У�ǡ����ȫ��Ӧ���ɼ����ƺͺ���������Ļ����Һ![]() ������Һ�������
������Һ�������![]() �������Һ��
�������Һ��![]() ����û����Һ�м���ĵ���ƽ�ⳣ��
����û����Һ�м���ĵ���ƽ�ⳣ��![]() ______
______![]() �ú�a��b�Ĵ���ʽ��ʾ
�ú�a��b�Ĵ���ʽ��ʾ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ����Ŀǰȼ��ȼ��ʱ�����Ļ�����Ⱦ��ͬʱ������ԴΣ�����й�ר�����������̫������ȡ���ܵĹ��롣����˵����ȷ����
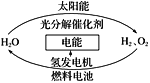
A. H2O�ķֽⷴӦ�Ƿ��ȷ�Ӧ
B. ��ֽ����ֻ�漰̫��������ܵ�ת��
C. 2H2O(l) = 2H2(g) + O2(g) ��H > 0
D. ����������������䣬�������ü�ֵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ���������ǣ� ��
A.0.1mol��L-1NaHCO3��Һ��Na+��Ba2+��NO3-��OH-
B.0.1mol��L-1NaAlO2��Һ��K+��OH-��Cl-��NO3-
C.![]() =1.0��1012����Һ��Fe2+��Mg2+��NO3-��I-
=1.0��1012����Һ��Fe2+��Mg2+��NO3-��I-
D.0.1mol��L-1FeCl3��Һ��K+��Cu2+��SCN-��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����͵ĵ�أ��ܷ�ӦΪ: 3Zn+2FeO42��+8H2O=2Fe(OH)3��+3Zn(OH)2��+4OH�����乤��ԭ����ͼ��ʾ������˵������ȷ����
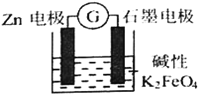
A. Zn���Ǹ���������������Ӧ
B. ���ŷ�Ӧ�Ľ��У���Һ��pH����
C. ������Zn��������ʯī�缫���پ�����Һ�ص�Zn�����γɻ�·
D. ʯī�缫�Ϸ����ķ�ӦΪ��FeO42��+3e��+4H2O=Fe(OH)3��+5OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����![]()
A.����ˮ��Һ�ữ������ˮ�����жϵ����Ƿ�ˮ����ȫ
B.ֲ��ոѡ�ţ�ͳ���ˮ��IJ����Ϊ������
C.�������м��뱥��̼������Һ�����ɵij�����ˮ�����ܽ�
D.����������ǡ���������ά�ؾ���Ϊͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ˮ��Һ�е�����ƽ������������ȷ���ǣ� ��
A.��10mL0.1mol��L��1������뵽10mL0.1mol��L��1̼������Һ�У�c(Na��)��c(Cl��)��c(HCO3-)��c(CO32-)
B.0.02mol��L��1HCN��Һ��0.02mol��L��1NaCN��Һ�������ϣ�c(HCN)��c(CN��)��0.04mol��L��1
C.�����ʵ���Ũ�ȵ�������Һ�У���NH4Al(SO4)2����NH4Cl����CH3COONH4����NH3��H2O��c(NH4+) �ɴ�С��˳���ǣ���=�ڣ��ۣ���
D.��0.01mol��L��1������Һ�м�ˮ��ϡ�ͺ���Һ��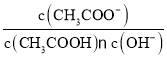 ��ֵ������ϡ��������Һ�¶ȱ仯��
��ֵ������ϡ��������Һ�¶ȱ仯��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com