
【题目】把500mLNH4HCO3和Na2CO3的混合溶液分为五等分,取一份加入含amol氢氧化钠的溶液恰好反应完全,另取一份加入含bmolHCl的盐酸恰好反应至不再产生CO2,则该混合溶液中c(Na+)为( )
A. (![]() )molL-1
)molL-1
B. (2b-a)molL-1
C. (5b-![]() )molL-1
)molL-1
D. (10b-5a)molL-1
【答案】D
【解析】
解:设100ml溶液中含有NH4HCO3 xmol,Na2CO3 ymol,NH4HCO3和Na2CO3的混合溶液加入NaOH,反应为:
NH4HCO3+2NaOH═NH3·H2O+Na2CO3+H2O,
1 2
x amol
解得:x=0.5amol;故:NH4HCO3为0.5amol;
加入含b mol HCl的盐酸的反应为:
NH4HCO3+HCl═NH4Cl+CO2↑+H2O,Na2CO3+2HCl═2NaCl+H2O+CO2↑,
1 1 1 2
0.5amol n(HCl) y b-n(HCl)
解得:n(HCl)=0.5amol,y=0.5(b-0.5amol);
n(Na+)=2n(Na2CO3)=(b-0.5a)mol,
c(Na+)=(b-0.5a)mol/0.1L=(10b-5a)mol·L-1;
故选:D。


科目:高中化学 来源: 题型:
【题目】下表中对应关系正确的是
A | CH3CH3+Cl2 | 均为取代反应 |
B | 由油脂得到甘油 | 均发生了水解反应 |
C | Cl2+2Br=2Cl+Br2 | 均为单质被还原的置换反应 |
D | 2Na2O2+2H2O+4NaOH+O2↑ | 均为水作还原剂的氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学为探究H2O2、H2SO3、Br2的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。

实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为红棕色 |
Ⅱ | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
请回答下列问题:
(1)A中反应的离子方程式是______。
(2)实验操作Ⅱ吹入热空气的目的是_____。
(3)装置C的作用是_____,C中盛放的药品是_____。
(4)实验操作Ⅲ,混合液逐渐变成红棕色,其对应的离子方程式是_____。
(5)由上述实验得出的结论是______。
(6)实验反思:
①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是(写出一条即可)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3 mol A和3 mol B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,C的平均反应速率为0.15 mol/(L·min)。试求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,C的平均反应速率为0.15 mol/(L·min)。试求:
(1)5 min后A的浓度__________________。
(2)B的平均反应速率为___________________。
(3)x的值为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
A. 常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
B. 2.3g钠在空气中燃烧生成多种氧化物是转移电子数为0.1NA
C. 1.8g D2O中含有的质子数为1.0NA
D. 235g核素![]() 发生裂变反应
发生裂变反应![]() +
+ ![]()
![]()
![]() Sr+
Sr+![]() Xe+10
Xe+10![]() n,净产生的中子(
n,净产生的中子(![]() n)数为10NA
n)数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案设计中,无法达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 除去NaCl固体中少量的KNO3杂质 | 将固定溶于水配成溶液,蒸发结晶并趁热过滤 |
B | 检验乙酸乙酯中是否含有乙酸 | 加入含有酚酞的NaOH溶液并振荡,观察下层溶液颜色变化 |
C | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中滴入BaCl2溶液,观察溶液的变化 |
D | 比较Fe3+和I2的氧化性强弱 | 向含有淀粉的KI溶液中滴入FeCl3溶液,观察溶液颜色变化 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)①H3PO2是一元中强酸,写出其电离方程式______________________。
②NaH2PO2为___________(填“正盐”或“酸式盐”),其溶液显___________(填“弱酸性”“中性”或“弱碱性”)。
③H3PO2中,P元素的化合价为___________;
(2)H3PO2可用于化学镀银,反应中Ag+还原为银,H3PO2氧化为H3PO4,该反应中氧化剂与还原剂的物质的量之比为________。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4 反应,写出白磷与Ba(OH)2溶液反应的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,科学家研发出一种新型质子膜电池,下列有关说法正确的是( )

A.电流方向为由电极a流向电极bB.a电极反应式:2H2S-4e- =S2+4H+
C.用此电源电解精炼铜,粗铜接在a电极D.该装置中H+由电极b经质子膜移动到电极a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)命名下列有机物:
CH3CHOHCH3____________
HOCH2CH2CHO____________
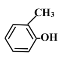 _________________
_________________
(2)燃烧某有机物A 1.50 g,生成1.12 L(标准状况)CO2和0.05 mol H2O,该有机物的蒸气对空气的相对密度是1.04,则该有机物的分子式为_____。
(3)已知端炔烃在催化剂存在下可发生偶联反应:![]() +H2, 称为Glaser反应,回答下列问题:
+H2, 称为Glaser反应,回答下列问题:
已知: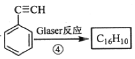 ,该转化关系的产物E(C16H10)的结构简式是_______,用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气____mol。
,该转化关系的产物E(C16H10)的结构简式是_______,用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气____mol。
(4)已知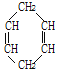 可简写为
可简写为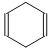 ,现有某化合物W的分子结构可表示为
,现有某化合物W的分子结构可表示为![]()
![]() 的一氯代物有______种
的一氯代物有______种![]()
![]() 下列有关W的说法不正确的是______
下列有关W的说法不正确的是______![]() 填编号
填编号![]() ;
;
a.能发生还原反应
b.能发生氧化反应
c.等质量的W与苯分别完全燃烧所消耗的氧气量,前者大
d.与苯互为同分异构体
![]() 写出W的芳香族同分异构体
写出W的芳香族同分异构体![]() 能发生聚合反应
能发生聚合反应![]() 的结构简式_________;该聚合反应的化学方程式为_________;
的结构简式_________;该聚合反应的化学方程式为_________;
![]() 属于______
属于______![]() 填编号
填编号![]() 。
。
![]() 芳香烃
芳香烃![]() 环烃
环烃![]() 不饱和烃
不饱和烃![]() 炔烃
炔烃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com