
����Ŀ�������ᣨH3PO2����һ�־�ϸ������Ʒ�����н�ǿ��ԭ�ԣ��ش��������⣺
��1����H3PO2��һԪ��ǿ�ᣬд������뷽��ʽ______________________��
��NaH2PO2Ϊ___________������������������ʽ������������Һ��___________��������������������������������������
��H3PO2�У�PԪ�صĻ��ϼ�Ϊ___________��
��2��H3PO2�����ڻ�ѧ��������Ӧ��Ag+��ԭΪ����H3PO2����ΪH3PO4���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ________��
��3��H3PO2�Ĺ�ҵ�Ʒ���:������(P4)��Ba(OH)2��Һ��Ӧ����PH3�����Ba(H2PO2)2����������H2SO4 ��Ӧ��д��������Ba(OH)2��Һ��Ӧ�Ļ�ѧ����ʽ______________________��
���𰸡�H3PO2![]() H++H2PO2- ���� ������ +1 4:1 2P4+3Ba(OH)2+6H2O =2PH3+3Ba(H2PO2)2
H++H2PO2- ���� ������ +1 4:1 2P4+3Ba(OH)2+6H2O =2PH3+3Ba(H2PO2)2
��������
(1)����H3PO2��һԪ��ǿ���֪��H3PO2��������ʣ���Һ�в��ֵ���������ӣ��ݴ�д�����뷽��ʽ���γɵ���Ϊ����ǿ���Σ�ˮ��ʼ��ԣ����ݻ��������ܻ��ϼ�Ϊ0�����PԪ�صĻ��ϼۣ�
(2)���ж�����������ԭ����Ȼ����ݻ��ϼ������غ㣬�����������ͻ�ԭ���ı�����
(3)������ԭ��Ӧ�����ݵ�ʧ�����غ��ԭ���غ���д����ʽ��
(1)��H3PO2��һԪ��ǿ�ᣬ��Һ�в��ֵ���������ӣ���������뷽��ʽΪ��H3PO2![]() H2PO2��+H����
H2PO2��+H����
��H3PO2��һԪ�ᣬֻ�ܵ����1��H����NaH2PO2����ȻH2PO2���к���2��Hԭ�ӣ����Ǿ����ܵ������������NaH2PO2Ϊ���Ρ�H2PO2��Ϊ�������������ӣ��ܹ����ˮ���������H����ʹ����Һ�е�OH����Ũ�ȴ���H����Ũ�ȣ���Һ���������ԣ�
�۸��ݻ��ϼ۴�����ΪO����P�Ļ��ϼ�Ϊx����3��1��x��2��(��2)=0����x=��1��P�Ļ��ϼ�Ϊ+1��
(2)Ag����ԭ��Ag��Ag��Ϊ�����������ϼ۽���1�ۡ�H3PO2����ΪH3PO4��H2PO2����ԭ�����仯�ϼ۴ӣ�1���ߵ���5������4�ۣ����ϼ������غ㣬�������ͻ�ԭ���ı���Ϊ4��1��
(3)PH3��P�Ļ��ϼ�Ϊ��3�����ϼ۴�0���͵���3���ܹ�������3�ۡ�Ba(H2PO2) 2��P�Ļ��ϼ�Ϊ��1��������2��P�����ϼ��ܹ�����2�ۡ�P4�������绯��Ӧ�����ϼ������غ㣬��PH3��Ba(H2PO2) 2�ı���Ϊ2��3���ٸ���ԭ���غ���ƽ����ѧ����ʽΪ2P4+3Ba(OH)2��6H2O =2PH3��3Ba(H2PO2)2��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������и������ʻ�����
��O2��O3����12C��14C����CH4��C7H16����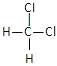 ��
��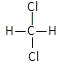 ����
����![]() ��
��![]() ��
��
��1������˵����ȷ����______��
A.����������Ϊͬλ��
B.���黥Ϊͬ��������
C.���������ʻ�Ϊͬϵ��
D.���������ʻ�Ϊͬ���칹��
E.���黥Ϊͬ���칹��
��2���л���![]() ������Ϊ______��
������Ϊ______��
��3����һ��Clȡ��![]() ���е�һ����ԭ�ӿ��Եõ�______�ֽṹ��ͬ���л��
���е�һ����ԭ�ӿ��Եõ�______�ֽṹ��ͬ���л��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Na��CO2����ؿɽ� CO2 ���Ϊ�����ҹ�������Ա���Ƴ��Ŀɳ����Na��CO2����أ����Ʋ��Ͷ��̼���ܣ�MWCNT��Ϊ�缫���ϣ��ŵ�ʱ�ܷ�Ӧ�Ļ�ѧ����ʽΪ 4Na��3CO2=2Na2CO3��C���ŵ�ʱ�õ����������CO2���乤��ԭ����ͼ��ʾ������˵���в���ȷ����
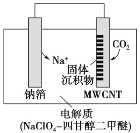
A.��������Ϊ MWCNT���������Ʋ�
B.�ŵ�ʱ�������ĵ缫��ӦʽΪ 3CO2��4Na����4e��=2Na2 CO3��C
C.ѡ�ø����������ĸʴ������������Һ���ŵ��ǵ����Ժã���������Ʒ�Ӧ���ѻӷ�
D.ԭ���缫������ȣ������ɵ�Na2CO3 ��C ȫ�������ڵ缫���棬��ת�� 0.2 mol e��ʱ��������������Ϊ 11.2 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����500mLNH4HCO3��Na2CO3�Ļ����Һ��Ϊ��ȷ֣�ȡһ�ݼ��뺬amol�������Ƶ���Һǡ�÷�Ӧ��ȫ����ȡһ�ݼ��뺬bmolHCl������ǡ�÷�Ӧ�����ٲ���CO2����û����Һ��c��Na+��Ϊ�� ��
A. ��![]() ��molL-1
��molL-1
B. ��2b-a��molL-1
C. ��5b-![]() ��molL-1
��molL-1
D. ��10b-5a��molL-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NH3��CO��Na��Na2O2��Fe��NO��NO2��F2��SO2��SOCl2�����ʣ��������ǵ���ɼ����ʽ������·��ࣺ
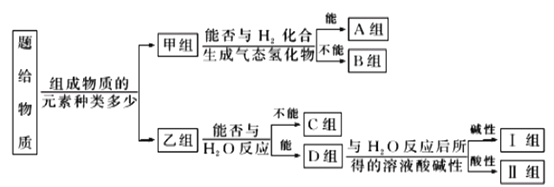
��ش��������⣺
��1��ͼ����ʾ�ķ������___________��
��2������ɫ��������λ��__________�飬���ĵ���ʽΪ___________��
��3��B������һ�������ڸ���������ˮ������Ӧ�����÷�Ӧ��������8��6.02��1023������ת�ƣ�����__g�����ʲ��뷴Ӧ��
��4��C����һ�����峣������ҵ��ұ�����Ļ�ԭ����д������������ԭFe2O3�Ļ�ѧ����ʽ___________��
��5��II��ij����������ˮ����������ԭ��Ӧ���÷�Ӧ�б�����Ԫ���뱻��ԭ��Ԫ�ص�������Ϊ___________��
��6��II������һ�����ʵ���ˮ�к���ˮ���ҷ�Ӧ��Ԫ�ػ��ϼ۲������仯����������ˮ��Ӧ�Ļ�ѧ����ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.02mol��L-1CuSO4��Һ�����ٵμ�1mol��L-1��ˮ���ȹ۲쵽��dz��ɫ����[Cu2(OH)2SO4]���ɣ�������ܽ⣬��Ϊ����ɫ��Һ����ʵ�������ϵ��pH�͵絼����ʱ��ı仯��ͼ��ʾ������˵����ȷ����
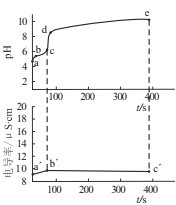
A.c(Cu2+)��a��=b��
B.bc������dz��ɫ�����ķ�ӦΪ![]()
C.d��ʱ��![]()
D.����������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��Ru�������g-C3N4���Ϲ������CO����ԭΪHCOOH��ԭ��ͼ��ͼ��ʾ��
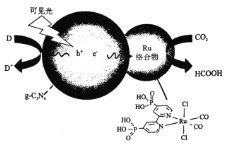
��1����̬̼ԭ�ӵļ۵����Ų�ͼΪ_____________��
��2��1molHCOOH�к��еĦҼ���ĿΪ_____________��HCOOH�ķе��CO2�ߵ�ԭ��Ϊ_____________��
��3��Ru������еڶ�����Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ_____________
��4��Ru���������Ru��λ��ԭ����N��_____________��
��5��Ru����ﺬ�е�Ƭ��![]() ��
��![]() �е�ԭ�Ӿ�����sp2�ӻ��������ڴ�м�����ԭ����λ������ǿ����_____________���ǰ�ߡ����ߡ�����
�е�ԭ�Ӿ�����sp2�ӻ��������ڴ�м�����ԭ����λ������ǿ����_____________���ǰ�ߡ����ߡ�����
��6��һ����ʯī�ľۺ���뵼��g-C3N4���䵥��ƽ��ṹ��ͼ1�������ṹ��ͼ2��

��g-C3N4�е�ԭ�ӵ��ӻ�������_____________��
�ڸ���ͼ2����ͼ1����ƽ���ı��λ���һ����С�ظ���Ԫ��_____________
����֪�þ��������ΪVcm3���м��ԭ�Ӿ��ھ����ڲ����谢���ӵ�������ֵΪNA����g-C3N4���ܶ�Ϊ____g.cm-3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����ʾ������ȷ���ǣ� ��
A.�������������������������ֱ���ȫȼ�գ����߷ų�������
B.��C(ʯī)=C(���ʯ) ��H=+1.9kJ/mol��֪ʯī�Ƚ��ʯ�ȶ�
C.��101kPaʱ��2g H2��ȫȼ������Һ̬ˮ�ų�285.8 kJ��������ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ2H2(g)+O2(g) =2H2O(l) ��H= -285.8 kJ/mol
D.��ϡ��Һ�У�H+(aq)+OH-(aq) =H2O(l) ��H= -57.3 kJ/mol��������1mol H2SO4 �뺬1mol Ba(OH)2��ϡ��Һ��ϣ��ų�����������114.6 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ���������ֵ������˵����ȷ���ǣ� ��
A. 28g��ϩ����ϩ�Ļ������������ԭ����Ϊ6NA
B. 28g��ϩ�������õ��Ӷ���ĿΪ4NA
C. ��״���£�11.2 L�ȷ£�CHCl3������������Ϊ0.5 NA
D. 78g���к���C��C����ĿΪ3NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com