
【题目】有下列各组物质或微粒:
①O2和O3;②12C和14C;③CH4和C7H16;④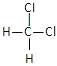 和
和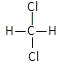 ;⑤
;⑤![]() 和
和![]() 。
。
(1)下列说法正确的是______。
A.①组两微粒互为同位素
B.②组互为同素异形体
C.③组两物质互为同系物
D.④组两物质互为同分异构体
E.⑤组互为同分异构体
(2)有机物![]() 的名称为______。
的名称为______。
(3)用一个Cl取代![]() 分中的一个氢原子可以得到______种结构不同的有机物。
分中的一个氢原子可以得到______种结构不同的有机物。
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.CH3Cl(g)+Cl2(g)![]() CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0
CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0
B.室温下,稀释0.1 mol·L1 NH4Cl溶液,溶液中![]() 增大
增大
C.反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0达平衡后,降低温度,正反应速率增大、逆反应速率减小,平衡向正反应方向移动
2NH3(g) ΔH<0达平衡后,降低温度,正反应速率增大、逆反应速率减小,平衡向正反应方向移动
D.向硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,向沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到。
![]() +H2SO4
+H2SO4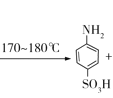 H2O
H2O
已知:苯胺是一种无色油状液体,微溶于水,易溶于乙醇,熔点6.1℃,沸点184.4℃。对氨基苯磺酸是一种白色晶体,微溶于冷水,可溶于沸水,易溶于碱性溶液,不溶于乙醇。实验室可用苯胺、浓硫酸为原料,利用如图所示实验装置合成对氨基苯磺酸。
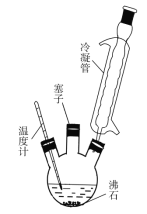
实验步骤如下:
步骤1:在250 mL三颈烧瓶中加入10 mL苯胺及几粒沸石,将三颈烧瓶放在冰水中冷却,小心地加入18 mL浓硫酸。
步骤2:将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5小时。
步骤3:将反应产物冷却至约50℃后,倒入盛有100 mL冷水的烧杯中,用玻璃棒不断搅拌,促使对氨基苯磺酸晶体析出。将烧瓶内残留的产物冲洗到烧杯中,抽滤,洗涤,得到对氨基苯磺酸粗产品。
步骤4:将粗产品用沸水溶解,冷却结晶,抽滤,收集产品,晾干可得纯净的对氨基苯磺酸。
(1)装置中冷凝管的作用是__________。
(2)步骤2油浴加热的优点有____________________。
(3)步骤3中洗涤沉淀的操作是______________。
(4)步骤3和4均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先__________,然后__________,以防倒吸。
(5)若制得的晶体颗粒较小,分析可能的原因______(写出两点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中对应关系正确的是
A | CH3CH3+Cl2 | 均为取代反应 |
B | 由油脂得到甘油 | 均发生了水解反应 |
C | Cl2+2Br=2Cl+Br2 | 均为单质被还原的置换反应 |
D | 2Na2O2+2H2O+4NaOH+O2↑ | 均为水作还原剂的氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于4NH3(g)+3O2(g)=2N2(g)+6H2O(g)的反应来说,以下化学反应速率的表示中反应速率最快的是( )
A.v(NH3)=0.6mol·L-1·s-1B.v(O2)=0.4mol·L-1·s-1
C.v(N2)=0.2mol·L-1·s-1D.v(H2O)=1.2mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质之间的化学反应,反应产物一定为纯净物的是( )
A. 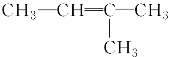 ―→
―→
B. CH2===CH—CH2—CH3+HCl![]()
C. CH3—CH===CH2+H2O![]()
D. nCH2===CH2+nCH2===CH—CH3![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应四个反应类型的说法正确的是

A. 复分解反应、复分解反应、化合反应、置换反应
B. 中和反应、置换反应、复分解反应、置换反应
C. 复分解反应、复分解反应、置换反应、置换反应
D. 分解反应、复分解反应、置换反应、置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学为探究H2O2、H2SO3、Br2的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。

实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为红棕色 |
Ⅱ | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
请回答下列问题:
(1)A中反应的离子方程式是______。
(2)实验操作Ⅱ吹入热空气的目的是_____。
(3)装置C的作用是_____,C中盛放的药品是_____。
(4)实验操作Ⅲ,混合液逐渐变成红棕色,其对应的离子方程式是_____。
(5)由上述实验得出的结论是______。
(6)实验反思:
①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是(写出一条即可)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)①H3PO2是一元中强酸,写出其电离方程式______________________。
②NaH2PO2为___________(填“正盐”或“酸式盐”),其溶液显___________(填“弱酸性”“中性”或“弱碱性”)。
③H3PO2中,P元素的化合价为___________;
(2)H3PO2可用于化学镀银,反应中Ag+还原为银,H3PO2氧化为H3PO4,该反应中氧化剂与还原剂的物质的量之比为________。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4 反应,写出白磷与Ba(OH)2溶液反应的化学方程式______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com