
【题目】多晶硅被称为“微电子大厦的基石”,制备中副产物以SiCl4为主,它对环境污染很大,能遇水强烈水解,放出大量的热。研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成份为BaCO3,且含有铁、镁等离子)制备BaCl2·2H2O,工艺流程如下:
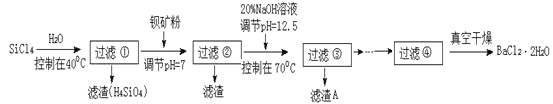
已知:常温下Fe3+、Mg2+完全沉淀的pH分别是:3.4、12.4。
(1)SiCl4水解反应的化学方程式为_________________________________________________。过滤操作需要的玻璃仪器有_________________________________。
(2)加钡矿粉调节pH=7的作用是________________________、_______________________。
(3)加20% NaOH调节pH=12.5,得到滤渣A的主要成分是_______________________。
(4)BaCl2滤液经__________、_________、过滤、洗涤,再经真空干燥后得到BaCl2·2H2O。
(5)10吨含78.8 % BaCO3的钡矿粉理论上最多能生成BaCl2·2H2O_________吨。实际产量为9.70吨,相对误差为__________________%。
【答案】SiCl4+4H2O→H4SiO4↓+4HCl 烧杯、漏斗、玻璃棒 使BaCO3转化为BaCl2 使Fe3+完全沉淀 Mg(OH)2 蒸发浓缩 冷却结晶 9.76 -0.61
【解析】
(1)根据水解机理相当于水中的羟基取代了氯原子,即SiCl4水解反应的化学方程式为SiCl4+4H2O→H4SiO4↓+4HCl。过滤操作需要的玻璃仪器有烧杯、漏斗、玻璃棒。
(2)加钡矿粉调节pH=7的作用是使BaCO3转化为BaCl2,使Fe3+完全沉淀。
(3)根据题中信息,常温下Fe3+、Mg2+完全沉淀的pH分别是:3.4、12.4。加20% NaOH调节pH=12.5,主要是沉淀镁离子,得到滤渣A的主要成分是Mg(OH)2。
(4)BaCl2滤液经蒸发浓缩、冷却结晶,过滤、洗涤,再经真空干燥后得到BaCl2·2H2O。
(5)反应关系式为
BaCO3~BaCl2·2H2O
197 244
10×78.8% m
m=![]() =9.76吨
=9.76吨
相对误差=![]() =-0.61%。
=-0.61%。


科目:高中化学 来源: 题型:
【题目】实验室制备苯甲醇和苯甲酸的化学原理是
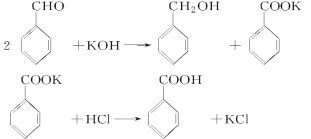
已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3 ℃;苯甲酸的熔点为121.7 ℃,沸点为249 ℃,溶解度为0.34 g;乙醚的沸点为34.8 ℃,难溶于水。制备苯甲醇和苯甲酸的主要过程如下所示:
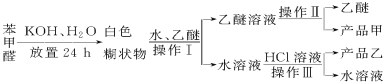
试根据上述信息回答下列问题:
(1)操作Ⅰ的名称是________,乙醚溶液中所溶解的主要成分是________。
(2)操作Ⅱ的名称是________,产品甲是________。
(3)操作Ⅲ的名称是________,产品乙是________。
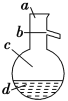
(4)如图所示,操作Ⅱ中温度计水银球上沿放置的位置应是________(填“a”“b”“c”或“d”),该操作中,除需蒸馏烧瓶、温度计外,还需要的玻璃仪器是__________________,收集产品甲的适宜温度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是资源宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。完成下列填空:
(1)氯离子原子核外有_____种不同运动状态的电子、有____种不同能量的电子。
(2)溴在周期表中的位置_________。
(3)卤素单质及其化合物在许多性质上都存在递变规律,请说明下列递变规律的原因。
① 熔点按F2、Cl2、Br2、I2的顺序依次升高,原因是______________。
② 还原性按Cl—、Br—、I—的顺序依次增大,原因是____________。
(4)已知X2 (g) + H2 (g)![]() 2HX (g) + Q(X2 表示Cl2、Br2),如图表示上述反应的平衡常数K与温度T的关系。
2HX (g) + Q(X2 表示Cl2、Br2),如图表示上述反应的平衡常数K与温度T的关系。

① Q表示X2 (g)与H2 (g)反应的反应热,Q_____0(填“>”、“<”或“=”)。
② 写出曲线b表示的平衡常数K的表达式,K=______(表达式中写物质的化学式)。
(5)(CN)2是一种与Cl2性质相似的气体,在(CN)2中C显+3价,N显-3价,氮元素显负价的原因_________,该分子中每个原子都达到了8电子稳定结构,写出(CN)2的电子式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列装置说法正确的是
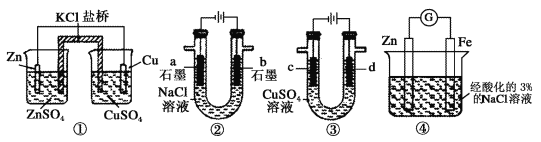
A.装置①中,一段时间后左侧SO42-浓度增大
B.装置②中滴入酚酞,b极附近先变红
C.用装置③精炼铜时,c极为粗铜
D.装置④中在Fe电极附近滴入K3[Fe(CN)6]溶液,可验证Fe电极被保护
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgc(M2+)]与溶液pH的变化关系如图所示,已知该温度下Ksp[Cu(OH)2]<Ksp[Fe(OH)2]。下列说法正确的是( )
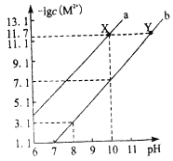
A.曲线b表示Cu(OH)2饱和溶液中的变化关系
B.除去CuSO4溶液中含有的少量Fe2+,可加入适量CuO
C.当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中c(Fe2+)∶c(Cu2+)=104.6∶1
D.向X点对应的饱和溶液中加入少量NaOH固体,可转化为Y点对应的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3溶液可以蚀刻印刷电路板上的Cu。某实验兴趣小组模拟该过程,并回收Cu和蚀刻液的流程如下:
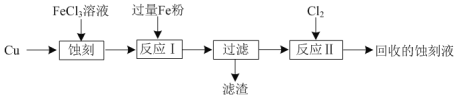
(1)“蚀刻”时的化学反应方程式为____。
(2) 滤渣的成分为____。
(3)“反应Ⅱ”的离子方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分。
(1)NaClO4溶液和NH4Cl溶液混合后发生复分解反应,有NH4ClO4固体析出,写出该反应的化学方程式:____。
(2)通过如下图所示的装置及实验步骤可以测定某高氯酸铵样品的纯度。
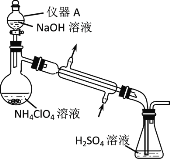
步骤1:检查装置气密性。
步骤2:准确称取样品0.2500 g于蒸馏烧瓶中,加入约150 mL水溶解。
步骤3:准确量取40.00 mL 0.1000 mol·L—1 H2SO4 溶液于锥形瓶中。
步骤4:经仪器A向蒸馏瓶中加入20 mL 3 mol·L—1NaOH 溶液。
步骤5:加热蒸馏至蒸馏烧瓶中剩余约100 mL溶液。
步骤6:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤7:向锥形瓶中加入酸碱指示剂,用0.2000mol·L—1 NaOH标准溶液滴定至终点,消耗NaOH标准溶液30.00 mL。
步骤8:将实验步骤1~7重复2次。
①仪器A的名称是____。
②步骤1~7中,确保生成的氨被稀硫酸完全吸收的实验步骤是____(填步骤序号)。
③计算样品中高氯酸铵的质量分数____(写出计算过程,已知杂质不参与反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
①常温下,强酸溶液的pH=a,将溶液的体积稀释到原来10n倍,则pH=a+n;
②已知BaSO4的Ksp=c(Ba2+)·c(SO42-),所以在BaSO4溶液中有c(Ba2+)= c(SO42-)=![]()
③将0.1mol·L-1的NaHS和0.1mol·L-1Na2S溶液等体积混合,所得溶液中有c(S2-)+2c(OH-)=2c(H+)+c(HS-)+3c(H2S)
④在0.1 mol·L-1氨水中滴加0.1mol·L-1盐酸,刚好完全中和时pH=a,则由水电离产生的c(OH-)=10-amol·L-1
A.①④B.②③C.③④D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,常温下,抽去右图所示装置中的玻璃片,使两种气体充分反应。下列说法正确的是

A.反应前气体的总体积为0. 448 L
B.生成物中含有0.01NA个分子
C.装置中氢元素的总质量为0.04 g
D.生成物完全溶于水后所得溶液含有0.01 NA个F-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com