
【题目】(1)无机化合物可根据其组成和性质进行分类。以下是一组对“一些物质与水反应”的分类图,请按要求填空:

①上述分类中,分成A、B两组的依据是 ;
②C组物质与水反应的离子方程式为 ;
③D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶1的物质有 (填化学式)。
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中,发生还原反应的过程是 → 。
②写出该反应的化学方程式,并标出电子转移的方向和数目____________。
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 。
④H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN)。H2O2被称为绿色氧化剂的理由是____________。
【答案】(1)①与水反应是否是氧化还原反应;
②2Na+2H2O=2Na++2OH-+H2↑;
③Cl2、Na2O2;
(2)①H2CrO4 Cr(OH)3
②2H2CrO4+3H2O2 = 3O2↑+2H2O+2Cr(OH)3
③3.36L
④H2O2作氧化剂,其还原产物是H2O;H2O没有毒性及污染性;
【解析】
试题分析:(1)①上述分类中,A组的物质与水反应,元素的化合价都没有发生变化,B组中元素的化合价发生了变化。因此分成A、B两组的依据是与水反应是否是氧化还原反应;
②在C组的物质中,与水发生反应,水只作氧化剂的是Na,Na与水反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑;
③D组物质Cl2、Na2O2、NO2与水反应中,水即不作氧化剂,也不作还原剂,反应的方程式是:Cl2+H2O= HCl+HClO;该反应中氧化剂和还原剂物质的量之比为1∶1,符合题意;2Na2O2+2H2O=4NaOH+O2↑;该反应中氧化剂和还原剂物质的量之比为1∶1,符合题意;3NO2+H2O=2HNO3+NO,该反应中氧化剂和还原剂物质的量之比为1∶2,不符合题意,因此氧化剂和还原剂物质的量之比为1∶1的物质有Cl2、Na2O2;(2)①H2O2→O2的过程中,氧元素的化合价由-1价升到了0价,所以H2O2是还原剂,H2CrO4为氧化剂,发生还原反应H2CrO4→Cr(OH)3;
②根据电子得失守恒可知配平方程式为2H2CrO4+3H2O2 = 3O2↑+2H2O+2Cr(OH)3;
③根据以上分析可知还原剂失去的电子总数为6e-,氧化剂得到的电子总数为6e-,所以电子的转移数目为6e-,反应转移了6mol电子生成3mol氧气,如反应转移了0.3mol电子,则会生成0.15mol即3.36L氧气;
④H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN)。H2O2被称为绿色氧化剂的理由是H2O2作氧化剂,其还原产物是H2O;H2O没有毒性及污染性。


科目:高中化学 来源: 题型:
【题目】反应![]() 在2L的密闭容器中进行,30s后NO的物质的量增加了0.30mol。下列说法正确的是( )
在2L的密闭容器中进行,30s后NO的物质的量增加了0.30mol。下列说法正确的是( )
A.容器中NH3的物质的量一定增加了0.30mol
B.容器中H2O(g)的物质的量至少为0.45mol
C.NH3的平均反应速率为0.010mol/(L·s)
D.NH3、O2、NO、H2O的物质的量之比一定为4:5:4:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用浓硫酸和乙醇反应制备乙烯,若温度过高或加热时间过长,制得的乙稀往往混有CO2、SO2、H2O(气体少量)。请回答下列问题:
(1)试分析CO2和SO2是怎么样产生的? (用一句话说明)。
(2)试用下图所示的装置设计一个实验,验证制得的气体中确实含有CO2和SO2、H2O(g),按气流的方向,各装置的连接顺序是: 。
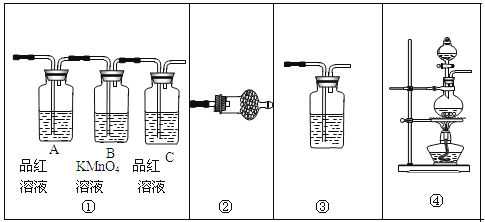
(3)实验时若观察到:①中从左到右A瓶中品红溶液褪色,B瓶中高锰酸钾溶液颜色逐渐变浅,C瓶中品红溶液不褪色,则A瓶的作用是______,B瓶的作用是______,C瓶的作用是______。
(4)装置②中所加的试剂名称是______,它可以验证的气体是______,简述确定装置②在整套装置中的位置的理由是___ ___。
(5)装置③中所盛溶液的名称是______,它可以用来验证的气体是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸性质是中学化学学习的重点。请回答下列问题:
(1)中学化学中利用物质与浓硫酸共热可制备SO2气体,写出用浓硫酸还可制备不同类别的气体的名称: (写一种)。
(2)某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用下图所示装置进行有关实验。
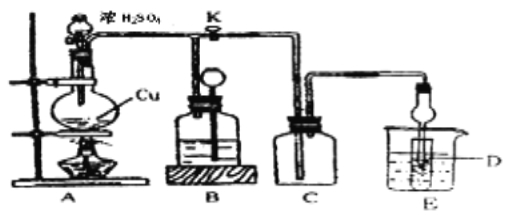
①装置B的作用是贮存多余的气体。B中应放置的液体是_______(填序号)
a.饱和Na2SO3溶液 b.酸性 KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
②反应完毕后,烧瓶中还有一定量的余酸,使用足量的下列药品不能用来证明反应结束后的烧瓶中的确有余酸的是____(填序号)。
a.Fe粉 b.BaCl2溶液 c.CuO d.Na2CO3溶液
③实验中某学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该反应的化学方程式是_________。
④为验证二氧化硫的还原性,C中盛有氯水,充分反应后,取C中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是 (填“I”、“Ⅱ”或“Ⅲ”);C中发生反应的离子方程式为 。D中盛有氢氧化钠溶液,当通入二氧化硫至试管D中溶液显中性时,该溶液中c(Na+)= (用含硫微粒浓度的代数式表示)。
(3)利用FeCl3溶液的氧化性也可以吸收SO2。该反应的离子方程式是 。检验FeCl3是否完全被还原的方法为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届济南一模】高锰酸钾是常用的消毒剂、除臭剂、水质净化剂以及强氧化剂,下图是在实验室中制备KMnO4晶体的流程:
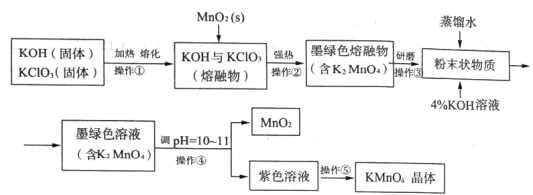
回答下列问题:
(1)操作②目的是获得K2MnO4,同时还产生了KCl和H2O,试写出该步反应的化学方程式: _______________。操作①和②均需在坩埚中进行,根据实验实际应选择_______________(填序号)。
a.瓷坩埚 b.氧化铝坩埚 c.铁坩埚 d.石英坩埚
(2)操作④是使K2MnO4转化为KMnO4和MnO2,该转化过程中发生反应的离子方程式为_______________。若溶液碱性过强,则MnO4-又会转化为MnO42-,该转化过程中发生反应的离子方程式为_______________。因此需要通入某种气体调pH=10-11,在实际操作中一般选择CO2而不是HCl,原因是_______________。
(3)操作⑤过滤时,选择图2所示装置而不用图1所示装置的原因是_______________。
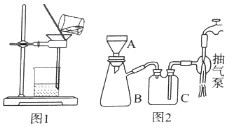
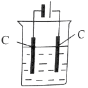
(4)还可采用电解K2MnO4溶液(绿色)的方法制造KMnO4(电解装置如图所示),电解过程中右侧石墨电极的电极反应式为_______________。溶液逐渐由绿色变为紫色。但若电解时间过长,溶液颜色又会转变成绿色,可能的原因是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中蕴藏的元素高达80多种,是人类财富的重要集散地。下图是对海水资源的综合利用的示意图。
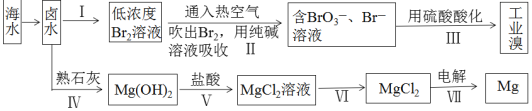
请回答下列问题:
(1)地球上99%以上的溴元素存在于海洋中,资料显示海水中溴的含量约为![]() 。上图中制备溴涉及步骤I、II、III,分别写出步骤II和步骤III中反应的离子方程式: 、 。
。上图中制备溴涉及步骤I、II、III,分别写出步骤II和步骤III中反应的离子方程式: 、 。
(2)制备镁的工艺中,从卤水到![]() 经历了
经历了![]() 的过程,生成
的过程,生成![]() 的过程看似多余,其实该过程的作用是 。
的过程看似多余,其实该过程的作用是 。
(3)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气的冷却剂的是 (填字母序号)。
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂严重影响人体健康,化合物E是一种临床治疗高血脂症的药物。E的合成路线如下(部分反应条件和试剂略):
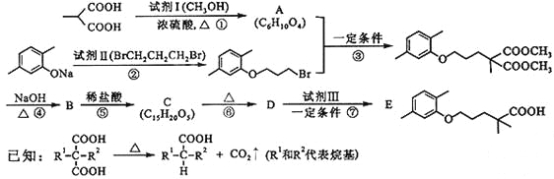
请回答下列问题:
(1)试剂Ⅰ的名称是___a___,试剂Ⅱ中官能团的名称是___b___,第② 步的反应类型是____c___。
(2)第①步反应的化学方程式是_____________。
(3)第⑥步反应的化学方程式是_____________。
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,其结构简式是_________ 。
(5)C的同分异构体在酸性条件下水解,生成X、Y和CH3(CH2)4OH。若X含有羧基和苯环,且X和Y的核磁共振氢谱都只有两种类型的吸收峰,则X与Y发生缩聚反应所得缩聚物的结构简式是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com