
【题目】在一体积固定的密闭容器中,某化学反应2A(g)![]() B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如表:
实验序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)实验1中,在10~20min内,用A表示的该反应的平均速率为________mol·L-1·min-1。
(2)实验2中c2=________,反应经20min就达到平衡,可推测实验2中还隐含的条件是________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3______(填“>”“<”或“=”,下同)v1,且c3_____1.0。
(4)请根据以上实验指出要加快该反应速率可采取的方法:________。(至少列举2种方法)
【答案】0.013 1.0 使用了催化剂 > > 增大反应物A的浓度、升高温度、使用催化剂
【解析】
从反应2A(g)![]() B(g)+D(g)可以看出,反应前后气体的分子数相等,即改变压强平衡不发生移动;从图中数据看,实验1应是参照系。实验2与实验1相比,平衡时A的浓度相同,但达平衡的时间短,由此可推出起始浓度的关系及条件的差异。实验3与实验1相比,10~20分钟内A的浓度变化量大,平衡浓度A也大,由此可推出起始浓度关系。实验4与实验1相比,温度高,达平衡时A的浓度小,由此可推出升高温度对平衡移动的影响。
B(g)+D(g)可以看出,反应前后气体的分子数相等,即改变压强平衡不发生移动;从图中数据看,实验1应是参照系。实验2与实验1相比,平衡时A的浓度相同,但达平衡的时间短,由此可推出起始浓度的关系及条件的差异。实验3与实验1相比,10~20分钟内A的浓度变化量大,平衡浓度A也大,由此可推出起始浓度关系。实验4与实验1相比,温度高,达平衡时A的浓度小,由此可推出升高温度对平衡移动的影响。
(1)实验1中,在10~20min内,c(A)=0.80mol/L-0.67mol/L=0.13mol/L,用A表示的该反应的平均速率为![]() =0.013mol·L-1·min-1。答案为:0.013;
=0.013mol·L-1·min-1。答案为:0.013;
(2)实验2 与实验1 温度相同,则平衡常数相同,平衡时A的浓度相同,则起始浓度相同,实验2中c2=1.0;实验2 达平衡所用时间比实验1 短,则反应速率快,但条件改变没有使平衡发生移动,没有改变平衡浓度,则可推测实验2中还隐含的条件是使用了催化剂。答案为:1.0;使用了催化剂;
(3)设实验3的反应速率为v3,实验1的反应速率为v1,从表中可以看出,10~20分钟内A的浓度变化量大,平衡浓度A也大,则起始浓度也大,反应速率必然快,从而得出v3>v1,且c3>1.0。答案为:>;>;
(4)以上实验,分别从增大浓度、升高温度、使用催化剂进行实验设计,得出条件改变都能加快反应速率的结论,从而得出要加快该反应速率可采取的方法:增大反应物A的浓度、升高温度、使用催化剂。答案为:增大反应物A的浓度、升高温度、使用催化剂。


科目:高中化学 来源: 题型:
【题目】某温度时,VIA元素单质与H2反应生成气态H2X的热化学方程式如下:
1/2O2(g) + H2(g) =H2O(g) ΔH = -242 kJ·mol-1
S(g) + H2(g) =H2S(g) ΔH = -20 kJ·mol-1
Se(g) + H2(g)![]() H2Se(g) ΔH = +81 kJ·mol-1
H2Se(g) ΔH = +81 kJ·mol-1
下列说法正确的是( )
A. 稳定性:H2O > H2S > H2Se
B. 降温有利于Se与H2反应生成H2Se
C. O2(g) + 2H2S(g)=2H2O(g) + 2S(g) ΔH = 444 kJ·mol-1
D. 随着核电荷数的增加,VIA族元素单质与H2的化合反应越容易发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇催化氧化制取乙醛(沸点为20.8℃,能与水混溶)的装置(夹持装置已略)如图所示:
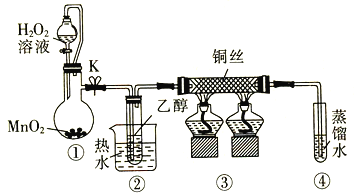
下列说法错误的是
A.向圆底烧瓶中滴入H2O2溶液前需打开K
B.实验开始时需先加热②,再通O2,然后加热③
C.装置③中发生的反应为2CH3CH2OH +O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D.实验结束时需先将④中的导管移出。再停止加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于室温下下列溶液的说法不正确的是( )
编号 | ① | ② | ③ | ④ |
溶液 | 氨水 | 氢氧化钠溶液 | 盐酸 | 醋酸溶液 |
pH | 11 | 11 | 3 | 3 |
A. 水的电离程度:①=②=③=④
B. 分别加水稀释10倍,溶液的pH:①>②>③>④
C. ①③两溶液等体积混合:c(Cl-)>c(NH![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D. V1 L溶液②与V2 L溶液③混合,若V1∶V2=9∶11,则混合溶液pH=4(忽略溶液体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的许多植物中含有醛,其中有些具有特殊香味,可作为植物香料使用,例如桂皮含肉桂醛(![]() ),杏仁含苯甲醛(
),杏仁含苯甲醛(![]() )。下列说法错误的是
)。下列说法错误的是
A. 肉桂醛和苯甲醛互为同系物
B. 肉桂醛能发生加成反应、取代反应和加聚反应
C. 可用新制氢氧化铜悬浊液检验肉桂醛分子中的含氧官能团
D. 1mol肉桂醛分子在一定条件下最多与5mol氢气加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂,工业上可用NO和Cl2合成。回答下列问题:
(1)已知:①2NO2(g)+NaCl(s)NaNO3(s)+NOCl(g) △H1
②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) △H2
③2NO(g)+Cl2(g) 2NOCl(g) △H3
则△H3=_____________(用含△H1、△H2的代数式表示)。
(2)一定温度下,向2L密闭容器中充入amol NOCl(g),发生反应2NOCl(g)2NO(g)+Cl2(g)。
①已知上述反应中正反应速率的表达式为v正=k·cn(NOCl)。300℃时,测得正反应速率与NOCl的浓度的关系如表所示:
c(NOCl)/(mol/L) | v正/(molL-1s-1) |
0.20 | 1.6×10-9 |
0.40 | 6.4×10-9 |
0.60 | 1.44×10-8 |
n=______;k=_____L·mol-1·s-1;当c(NOCl)=0.50 mol·L-1时,v正=_____mol·L-1·s-1。
②测得NO的物质的量浓度与温度的关系如图所示(x<0.5a),T1________T2(填“>”“<”或“=”);T2温度下,该反应的平衡常数K=________mol·L-1(用含a、x的代数式表示)。
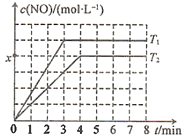
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0. 100mol·L-1的NaOH溶液分别滴定10.00mL浓度均为0.100mol·L-1的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
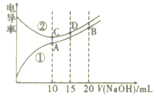
A.曲线②代表滴定CH3COOH溶液的曲线
B.在相同温度下,C、D两点溶液中水的电离程度: C>D
C.取A点溶液1mL加水稀释,溶液中的所有离子浓度都减小
D.B点溶液中: c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑索金是一种爆炸力极强的烈性炸药,比TNT猛烈1.5倍。可用浓硝酸硝解乌洛托品得到黑索金,同时生成硝酸铵和甲醛(HCHO)。下列说法不正确的是( )
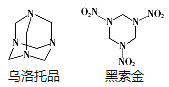
A.乌洛托品的分子式为C6H12N4
B.乌洛托品分子结构中含有3个六元环
C.乌洛托品的一氯代物只有一种
D.乌洛托品得到黑索金反应中乌洛托品与硝酸的物质的量之比为1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在某200mL的稀硫酸和稀硝酸的混合溶液中逐量地加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。(设硝酸只被还原为NO气体,Fe的相对原子质量为56)。下列有关分析错误的是
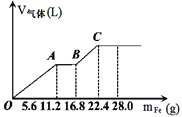
A.原混合酸中NO3-的物质的量为0.2mol
B.原混合酸中H2SO4物质的量浓度为2mol/L
C.OA段与BC段反应中电子转移的物质的量之比为2:1
D.取20mL原混合酸加水稀释至1L后溶液的pH=1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com