
【题目】取浓度均为0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。将浓度均为0.1mol/L、体积均为1L的HA溶液和HB溶液分别加水稀释至体积为VL,溶液pH的变化曲线如图所示,则下列说法正确的是

A.HA是强酸,HB是弱酸
B.X是HB,Y是HA
C.常温下,pH相等的NaA溶液与NaB溶液的物质的量浓度:c(NaA)<c(NaB)
D.NaA与NaB的混合溶液中:c(Na+)+c(H+)=c(A-)+c(B-)+c(HA)+c(HB)
【答案】B
【解析】
试题分析:由反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3可知,酸性:H2CO3>HA>HCO3->HB。A.HA、HB浓度均为0.1mol/L,由图中起点pH值可知,pH(HA)=2,pH(HB)>3,则HA、HB都是弱酸,故A错误;B.加水稀释,促进弱酸的电离。酸性越弱,溶液稀释后pH变化越小,所以相同倍数稀释时,pH变化小的X为酸性更弱的HB,Y为HA,故B正确;C.酸越弱,对应离子的水解能力越强,则水解能力NaB>NaA,因两溶液水解呈碱性且pH相等,则c(NaA)>c(NaB),故C错误;D.NaA与NaB的混合溶液中,根据电荷守恒可得,c(Na+)+c(H+)=c(A-)+c(B-)+c(OH-),故D错误。故选B。


科目:高中化学 来源: 题型:
【题目】分部分中学化学常见元素原子结构及性质如表所示:
序号 | 元素 | 结构及性质 |
① | A | A是一种常见金属,它的一种氧化物是具有磁性的黑色晶体 |
② | B | B是一种常见金属,原子核外有三个电子层且最外层电子为偶数 |
③ | C | C的气态氢化物易液化常作制冷剂 |
④ | D | D为灰黑色具有金属光泽的固体,是太阳能电池板的常用材料 |
⑤ | E | E原子最外层电子数是内层电子总数的3倍 |
⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(1)A原子在周期表中的位置为______________,离子半径:B2+_________C3-(填"大于、小于或等于”)。
(2)简单气态氢化物的热稳定性:D__________E(填"大于、小于或等于”)。
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是________________。
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的电子式为__________,N的结构式为___________。
(4)用化学方程式表明C与E这两种元素的非金属性的强弱_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①参加反应的物质本身的性质是影响化学反应速率的主要因素 ②光是影响某些化学反应速率的外界条件之一 ③决定化学反应速率的主要因素是浓度 ④不管什么反应,增大浓度、加热、加压、使用催化剂都可以加快反应速率
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有以下四种物质 ①22g二氧化碳;②5g氢气;③1.204╳1024个氮气分子; ④4℃时18g水,它们所含分子数最多的是 ;质量最大的是 ;常温时体积最大的是 (填序号)。
(2)已知反应
①SO3+H20=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④2Na+2H2O=4NaOH+H2↑
⑤SiO2+2NaOH=Na2SiO3+H2O
上述反应中不属于氧化还原反应的是 (填序号,下同);属于氧化还原反应,其中H2O被氧化的是____ _ ;H2O被还原的是_ ;属于氧化还原反应,但H2O既不被氧化,也不被还原的是 。
(3)现有下列十种物质:
①蔗糖 ②熔融NaCl ③盐酸 ④铜丝 ⑤NaOH固体 ⑥SO2 ⑦CuSO4固体 ⑧K2O固体 ⑨液态H2SO4⑩液氯
上述物质中可导电的是 (填序号,下同);上述物质中不能导电,但属于电解质的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+Cl2(g)===2HCl(g) ΔH=-184.6 kJ·mol-1,则反应:HCl(g)===1/2H2(g)+1/2Cl2(g)的ΔH为( )
A.+184.6 kJ·mol-1 B.-92.3 kJ·mol-1
C.-369.2 kJ·mol-1 D.+92.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是( )
A.Cu能与浓硝酸反应,但不能与浓盐酸反应
B.Cu与浓硝酸反应比与稀硝酸反应快
C.N2与O2在常温、常压下不反应,放电时可反应
D.Fe与浓盐酸反应比与稀盐酸反应快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用碳酸钠晶体(Na2CO310H2O),配制0.2mol/L的Na2CO3溶液480mL。
(1)所需主要仪器为:药匙、托盘天平、烧杯、玻璃棒、_________和胶头滴管。
(2)本实验所需称量碳酸钠晶体(Na2CO310H2O)_________g;
(3)根据下列操作对所配溶液的浓度产生的影响,完成下列要求。
①Na2CO310H2O晶体失去了部分结晶水
②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有_________,偏低的有__________,无影响的有_________。(填序号)
(4)某同学改用固体Na2CO3配制上述Na2CO3溶液的过程如图所示:
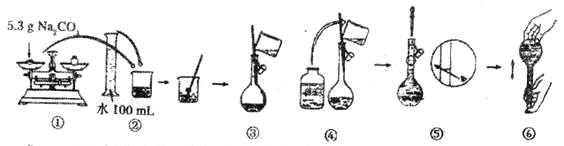
你认为该同学的操作步骤中错误(包含遗漏)之处有___________。
A.1处 | B.2处 | C.3处 | D.4处 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某恒温密闭容器中,投入一定量的A发生可逆反应:A(s)![]() B(g)+C(g),△H=-Q kJ/mol(Q>O)。一段时间后反应达到平衡,然后缩小容器体积,重新达到平衡。下列分析不正确的是
B(g)+C(g),△H=-Q kJ/mol(Q>O)。一段时间后反应达到平衡,然后缩小容器体积,重新达到平衡。下列分析不正确的是
A. 两次平衡时,C(g)的浓度相等
B. 平衡时,单位时间内n(B)生成:n(C)消耗=1:1
C. 若再向平衡体系中加入少量A,平衡不移动
D. 若开始时向容器中加入1 mol B和1 mol C,则达到平衡时吸收QkJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知拆开1 mol氢气中的化学键需要消耗436 kJ能量,拆开1 mol氧气中的化学键需要消耗498 kJ 能量,根据图中的能量图,回答下列问题:

(1)分别写出①②的数值:①___________KJ;②____________KJ。
(2)生成H2O(g)中的1 mol H—O键放出_____________kJ的能量。
(3)已知:H2O(l)==H2O(g) ΔH = + 44 kJ·mol-1,试写出2 mol氢气在足量氧气中完全燃烧生成液态水的热化学方程式___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com