
【题目】如图是s能级和p能级的原子轨道图,试回答下列问题:
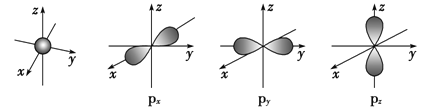
(1)s电子的原子轨道呈______形,每个s能级有______个原子轨道;p电子的原子轨道呈________形,每个p能级有________个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是________电子,其电子云在空间有________方向;元素X的名称是_______,它的氢化物的电子式是____________。若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为________,原子的电子排布图为___________。
【答案】球 1 哑铃 3 2p 三个互相垂直的伸展 氮 ![]() S
S ![]()
【解析】
(1)s电子的原子轨道都是球形的,每个s能级有1个原子轨道;p电子的原子轨道都是哑铃形的,每个p能级有3个原子轨道,它们相互垂直,分别以px、py、pz表示。
(2)因为元素X的原子最外层电子排布式为nsnnn+1,np轨道已排上电子,说明ns轨道已排满电子,即n=2,则元素X的原子核外电子排布式为1s22s22p3,是氮元素,其中原子中能量最高的是2p电子,其电子云在空间有三个互相垂直的伸展方向;氮元素的氢化物是氨气,含有极性键,其电子式是![]() ;当元素X的原子最外层电子排布式为nsn-1npn+1时,根据上述分析,有n-1=2,则n=3,所以X元素的原子核外电子排布式为1s22s22p63s23p4,是硫元素;硫元素的元素符号为S,其原子的电子排布图为
;当元素X的原子最外层电子排布式为nsn-1npn+1时,根据上述分析,有n-1=2,则n=3,所以X元素的原子核外电子排布式为1s22s22p63s23p4,是硫元素;硫元素的元素符号为S,其原子的电子排布图为![]() 。
。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】柔红酮是一种医药中间体,其结构简式如图所示。下列说法正确的是( )
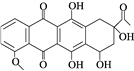
A. 每个柔红酮分子中含有2个手性碳原子
B. 柔红酮分子中所有的碳原子都在同一个平面上
C. 1 mol柔红酮最多可与2 mol Br2发生取代反应
D. 一定条件下柔红酮可发生氧化、加成、消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在柑橘、柠檬等水果中含有柠檬酸,且已知柠檬酸中只含C、H、O三种元素。取柠檬酸19.2g,在氧气中完全燃烧,产生CO2和H2O分别为26.4g和7.2g,现对该物质进行质谱分析,可获得柠檬酸的相对分子质量为192,利用红外光谱分析可知柠檬酸分子中含有﹣COOH和﹣OH。请回答:
(1)通过计算,可获得柠檬酸的分子式为_____。
(2)再利用核磁共振氢谱分析发现有4个吸收峰,其峰面积之比为4:2:1:1.综合以上信息,写出柠檬酸的结构简式_____。
(3)柠檬酸与有机物C在一定条件下发生酯化反应可生成一种相对分子质量为220的酯类物质。写出C所有可能的结构简式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,用0.200molL-1盐酸滴定 20.00mL 0.200 molL-1 的 NaY 溶液,溶液中水的电离程度随所加盐酸的体积变化如图所示(忽略滴定过程中溶液体积变化),则下列有关说法正确的是[已知 Ka(HY)=5.0×10-11]

A.可选取酚酞作为滴定指示剂B.M 点溶液的 pH>7
C.Q 点水的电离程度最小,Kw<l0-14D.M点,c(Na+)=c (HY)+c (Y-)+c (Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型材料 AIN 应用前景广泛,对其制备过程的研究成为热点。
(1)将物质的量均为a mol 的 Al2O3与N2 充入恒温恒容密闭容器中,控制温度发生反应:2Al2O3(s)+2N2(g) ![]() 4AlN(s) +3O2(g) △H>0。
4AlN(s) +3O2(g) △H>0。
①下列可作为反应达到平衡的判据是_________(填序号)。
A.固体的质量不再改变
B.2v正(N2)=3v逆(O 2)
C.△H 不变
D.容器内气体的压强不变
E.N2分子数与 O2 分子数比为 2:3
②在起始压强为p的反应体系中,平衡时 N2的转化率为α,则上述反应的平衡常数 Kp__________(对于气相反应,用某组分 B 的平衡压强 p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp,如p(B) =p总·x(B) ,p总为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
③为促进反应的进行,实际生产中需加入焦炭,其原因是____________。
(2)铝粉与 N2 在一定温度下可直接生成 AlN, 加入少量 NH4Cl 固体可促进反应。将等质量的A1粉与不同量的 NH4Cl混合均匀后置于充 N2的密闭容器中,电火花引燃,产品中 AlN的质量分数[ω(AlN)] 随原料中ω(NH4Cl)的变化如图1所示,燃烧过程中温度随时间变化如图2所示。则:
①固体混合物中,ω(NH4Cl)的最佳选择是__________。
②结合图2解释当ω(NH4Cl)超过一定值后,ω(AlN)明显减少的原因__________。

(3)AIN粉末会缓慢发生水解反应,粒径为100 nm 的 AlN 粉末水解时溶液 pH的变化如图3 所示。

①AlN 粉末水解的化学方程式是______________。
②相同条件下,请在图3中画出粒径为40 nm 的AlN粉末水解的变化曲线____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂辉石(主要成分为LiAl(SiO3)2,还含有Fe2O3、MgO、Al2O3等杂质)是最重要的提锂矿石原料,工业上以α-锂辉石为原料制备碳酸锂,其工艺流程如图:

已知:①α-锂辉石化学惰性大,除HF外,几乎不与任何酸碱反应,α-锂辉石在高温下可转化为β-锂辉石,β-锂辉石具有更高的化学活性。
②β-锂辉石可与浓硫酸发生反应:2β-LiAl(SiO3)2+H2SO4(浓) ![]() Li2SO4+Al2O3·4SiO2·H2O。
Li2SO4+Al2O3·4SiO2·H2O。
③部分金属氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
请回答下列问题:
(1)将LiAl(SiO3)2改写成氧化物的形式为___,1000℃焙烧α-锂辉石的目的为___。
(2)滤渣2的主要成分为___,调节pH值的范围为___。
(3)“除大部分Mg”步骤的离子方程式为___。
(4)实验室蒸发浓缩操作中所需的仪器为酒精灯、铁架台(带铁圈)、___。
(5)洗涤过程中检验沉淀是否洗涤干净的操作为___。
(6)碳酸锂是制备锂离子电池的原料之一,某锂离子电池以CoP3作为负极材料,以LiMn1.5Ni0.5O4作为正极材料,以可传导放电Li+的无机固体电解质c-LATP作为电解液,其工作时电池反应为Li1-xMn1.5N0.5O4+Lix(CoP3)n![]() LiMn1.5Ni0.5O4+(CoP3)n,则该电池放电时负极的电极反应式为___,充电时阳极的电极反应式为___。
LiMn1.5Ni0.5O4+(CoP3)n,则该电池放电时负极的电极反应式为___,充电时阳极的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠与工农业生产、日常生活紧密相关。工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品往往含有少量的NaCl,现欲测定碳酸钠样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀________(填操作名称)、洗涤、烘干、称量。洗涤沉淀的操作是________________________________________.
方案二:气体分析法
(2)用如图所示装置,将一定质量的样品与足量盐酸反应,并测定产生CO2气体的体积,为了使测量结果准确,B中的溶液最好采用________(填字母)。
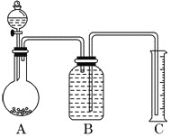
a.饱和碳酸钠溶液 b.饱和碳酸氢钠溶液
c.饱和氢氧化钠溶液 d.氯化钠溶液
但选用该溶液后实验结果仍然不够准确,原因是________________________________
方案三:质量差分析法
(3)采用如图所示装置,将一定质量的样品与足量的稀硫酸反应,通过称量反应前后盛有碱石灰的干燥管的质量,利用其质量差计算样品的纯度。
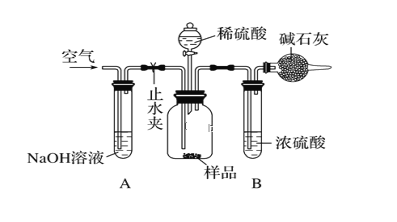
该实验的操作步骤:
①在干燥管内装满碱石灰,质量为m1g ②取ng样品装入广口瓶中 ③检查装置的气密性 ④缓慢鼓入空气数分钟,再称量干燥管质量为m2g ⑤关闭止水夹 ⑥打开止水夹 ⑦缓慢加入稀硫酸至不再产生气体为止 ⑧缓慢鼓入空气数分钟
Ⅰ.正确的操作顺序是(填序号):③→_____→⑥→_____→⑤→________→⑦→________→④。
Ⅱ.在操作④中,要缓慢鼓入空气数分钟,鼓入空气的作用是________________;装置 B的作用是__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO,其过程如下:mCeO2 (m-x)CeO2·xCe+xO2;(m-x)CeO2·xCe+xH2O+xCO2
(m-x)CeO2·xCe+xO2;(m-x)CeO2·xCe+xH2O+xCO2![]() mCeO2+xH2+xCO
mCeO2+xH2+xCO

下列说法不正确的是( )
A.该过程中CeO2没有消耗B.该过程实现了太阳能向化学能的转化
C.图中ΔH1=ΔH2+ΔH3D.H2(g)+O2(g)=H2O(g)的反应热大于ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的CO2气体通入2L的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与消耗的HC1物质的量关系如图所示(忽略气体的溶解和HC1的挥发).下列说法不正确的是
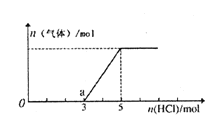
A. 0点溶液中所含溶质的化学式为NaOH、Na2CO3
B. 0到a点发生反应的离子方程式:H++OH-=H2O、CO32-+H+=HCO3-
C. 通入CO2气体的体积在标准状况下为22.4L
D. NaOH溶液的物质的量浓度为2.5mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com