
| A. | 因为水果中一般含有各种芳香族有机酸,食用时能感到较强的酸味,刺激食欲 | |
| B. | 猪肉因含有 而有香味,该物质属于烃的衍生物,能发生加聚反应 而有香味,该物质属于烃的衍生物,能发生加聚反应 | |
| C. | 除去苯中 的方法:加溴水,充分振荡,静置分液 的方法:加溴水,充分振荡,静置分液 | |
| D. | 在分子筛固体酸作催化剂的条件下,用苯和丙烯反应制备异丙苯,符合绿色化学工艺 |
分析 A.水果中一般还含有各种芳香族有机酸,苯甲酸和水杨酸是两种最主要的芳香族有机酸;
B. 含有N=C键,可发生加聚反应,含有N、S元素,为烃的衍生物;
含有N=C键,可发生加聚反应,含有N、S元素,为烃的衍生物;
C.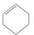 与溴单质发生加成反应生成1,2-二溴环己烷,该有机物能够溶于苯;
与溴单质发生加成反应生成1,2-二溴环己烷,该有机物能够溶于苯;
D.“绿色化学工艺”是防止污染的基本手段,其理想状态是参加的原子全部转化为某种需要的产物,即原子的利用率为100%.
解答 解:A.由于水果中一般还含有各种芳香族有机酸,苯甲酸和水杨酸是两种最主要的芳香族有机酸,食用时能感到较强的酸味,刺激食欲,故A正确;
B. 含有N=C键,可发生加聚反应,含有N、S元素,为烃的衍生物,故B正确;
含有N=C键,可发生加聚反应,含有N、S元素,为烃的衍生物,故B正确;
C.由于 与溴反应生成产物易溶于有机溶剂苯,所以无法通过分液操作分离,故C错误;
与溴反应生成产物易溶于有机溶剂苯,所以无法通过分液操作分离,故C错误;
D.采用分子筛固体酸作为苯和丙烯反应的催化剂来制备异丙苯,反应物完全转化成生成物,原子的利用率为100%,符合绿色化学工艺,故D正确;
故选C.
点评 本题考查了有机物结构与性质、物质的分离与提纯方法判断,题目难度不大,注意掌握常见有机物结构与性质,明确绿色化学工艺的概念及判断方法.


 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 化学键的断裂和形成是物质在化学反应中发生能量变化的主要原因 | |
| B. | 水分解生成氢气跟氧气的同时吸收能量 | |
| C. | 1mol H2跟$\frac{1}{2}$mol O2反应生成1mol H2O释放能量一定为245kJ | |
| D. | 为开发氢能,可研究设法将太阳能聚焦,产生高温使水分解产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该化合物既可以与Br2的CCl4溶液发生加成又可以与浓溴水发生取代反应 | |
| B. | 该化合物具有还原性,能被过氧化物氧化,还能与氯化铁溶液反应 | |
| C. | 具有苯环上与阿魏酸相同取代基,又与阿魏酸互为同分异构体的化合物应有8种 | |
| D. | 阿魏酸乙酯的分子式为C12H14O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属性X>Y>Z | |
| B. | X、Y、Z形成的阴离子还原性逐渐增强 | |
| C. | 原子半径X<Y<Z | |
| D. | X、Y、Z的气态氢化物稳定性由弱到强 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | X、Z、Y、W的原子半径依次减小 | |
| B. | 若W与Y的原子序数相差5,则二者形成化合物的化学式可能为Y3W2 | |
| C. | W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 | |
| D. | W与X形成的化合物只含离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com