
【题目】琥珀酸二乙酯是良好的增塑剂和特种润滑剂,也是重要的有机合成的中间体。分析下图中物质间的转化关系,回答问题。

已知:RCN![]() RCOOH
RCOOH
(1)B的结构简式为 。
(2)C的同分异构体中,与C具有相同官能团的是 (写结构简式)。
(3)由C制备琥珀酸二乙酯的化学方程式为: 。
(4)若E为高分子化合物,则由C与D制备E的化学方程式为 。
(5)若E为八元环状化合物,其分子式为 。
【答案】(1)NC-CH2CH2-CN (2)CH3CH(COOH)2
(3)HOOC- CH2CH2-COOH + 2C2H5OH![]() C2H5OOCCH2CH2COOC2H5 +2H2O
C2H5OOCCH2CH2COOC2H5 +2H2O
(4)nHO- CH2CH2-OH + nHOOC- CH2CH2-COOH![]() [OCH2CH2OOCCH2CH2CO]n +2nH2O
[OCH2CH2OOCCH2CH2CO]n +2nH2O
(5)C6H8O4
【解析】
试题分析:根据题中各物质转化关系,乙烯与溴发生加成反应生成A为BrCH2CH2Br,A在氢氧化钠水溶液、加热条件下发生水解反应生成D为HOCH2CH2OH,A与NaCN发生取代反应生成B为NCCH2CH2CN,B酸性水解得C为HOOCCH2CH2COOH,C在酸、加热条件下与乙醇发生酯化反应琥珀酸二乙酯为CH3CH2OOCCH2CH2COOCH2CH3,HOOCCH2CH2COOH和HOCH2CH2OH,发生酯化反应生成E,E为可为高分子也可为环状化合物。(1)根据上面的分析可知,B为NC-CH2CH2-CN 。(2)C为HOOCCH2CH2COOH,C的同分异构体中,与C具有相同官能团即有两个羧基,其结构的是CH3CH(COOH)2。(3)C为HOOCCH2CH2COOH,由C制备琥珀酸二乙酯的化学方程式为:HOOC- CH2CH2-COOH + 2C2H5OH![]() C2H5OOCCH2CH2COOC2H5 +2H2O。(4)E为高分子化合物,则由C与D制备E的化学方程式为nHO- CH2CH2-OH + nHOOC- CH2CH2-COOH
C2H5OOCCH2CH2COOC2H5 +2H2O。(4)E为高分子化合物,则由C与D制备E的化学方程式为nHO- CH2CH2-OH + nHOOC- CH2CH2-COOH![]() [OCH2CH2OOCCH2CH2CO]n +2nH2O。(5)若E为八元环状化合物,则可由C与D脱去两分子水制得E,所以E的分子式为C6H8O4。
[OCH2CH2OOCCH2CH2CO]n +2nH2O。(5)若E为八元环状化合物,则可由C与D脱去两分子水制得E,所以E的分子式为C6H8O4。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)基态Cu2+的核外电子排布式为 ,在高温下CuO 能分解生成Cu2O,试从原子结构角度解释其原因: 。根据元素原子的外围电子排布特征,可将周期表分成五个区域,元素Cu属于 区。
(2)下列叙述不正确的是 。(填字母)
a.HCHO和CO2分子中的中心原子均采用sp杂化
b.因为HCHO与水分子间能形成氢键,所以HCHO易溶于水
c.C6H6分子中含有6个σ键和1个大π键,C2H2是非极性分子
d.CO2晶体的熔点、沸点都比二氧化硅晶体的低,原因是CO2为分子晶体而二氧化硅是原子晶体
(3)氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。其中的C的杂化类型为 ,写出一种与 CN— 互为等电子体的单质分子式 。
(4)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
① 与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 。
② 六氰合亚铁离子[Fe(CN)6]4 -中不存在 。
a.共价键
b.非极性键
c.配位键
d.σ键
e.π键
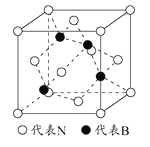
(5)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其晶胞结构与金刚石类似,一个该晶胞中含有 个氮原子, 个硼原子,设氮原子半径为a pm,硼的原子半径b pm ,求该晶胞的空间利用率 。(用含a、b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年8月12日23:30左右,天津滨海新区某公司仓库发生爆炸,事发仓库里存放了大量的硝酸铵、氰化钠(NaCN)和金属钠等危险化学品。
(1)钠在周期表中的位置是 ,实验室少量的钠保存于 中。
(2)NaCN的电子式是 。
(3)氰化钠是一种重要的化工原料,也是剧毒危险品,皮肤伤口接触、吸入、吞食微量可中毒死亡。氰化钠易溶于水,水溶液呈强碱性。氰化钠泄露可用双氧水或硫代硫酸钠中和。
①用离子方程式表示其水溶液呈强碱性的原因: 。
②用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的离子方程式 ;
③用硫代硫酸钠中和的离子方程式为:CN-+S2O32- = A+SO32-,A为 (填化学式)。
④可用纯碱、焦炭、氨气反应制取NaCN,写出反应的化学方程式,并用单线桥标明电子转移的方向和数目 。
(4)CN-中C元素显+2价, N元素显-3价,则非金属性N C(填<、=或>),请用简单的实验方法证明(要求说明简单操作、现象和结论): 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的位置如图所示。下列说法中正确的是

A. W的最高价氧化物对应的水化物是强酸
B. Y的原子半径在同周期主族元素中最大
C. W的非金属性比Z的弱
D. Z的气态氢化物的稳定性在同主族元素中最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中的杂质(括号内的物质)除去时,所使用的试剂和主要操作都正确的是( )
选项 | 物质 | 使用的试剂 | 主要操作 |
A | 乙醇(水) | 金属钠 | 过滤 |
B | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
C | 苯(苯酚) | 浓溴水 | 振荡、分液 |
D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ⅰ.质谱分析测得有机化合物A的相对分子质量为92.5,含有碳、氢、氯三种元素,且氢的质量分数为9.73%。
Ⅱ.A有如下的转化关系

Ⅲ.与羟基相连的碳上没有氢原子的醇(结构: )不能氧化成醛或酮。
)不能氧化成醛或酮。
Ⅳ.F的核磁共振氢谱有两种吸收峰,其峰面积之比为9∶1。
Ⅴ.E和G都能和新制的Cu(OH)2悬浊液反应,但反应类型不同,H是一种具有果香味的液体。
根据以上信息回答下列问题
(1)A的结构简式为______________________。
(2)反应⑦的反应类型为_____________________。
(3)D还有两种相同类别的同分异构体在Ⅱ中没有出现,它们的名称分别为______________________________________和______________________________________。
(4)在B的同分异构体中存在顺反异构现象,请写出其反式异构体的结构简式:___________。
(5)写出下列反应的化学方程式:
E与新制的Cu(OH)2悬浊液反应_____________________________________________。
反应⑧_____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com