
【题目】合理处理燃气中的H2S,不仅可资源化利用H2S,还可减少对大气的污染。回答下列问题:
(1)反应2H2S(g)=2H2(g)+S2(g) ΔH=+171.59 kJ·mol-1,该反应可在____(填“低温”“高温”或“任何温度”)下自发进行。
(2)利用H2S代替H2O通过热化学循环可高效制取H2,原理如图a所示:
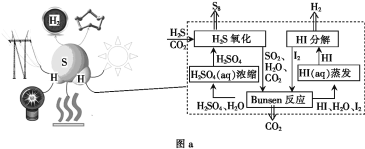
①“Bunsen反应”的离子方程式为________。
②已知键能E(I—I)=152.7 kJ·mol-1,E(H—H)=436.0 kJ·mol-1,E(H—I)=298.7 kJ·mol-1,HI气体分解为碘蒸气和氢气的热化学方程式为________。
③上述循环过程总反应方程式为________。
(3)Ahmed Daham Wiheeb等介绍的一种燃料电池的装置如图b所示:
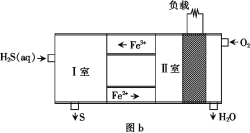
通入O2的电极为________(填“正极”或“负极”),每消耗3.36 L(标准状况下)O2,理论上消耗H2S的质量为____。
(4)为探究H2S直接热解[H2S(g) ![]() H2(g)+
H2(g)+![]() S2(g)],在一密闭容器中充入1 mol H2S与4 mol N2(N2不参与反应),维持总压在101 kPa下进行实验,图c是不同温度下反应时间与H2S的转化率的关系,图d是平衡时气体组成与温度的关系。
S2(g)],在一密闭容器中充入1 mol H2S与4 mol N2(N2不参与反应),维持总压在101 kPa下进行实验,图c是不同温度下反应时间与H2S的转化率的关系,图d是平衡时气体组成与温度的关系。
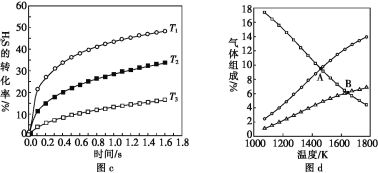
①图c中温度由高到低的顺序是________。
②图d中A点H2S的平衡转化率为______,B点时反应的平衡常数Kp=____(已知![]() ≈10)。
≈10)。
【答案】高温 SO2+I2+2H2O=4H++2I-+SO42- 2HI(g) ![]() H2(g)+I2(g) ΔH=+8.7 kJ·mol-1 8H2S
H2(g)+I2(g) ΔH=+8.7 kJ·mol-1 8H2S![]() 8H2+S8 正极 10.2 g T1>T2>T3 50% 5
8H2+S8 正极 10.2 g T1>T2>T3 50% 5
【解析】
判断反应能否自发进行,根据自由能判据△G=△H-T△S,△G<0才能自发进行;而在分析循环反应的流程图时,要看箭头方向和进来、出去的物质,找出循环的物质,分析总反应,上述流程图中,进入的是H2S和CO2,出来的是H2和S8以及CO2,可分析出是H2S分解成了H2和S8。
(1)反应的焓变△H>0,△S>0,要使得△H-T△S<0,则需要在高温下进行反应,故答案为:高温;
(2)①“Bunsen反应”是SO2、I2、H2O反应生成H2SO4和 HI,故离子方程式为SO2+I2+2H2O=4H++2I-+SO42-,故答案为:SO2+I2+2H2O=4H++2I-+SO42-;
②反应热ΔH =反应物键能总和-生成物键能总和,故2HI(g)H2(g)+I2(g)的反应热为:298.7×2-436.0-152.7=8.7kJmol-1,故答案为:2HI(g) ![]() H2(g)+I2(g) ΔH=+8.7 kJ·mol-1;
H2(g)+I2(g) ΔH=+8.7 kJ·mol-1;
③上述流程图中,进入的是H2S和CO2,出来的是H2和S8以及CO2,可分析出是H2S分解成了H2和S8,故总反应方程式为8H2S![]() 8H2+S8,故答案为:8H2S
8H2+S8,故答案为:8H2S![]() 8H2+S8;
8H2+S8;
(3)该燃料电池是硫化氢失去电子,氧气得到电子,故通入O2的电极为正极,根据电子守恒,得出关系式:2H2S~O2,当氧气的物质的量为0.15 mol时,H2S为0.3mol,质量为0.3×34g=10.2g,故答案为:正极,10.2 g;
(4)①分解反应为吸热反应,温度越高,H2S的转化率越大,故答案为:T1>T2>T3:
②图d中A点表示H2S和H2的物质的量相等,根据方程式H2S(g) ![]() H2(g)+
H2(g)+![]() S2(g)可知H2S反应了一半,转化率为50%;B点时:
S2(g)可知H2S反应了一半,转化率为50%;B点时:
H2S(g) ![]() H2(g)+
H2(g)+![]() S2(g)
S2(g)
起始物质的量 1 0 0
改变的物质的量 2x 2x x
B点物质的量 1-2x 2x x
由图可知H2S的物质的量等于S2的物质的量,由等式1-2x= x,得x=![]() ,则B点气体总物质的量为(
,则B点气体总物质的量为(![]() +4)mol,B点H2S的物质的量为
+4)mol,B点H2S的物质的量为![]() mol,H2的物质的量为
mol,H2的物质的量为![]() mol,S2的物质的量
mol,S2的物质的量![]() mol, H2S的体积分数为=
mol, H2S的体积分数为=![]() ,H2的体积分数为
,H2的体积分数为![]() , S2的体积分数为
, S2的体积分数为![]() ,则平衡常数Kp=
,则平衡常数Kp=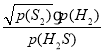 =
=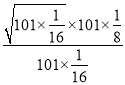 =5;故答案为:5。
=5;故答案为:5。


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 将1mol Cl2通入足量水中,溶液中HC1O、Cl-、ClO-粒子数之和为2NA
B. 100g CaCO3晶体和100g KHSO4晶体中含有的离子数分别为2NA和3NA
C. 标准状况下,4.48L NO和2.24L O2混合后,原子总数为0.6NA
D. 已知3BrF3 + 5H2O=HBrO3 + Br2 + 9HF + O2↑,若有5mol H2O参加反应,则被水还原的BrF3分子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关仪器的使用或实验操作正确的是
A.用稀盐酸洗涤H2还原CuO后试管内壁的铜
B.蒸发时,蒸发皿中溶液的量不能超过总容量的![]()
C.分离苯萃取溴水后的分层液体,从分液漏斗下口先放出水层,再放出有机层
D.用KMnO4溶液测定Na2C2O4的浓度时,KMnO4溶液盛放在碱式滴定管中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某条件下,合成氨反应的数据如下:
N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
起始浓度/mol·L-1 1.0 3.0 0.2
2s末浓度/mol·L-1 0.6 1.8 1.0
4s末浓度/mol·L-1 0.4 1.2 1.4
当用氨气浓度的增加来表示该反应的速率时,下列说法中错误的是 ( )
A. 2s末氨气的反应速率=0.4mol·(L·s)-1
B. 前2s时间内氨气的平均反应速率=0.4mol·(L·s)-1
C. 前4s时间内氨气的平均反应速率=0.3mol·(L·s)-1
D. 2~4s时间内氨气的平均反应速率=0.2mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知金属钠的活泼性非常强,甚至在常温时能和水发生反应2Na+2H2O===2NaOH+H2↑。现将9.2克钠、7.2克镁、8.1克铝分别放入100克10.95%的盐酸中,同温同压下产生气体的质量比是( )
A. 1∶2∶3B. 4∶3∶3C. 8∶6∶9D. 1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入__________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。

①A中发生反应离子方程式为_____________________。
②将仪器连接好以后,必须进行的第一步操作是_____________________。
③B装置出来的气体是否需要干燥_________________。(填“是”或“否”)
④写出装置C中发生的所有反应的化学方程式_____________,______________。
⑤D中NaOH溶液的作用_______________________。
⑥实验结束时,读取实验中生成气体的体积时,不合理的是_______________。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为__________________。
⑧实验完成后E到F之间导管内残留水的体积会使测量结果__________。(填“偏大”、“偏小”或“不影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方法1:铜铝混合物![]() 测定生成气体的体积
测定生成气体的体积
方法2:铜铝混合物![]() 测定生成固体的质量
测定生成固体的质量
下列有关判断中不正确的是( )
A.溶液A和溶液B均可以是盐酸或NaOH溶液B.实验室中方案Ⅱ更便于实施
C.若溶液B选用浓硝酸,测得铜的质量分数偏大D.方案一可能产生氢气,方案二可能剩余铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:![]() 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
A. 若甲为Cl2,则丁可能是铁B. 若甲为NH3,则丁可能是氧气
C. 若甲为AlCl3溶液,则丁可能是氨水D. 若甲为NaOH,则丁可能是SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)NA表示阿伏加德罗常数的数值.46g NO2和N2O4的混合气体中含有_____NA个氧原子;2L0.6 mol·L1 Fe(NO3)3溶液中含_____NA个NO![]() 离子.
离子.
(2)三氟化氮(NF3)是一种气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,
①写出该反应的化学方程式_________________________________
②三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F;据题意推测NF3,F2,NO三种气体中,氧化性由强到弱的顺序为________________________
(3)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮为催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2∶1,写出该反应的化学方程式_________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com