
【题目】某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方法1:铜铝混合物![]() 测定生成气体的体积
测定生成气体的体积
方法2:铜铝混合物![]() 测定生成固体的质量
测定生成固体的质量
下列有关判断中不正确的是( )
A.溶液A和溶液B均可以是盐酸或NaOH溶液B.实验室中方案Ⅱ更便于实施
C.若溶液B选用浓硝酸,测得铜的质量分数偏大D.方案一可能产生氢气,方案二可能剩余铜
科目:高中化学 来源: 题型:
【题目】根据下列实验现象,所得结论正确的是( )
实验 | 实验现象 | 结论 | |
A |
| 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 氧化性:Al3+>Fe2+>Cu2+ |
B |
| 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
C |
| 左边烧杯中无明显变化,右边烧杯中澄清石灰水变浑浊 | 热稳定性:Na2CO3>NaHCO3 |
D |
| 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A 是石油裂解气的主要产物之一,其产量常用于衡量一个国家石油化工发展水平的标志。下列是有机物 A~G 之间的转化关系:
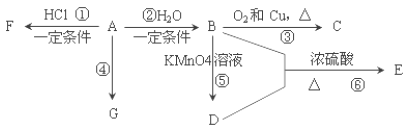
请回答下列问题:
(1)A 的官能团的名称是___________; C 的结构简式是________;
(2)E 是一种具有香味的液体, 由 B+D→E 的反应方程式为___________, 该反应类型是______________;
(3)G 是一种高分子化合物,其结构简式是______________;
(4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质 F(沸点 12.27°C)进行应急处理.写出由A 制 F 的化学反应方程式______________。
(5)E 的同分异构体能与 NaHCO3溶液反应,写出该同分异构体的结构简式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理处理燃气中的H2S,不仅可资源化利用H2S,还可减少对大气的污染。回答下列问题:
(1)反应2H2S(g)=2H2(g)+S2(g) ΔH=+171.59 kJ·mol-1,该反应可在____(填“低温”“高温”或“任何温度”)下自发进行。
(2)利用H2S代替H2O通过热化学循环可高效制取H2,原理如图a所示:
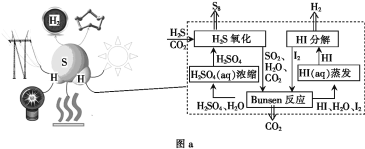
①“Bunsen反应”的离子方程式为________。
②已知键能E(I—I)=152.7 kJ·mol-1,E(H—H)=436.0 kJ·mol-1,E(H—I)=298.7 kJ·mol-1,HI气体分解为碘蒸气和氢气的热化学方程式为________。
③上述循环过程总反应方程式为________。
(3)Ahmed Daham Wiheeb等介绍的一种燃料电池的装置如图b所示:
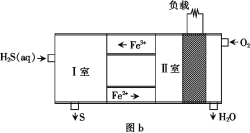
通入O2的电极为________(填“正极”或“负极”),每消耗3.36 L(标准状况下)O2,理论上消耗H2S的质量为____。
(4)为探究H2S直接热解[H2S(g) ![]() H2(g)+
H2(g)+![]() S2(g)],在一密闭容器中充入1 mol H2S与4 mol N2(N2不参与反应),维持总压在101 kPa下进行实验,图c是不同温度下反应时间与H2S的转化率的关系,图d是平衡时气体组成与温度的关系。
S2(g)],在一密闭容器中充入1 mol H2S与4 mol N2(N2不参与反应),维持总压在101 kPa下进行实验,图c是不同温度下反应时间与H2S的转化率的关系,图d是平衡时气体组成与温度的关系。
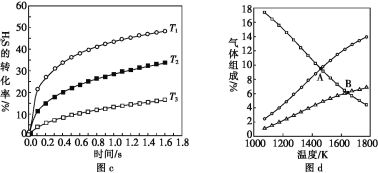
①图c中温度由高到低的顺序是________。
②图d中A点H2S的平衡转化率为______,B点时反应的平衡常数Kp=____(已知![]() ≈10)。
≈10)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某稀溶液中含有0.2 mol HNO3和x mol H2SO4,向其中加入25.6 g铜粉,充分反应后产生的气体在标准状况下的体积为4.48 L,则x值至少为( )
A.0.6B.0.4C.0.3D.0.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
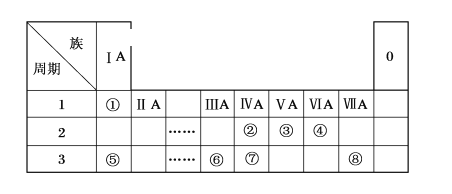
(1)④、⑤、⑥的原子半径由大到小的顺序是_____。(用元素符号表示)
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是____。
(3)③、④、⑥元素可形成含10个电子的微粒,其中A和B为分子,C和E为阳离子,D为阴离子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。用电子式表示下列4种微粒:A_____、B____、C_____、D____。并写出A、B、E三种微粒反应的离子方程式________。
(4)由④⑤⑧三种元素组成的某种盐是家用消毒液的主要成分,将该盐溶液滴入KI淀粉溶液中溶液变为蓝色,则反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化,试回答:

(1)写出B的化学式_______________,D的化学式_______________________。
(2)写出由B转变成E的化学方程式_____________________________。
(3)写出用KSCN鉴别G溶液的离子方程式______________;向G溶液加入A的有关离子反应方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应4NH3+5O2![]() 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(单位皆为molL-1min-1)表示,则下列式子中,正确的是( )
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(单位皆为molL-1min-1)表示,则下列式子中,正确的是( )
A. 4v(O2)=5v(NO)B. 5v(O2)=6v(H2O)
C. 2v(NH3)=3v(H2O)D. 4v(NH3)=5v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为制取纯净干燥的Cl2并让其与铁发生反应的装置,A是Cl2发生装置,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶;烧杯G为尾气吸收装置.试回答:
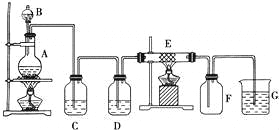
(1)C、G两个装置所盛放的试剂分别是: C G .
(2)①装置搭好须进行气密性检查,写出操作方法: .
②两处酒精灯应先点燃 处(填写A或B),目的是 .
③F中的现象为 ,G中出现了一种沉淀,该沉淀的化学式 .
(3)写出在A、E中发生反应的化学方程式为:
A: .
E: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com