
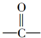 与HCN反应引入:
与HCN反应引入: $→_{一定条件}^{HCN}$
$→_{一定条件}^{HCN}$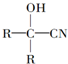
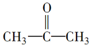 $→_{一定条件①}^{HCN}$A$\underset{\stackrel{{H}_{2}O,{H}^{+}}{→}}{②}$B$→_{③}^{浓H_{2}SO_{4},△}$C$→_{催化剂④}^{聚合}$D
$→_{一定条件①}^{HCN}$A$\underset{\stackrel{{H}_{2}O,{H}^{+}}{→}}{②}$B$→_{③}^{浓H_{2}SO_{4},△}$C$→_{催化剂④}^{聚合}$D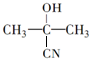 ,D
,D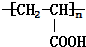 .
. $→_{△}^{浓硫酸}$CH2=CHCOOH+H2O.
$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O.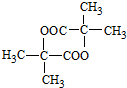 .
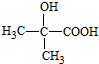
. 分析 丙酮与HCN发生加成反应生成A为 ,A水解生成B为
,A水解生成B为 ,B发生消去反应生成C为CH2=CHCOOH,C发生加聚反应生成D为
,B发生消去反应生成C为CH2=CHCOOH,C发生加聚反应生成D为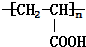 .
.
解答 解:丙酮与HCN发生加成反应生成A为 ,A水解生成B为
,A水解生成B为 ,B发生消去反应生成C为CH2=CHCOOH,C发生加聚反应生成D为
,B发生消去反应生成C为CH2=CHCOOH,C发生加聚反应生成D为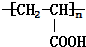 .
.
(1)A的结构简式为,D的结构简式为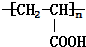 ,故答案为:
,故答案为: ;
;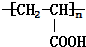 ;
;
(2)有机物B为 ,含有的官能团名称为羧基、羟基,故答案为:羧基、羟基;
,含有的官能团名称为羧基、羟基,故答案为:羧基、羟基;
(3)反应①属于加成反应,反应③属于消去反应,故答案为:加成反应;消去反应;
(4)B→C的化学方程式: $→_{△}^{浓硫酸}$CH2=CHCOOH+H2O,两分子B反应生成的环状酯的结构简式为:
$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O,两分子B反应生成的环状酯的结构简式为: ,
,
故答案为: $→_{△}^{浓硫酸}$CH2=CHCOOH+H2O;
$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O; .
.
点评 本题考查有机物的推断与合成,根据反应条件进行推断,较好的考查学生信息获取与迁移运用,熟练掌握官能团的性质与转化.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题

| A. | HX为弱酸,且电离平衡常数Ka≈1×10-10 | |
| B. | 水的电离程度:M点大于N点 | |
| C. | P点c(Cl-)=0.05mol•L-1. | |
| D. | M点c(HX)-c(X-)>c(OH-)-c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
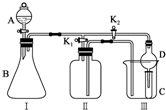

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm互为同位素 | |
| B. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的质量数相同 | |
| C. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm是同一种核素 | |
| D. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm是不同元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时溶液中的H+向负极移动 | |
| B. | 在放电时,正极发生的反应是 Pb(s)+SO42-(aq)=PbSO4(s)+2e- | |
| C. | 在放电时,该电池的负极材料是铅板 | |
| D. | 放电时负极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com