
| m |
| M |
| N |
| NA |
| m |
| M |
| 1 |
| 2 |
| 1 |
| 16 |
| 1 |
| 18 |
| 1 |
| 16 |
| 1 |
| 18 |
| 1 |
| 9 |
| 6.02×1024 |
| 6.02×1023mol-1 |
| 49g |
| 98g/mol |


科目:高中化学 来源: 题型:
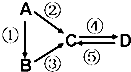 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S2- |
| B、S |
| C、SO32- |
| D、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1s22s22p2和1s22s22p4 |
| B、1s22s22p63s23p4和1s22s22p4 |
| C、1s22s22p63s2和1s22s22p5 |
| D、1s22s22p63s1和1s22s22p63s23p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O2+H2SO4=SO2↑+O2↑+2H2O |
| B、I2+SO2+2H2O=H2SO4+2HI |
| C、2Fe3++2I-=2Fe2++I2 |
| D、2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯碱(Na2CO3) |
| B、绿 矾( FeSO4?7H2O ) |
| C、硫磺(S) |
| D、碱石灰(Ca(OH)2 ) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、该饱和溶液硫酸铜物质的量浓度为 c=
| ||
B、该饱和溶液中硫酸铜的质量分数为ω=
| ||
C、25℃硫酸铜的溶解度为 S=
| ||
D、该饱和硫酸铜溶液的密度为 ρ=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、60克SiO2含有2NA个Si-O共价键 |
| B、实验室中用含4molHCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA |
| C、1L 0.2mol?L-1Al2(SO4)3溶液中的离子总数为NA |
| D、标准状况下,22.4LCO2约含有 3NA个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com