
| A、苯 | B、甲苯 | C、乙烯 | D、乙烷 |


科目:高中化学 来源: 题型:
| A、vA=0.03mol?L-1?min-1 |
| B、vB=0.045 mol?L-1?min-1 |
| C、vC=0.06mol?L-1?min-1 |
| D、vD=0.03 mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验目的 | 玻璃仪器 |
| A | 实验室用浓氨水与生石灰制备并收集NH3 | 普通漏斗、烧杯、玻璃棒 |
| B | 用1mol?L-1NaOH溶液配制96mL0.1mol?L-1NaOH溶液 | 100mL容量瓶、烧杯、胶头滴管、玻璃棒、量筒 |
| C | 用溴乙烷与硝酸银溶液制备且分离出溴化银 | 胶头滴管、试管 |
| D | 用浓硫酸与乙醇制备并收集乙烯 | 圆底烧瓶、酒精灯、导管、集气瓶 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
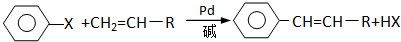 (X为卤原子,R为取代基)
(X为卤原子,R为取代基)
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、需要定期补充硫酸 | ||
| B、放电时电解质的密度减小 | ||
| C、放电时铅是负极,PbO2是正极 | ||
D、放电时负极上发生的反应是Pb+S
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验 | 操作 |
| A | 氨气的收集和检验 | 用向上排空气法收集氨气,并用干燥的红色石蕊试纸放在集气瓶口检验氨气是否收集满 |
| B | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 制备Fe(OH)3胶体 | 将FeCl3固体小心加入沸水中 |
| D | 取出分液漏斗中所需的上层液体 | 从分液漏斗下端管口放出下层液体,关闭活塞,换一个接收容器,从分液漏斗上端口倒出所需液体 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ | C、①④ | D、只有② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com