
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。
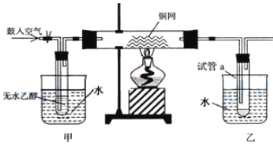
(1)请写出乙醇催化氧化的化学方程式:_____。
(2)反应进行一段时间后,试管a中收集到的主要有机生成物是_____(写名称)。若要检验试管a中收集的该物质,应用_____(试剂名称)来检验,发生的反应方程式为_____。
(3)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有_____。要除去该物质,可在混合液中加入_____(填写序号)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
【答案】2CH3CH2OH+O2![]() 2CH3CHO+2H2O 乙醛 新制Cu(OH)2或银氨溶液 CH3CHO+NaOH+2Cu(OH)2
2CH3CHO+2H2O 乙醛 新制Cu(OH)2或银氨溶液 CH3CHO+NaOH+2Cu(OH)2![]() CH3COONa+Cu2O↓+3H2O或CH3CHO+2Ag(NH3)2OH
CH3COONa+Cu2O↓+3H2O或CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+H2O+2Ag↓+3NH3 乙酸 c
CH3COONH4+H2O+2Ag↓+3NH3 乙酸 c
【解析】
装置甲中进行热水浴,产生乙醇蒸气进入装有铜丝的硬质玻璃管中,而装置乙中进行冷水浴,用于冷却收集得到的氧化产物,鼓入空气是为了保证反应器中有充分的氧气来氧化乙醇,据此来分析题目即可。
(1)乙醇催化氧化可以得到乙醛,方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(2)a中收集到的有机物主要就是乙醇的催化氧化产物,即乙醛,若要检验乙醛,实验室中常用新制![]() 悬浊液或银氨溶液来检验其醛基,发生的反应为CH3CHO+NaOH+2Cu(OH)2
悬浊液或银氨溶液来检验其醛基,发生的反应为CH3CHO+NaOH+2Cu(OH)2![]() CH3COONa+Cu2O↓+3H2O或CH3CHO+2Ag(NH3)2OH
CH3COONa+Cu2O↓+3H2O或CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+H2O+2Ag↓+3NH3;
CH3COONH4+H2O+2Ag↓+3NH3;
(3)石蕊显红色证明有酸性物质产生,可能为乙醛进一步被氧化得到了乙酸,若要除去乙醛中的乙酸,可以考虑选用一种碱性物质,即碳酸氢钠溶液,答案选c。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知氧化性:BrO3->IO3->Br2>I2。向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加KBrO3的物质的量的关系如图所示。请回答下列问题:
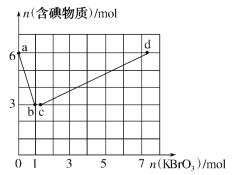
(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为__,还原产物是__。
(2)已知b→c过程中,仅有一种元素发生化合价变化,写出并配平该反应的离子方程式___。
(3)①已知反应:2BrO3-+I2→2IO3-+Br2;有同学由此得出氧化性:I2>Br2的结论,你认为是否正确___,并说明理由:___。
(4)计算c→d过程中消耗KBrO3的物质的量___。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯胺是一种长效缓释水消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2Cl,NHCl2和NCl3)。工业上可利用NH3(g)+Cl2(g) ![]() NH2Cl(g)+HCl(g)制备一氯胺。回答下列问题:
NH2Cl(g)+HCl(g)制备一氯胺。回答下列问题:
(1)氯胺作饮用水消毒剂是因为水解生成具有强烈杀菌作用的物质,该物质是___,二氯胺与水反应的化学方程式为___。
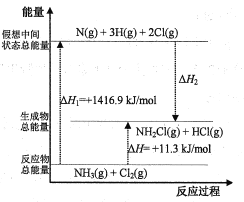
(2)已知部分化学键的键能和化学反应的能量变化如表和如图所示(忽略不同物质中同种化学键键能的细微差别)。
化学键 | N-H | N-Cl | H-Cl |
键能(kJ/mol) | 391.3 | x | 431.8 |
则ΔH2=___kJ/mol,x=___。
(3)在密闭容器中反应NH3(g)+Cl2(g) ![]() NH2Cl(g)+HCl(g)达到平衡,据此反应通过热力学定律计算理论上NH2Cl的体积分数随
NH2Cl(g)+HCl(g)达到平衡,据此反应通过热力学定律计算理论上NH2Cl的体积分数随![]() (氨氯比)的变化曲线如图所示。
(氨氯比)的变化曲线如图所示。
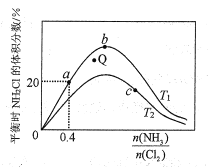
①a、b、c三点对应平衡常数的大小关系是___。T1温度下该反应的平衡常数为___(列出算式即可)。
②在T2温度下,Q点对应的速率:v正___v逆(填“大于”“小于”或“等于”)。
③在氨氯比一定时,提高NH3的转化率的方法是___(任写1种)
④若产物都是气体,实验测得NH2Cl的体积分数始终比理论值低,原因可能是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,用0.100 mol·L-1盐酸分别滴定20.00 mL 0.100 mol·L-1的NaHA和20.00 mL 0.100 mol·L-1 Na2A溶液,两溶液的pH与所加盐酸体积(V)的关系如图所示。下列说法正确的是( )
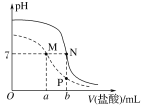
A.HA-的电离常数大于水解常数
B.b=2a
C.M、N点溶液均满足c(Na+)=2c(A2-)+c(HA-)
D.水的电离程度:M=N>P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下实验原理或操作中,正确的是![]()
A.用NaOH溶液滴定盐酸,滴定前尖嘴下端有气泡,滴定后气泡消失,会使结果偏高
B.仰视量筒刻度量取一定量浓硫酸所配制的![]()
![]()
![]() 溶液的浓度结果偏低
溶液的浓度结果偏低
C.焰色反应实验中,铂丝在蘸取待测溶液前应先用稀硫酸洗净并灼烧至无色
D.要将溶解在![]() 中的碘分离出来,应用蒸馏法,因为碘易升华,先分离出来
中的碘分离出来,应用蒸馏法,因为碘易升华,先分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语对事实的表述正确的是
A.硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH![]() C17H35COOC2H5+H218O
C17H35COOC2H5+H218O
B.向Na2SiO3溶液中通入过量的SO2:SiO32-+SO2+H2O=H2SiO3↓+SO32-
C.由Na和C1形成离子键的过程:![]()
D.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在碱的作用下,两分子酯缩合形成β—羰基酯,同时失去一分子醇,该反应称克莱森(R·L·Claisen)酯缩合反应,其反应机理如下:2RCH2COOC2H5![]()
 +C2H5OH。利用Claisen反应制备化合物H的一种合成路线如下:
+C2H5OH。利用Claisen反应制备化合物H的一种合成路线如下:

回答下列问题:
(1)A的名称为__________,C的结构简式为__________。
(2)F中含氧官能团的名称是__________;反应Ⅱ的反应类型是__________。
(3)E→F反应的化学方程式为_________________________________。
(4)B的含有苯环的同分异构体有_____________种(B自身除外),其中核磁共振氢谱显示3组峰的结构简式为__________、__________。
(5)乙酰乙酸乙酯( ![]() )是一种重要的有机合成原料,写出由乙醇制备乙酰乙酸乙酯的合成路线(无机试剂任选)。______________
)是一种重要的有机合成原料,写出由乙醇制备乙酰乙酸乙酯的合成路线(无机试剂任选)。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5mL 0.005mol/L FeCl3溶液和5mL 0.015mol/L KSCN溶液混合,达到平衡后呈红色。再将混合液分为5份,分别进行如下实验:下列说法不正确的是( )
| 实验①:滴加4滴水,振荡 |
实验②:滴加4滴饱和FeCl3溶液,振荡 | |
实验③:滴加4滴1 mol/L KCl溶液,振荡 | |
实验④:滴加4滴1 mol/L KSCN溶液,振荡 | |
实验⑤:滴加4滴6 mol/L NaOH溶液,振荡 |
A.对比实验①和②,为了证明增加反应物浓度,平衡发生正向移动
B.对比实验①和③,为了证明增加反应物浓度,平衡发生逆向移动
C.对比实验①和④,为了证明增加反应物浓度,平衡发生正向移动
D.对比实验①和⑤,为了证明减少反应物浓度,平衡发生逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的理解正确的是
A. 2-丁醇的结构简式:![]()
B. 电子式 ![]() : 可以表示羟基,也可以表示氢氧根离子
: 可以表示羟基,也可以表示氢氧根离子
C. 比例模型 ![]() :可以表示甲烷分子,也可以表示四氯化碳分子
:可以表示甲烷分子,也可以表示四氯化碳分子
D. 聚丙烯的结构简式: ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com