
����Ŀ��ij�о���ѧϰС��������롰�����仯����й����ʵ�ʵ��̽��������ͬ����������⣺
̽��һ
��1����FeCl3��Һ�����ˮ�����Ƶ�Fe(OH)3���壬д�������ӷ�Ӧ__��
��2�����ӹ�ҵ��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ������ӡˢ��·�壬��д��FeCl3��Һ��ͭ��Ӧ�����ӷ���ʽ__��
����ʦ��������ӡˢ��·��ķ�ˮ�л���ͭ�������FeCl3��Һ��������·�����
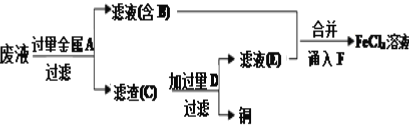
����������Ʒ����������ѧ֪ʶ�ش��������⡣
��3��������ҺE�н��������ӵķ�����__��
��4��ͨ��F������Ӧ�����ӷ���ʽΪ__��
̽����
FeBr2��һ�ֻ���ɫ��Ƭ״�Ĺ��壬ij�о���С����Ҫ90mL0.10mol��L-1FeBr2��Һ���ش��������⣺
��1������FeBr2��Һ���ձ�����Ͳ������������ͷ�ι����IJ���������__��
��2����������ƽ����FeBr2������Ϊ__g��
��3�������й����ƹ�����˵����ȷ����__������ţ���
a.�á���������ij���������������������ʹ�����룩��ƫ��
b.��������FeBr2��������ƿ�У���90mL����ˮ�ܽ�
C.ϴ���ܽ�FeBr2���ձ�������ϴ��Һת��������ƿ��
d.����ƿ��ǩ�����õ�FeBr2��Һ
e.����ʱ����������ƿ�̶���ʹ���Ƶ�FeBr2��ҺŨ��ƫ��
̽����
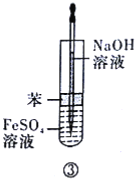
�Ʊ�Fe(OH)2������ͼ��ʾ��װ���У���NaOH��Һ����м��ϡH2SO4���Լ����Ʊ���
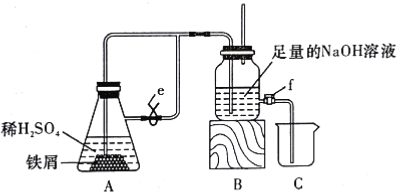
��1��ʵ�鿪ʼʱ������f�رգ���ֹˮ��e��__������رա����ġ�
��2����μ���װ���ڿ����Ѿ��ž���__��
��3���ž�װ���ڿ�����Ϊ���Ƶð�ɫFe(OH)2����������������__��
��4����������f�ŵ�Լ![]() Һ�壬��ʱ�b��B���Լ�ƿ�з����Ļ�ѧ��Ӧ����ʽΪ__��
Һ�壬��ʱ�b��B���Լ�ƿ�з����Ļ�ѧ��Ӧ����ʽΪ__��
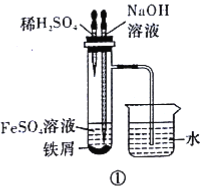
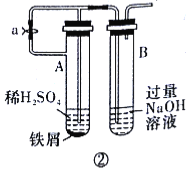
��5�����и�ͼʾ��__������ţ��ܽϳ�ʱ�俴��Fe(OH)2��ɫ������
���𰸡�Fe3++3H2O![]() Fe(OH)3(����)+3H+ 2Fe3++Cu=2Fe2++Cu2+ ȡ������ҺE���Թ��У��ȼ�KSCN��Һ���������ټ�������ˮ����Һ��ΪѪ��ɫ������ҺE�к���Fe2+ 2Fe2++Cl2=2Fe3++2Cl- 100mL����ƿ 2.2 C �� ����Bװ�õ��ܳ��ڴ��ų��������Ĵ��ȣ����ų���H2����ʱ���������ž� �ر�e 4Fe(OH)2+O2+2H2O=4Fe(OH)3 �٢ڢ�
Fe(OH)3(����)+3H+ 2Fe3++Cu=2Fe2++Cu2+ ȡ������ҺE���Թ��У��ȼ�KSCN��Һ���������ټ�������ˮ����Һ��ΪѪ��ɫ������ҺE�к���Fe2+ 2Fe2++Cl2=2Fe3++2Cl- 100mL����ƿ 2.2 C �� ����Bװ�õ��ܳ��ڴ��ų��������Ĵ��ȣ����ų���H2����ʱ���������ž� �ر�e 4Fe(OH)2+O2+2H2O=4Fe(OH)3 �٢ڢ�
��������
̽��һ��1����FeCl3��Һ�����ˮ��������Fe(OH)3������Ȼ��⣬��Ӧ���ӷ���ʽ��Fe3++3H2O![]() Fe(OH)3(����)+3H+��
Fe(OH)3(����)+3H+��
��2��FeCl3��Һ��ͭ��Ӧ�����Ȼ��������Ȼ�ͭ����Ӧ�����ӷ���ʽ��2Fe3++Cu=2Fe2++Cu2+��
��3�����ݷ�������ҺE�е��������Ȼ�������������ҺE���������ӵķ����ǣ�ȡ������ҺE���Թ��У��ȼ�KSCN��Һ���������ټ�������ˮ����Һ��ΪѪ��ɫ������ҺE�к���Fe2+��
��4���Ȼ�������Һͨ�����������Ȼ�����������Ӧ�����ӷ���ʽΪ2Fe2++Cl2=2Fe3++2Cl-��
̽��������1������90mL0.10mol��L-1FeBr2��Һ����Ҫѡ�ù��Ϊ100mL������ƿ������ƽ��ȡһ���������廯���������ձ����ܽ⣬���ò��������裬��ȴ���ò���������ת�Ƶ�100mL������ƿ�У�ϴ���ձ���������2��3�Σ�����ϴ��Һת�Ƶ�����ƿ��������ƿ�м�ˮ��Һ����̶���1��2cmʱ���ý�ͷ�ιܼ�ˮ���̶��ߣ�ҡ�ȣ����ƹ�������Ҫʹ�õ�����Ϊ���ձ�������������ͷ�ιܣ���ȱ�ٵ�����Ϊ100mL����ƿ��
��2������90mL0.10mol��L-1FeBr2��Һ����Ҫѡ�ù��Ϊ100mL������ƿ�� m=0.10mol��L-1��0.1L��216g/mol��2.2g����������ƽ����FeBr2������Ϊ2.2g��
��3��a.���ݡ���=��+�Ρ����á���������ij���������������������ʹ�����룩��ƫС����a����
b.��������FeBr2�����ձ��У�����������ˮ�ܽ⣬��b����
c.Ϊ��֤�廯������ȫ��������ƿ��ϴ���ܽ�FeBr2���ձ�������ϴ��Һת��������ƿ�У���c��ȷ��
d.����ƿ���ܳ��ڱ������ƺõ���Һ����d����
e.����ʱ����������ƿ�̶��ߣ���Һ���ƫ��ʹ���Ƶ�FeBr2��ҺŨ��ƫ�ͣ���e����ѡc��
̽��������1��ʵ�鿪ʼʱҪ�������ų�B�еĿ�����������f�رգ�������ֹˮ��e�Ǵġ�
��2������Bװ�õ��ܳ��ڴ��ų��������Ĵ��ȣ����ų���H2����ʱ���������ž���
��3���ž�װ���ڿ����ر�e��A�е�����������ѹ��B�����������Ʒ�Ӧ������������������ ��
��4����������f�ŵ�Լ![]() Һ�壬��������B������������������Ϊ������������ʱ�b��B�з�����Ӧ�ķ���ʽΪ4Fe(OH)2+O2+2H2O=4Fe(OH)3��
Һ�壬��������B������������������Ϊ������������ʱ�b��B�з�����Ӧ�ķ���ʽΪ4Fe(OH)2+O2+2H2O=4Fe(OH)3��
��5�����Թ������������ų�����������������������������ܽϳ�ʱ�俴��Fe(OH)2��ɫ���������Թ�A�����������ų�B�еĿ���������������������������ܽϳ�ʱ�俴��Fe(OH)2��ɫ�������۱����������������������������������ܽϳ�ʱ�俴��Fe(OH)2��ɫ��������ѡ�٢ڢۡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ����Ҫ�Ļ���ԭ�ϡ������йر���ϩ��˵���������
A. ��Һ���Ϻ�������ۿɷ���ȡ����Ӧ
B. ���Ȼ��ⷴӦ���������ȴ�����ϩ
C. ��ʹ���Ը��������Һ��ɫ
D. �ڴ��������¿����Ƶþ۱���ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���������ۼ��뵽һ��Ũ�ȵ�ϡ�����У�����ǡ����ȫ�ܽ⣬��Ӧ����Һ�д��ڣ�![]() ����μӷ�Ӧ��Fe��HNO3�����ʵ���֮��Ϊ��������
����μӷ�Ӧ��Fe��HNO3�����ʵ���֮��Ϊ��������
A.5��16B.1��1C.2��3D.3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ���ִ�������ԭ������ͨ����ѧ��������ʹ��������������������ʽת�����Ӷ���������Դ�������Դ�������ʣ�
��1��������O2��ȼ�յķ�Ӧ��______�ȷ�Ӧ����š������������������ڷ�Ӧ���������______�������������������ڡ�����С�ڡ����ڡ�����ͬ����
��2���ӻ�ѧ��Ӧ�ı��ʽǶ�������������ȼ�������ڶ��ѷ�Ӧ���еĻ�ѧ�����յ�������______�γɲ���Ļ�ѧ���ų�������������֪�ƻ�1mol H-H����1mol O=O����1mol H-O��ʱ�ֱ���Ҫ����a kJ��b kJ��c kJ����������2mol H2��g����1mol O2��g��ת��Ϊ2mol H2O��g��ʱ�ų�������Ϊ
____________________kJ��
��3��ͨ��������ȼ�շ�Ӧ�������������̺��Ļ�ѧ��ת��Ϊ���ܣ��������������ԭ��Ӧ��Ƴ�ԭ���װ�ã��Ϳ����������̺��Ļ�ѧ��ת��Ϊ���ܣ���ͼ�����ܹ�ʵ�ָ�ת����װ�ã����е������ҺΪKOH��Һ��������Ϊ����ȼ�ϵ�أ��õ�ص�������___����a��b����������ӦʽΪ______________��
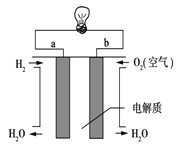
(4)������ͼ�е�����ȼ�ϵ���ù�������������մ�������ʣ��ܹ�����O2��������֪�����Ϸ����ĵ缫��ӦʽΪ��O2��4e��===2O2�����Ϸ����ĵ缫��ӦʽΪ________�����Ӵ�________��(��a��b)������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��ǵ������ڲ���Ԫ�صĵ��������ݣ�����˵����ȷ���ǣ� ��
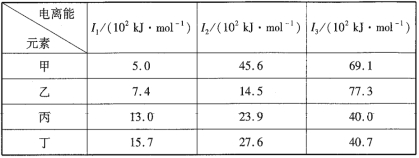
A.�Ľ����Ա�����B.�ҵ���������ϼ�Ϊ+1
C.��һ��Ϊ�ǽ���Ԫ��D.��һ���ǽ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ����������
A. 0.1 mol��L1NaOH��Һ��Na+��K+��![]() ��
��![]()
B. 0.1 mol��L1FeCl2��Һ��K+��Mg2+��![]() ��
��![]()
C. 0.1 mol��L1K2CO3��Һ��Na+��Ba2+��Cl��OH
D. 0.1 mol��L1H2SO4��Һ��K+��![]() ��
��![]() ��
��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2007��ŵ������ѧ�����谣�ض��Ա�������ںϳɰ���Ӧ�������о������������������ڴ�������IJ��ֱ仯������ͼ��ʾ������˵������ȷ����( )
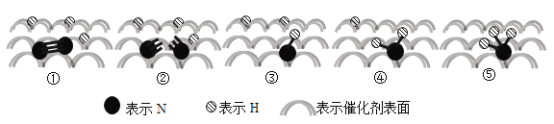
N2(g)+3H2(g)![]() 2NH3(g) ��H = 92 kJ/mol
2NH3(g) ��H = 92 kJ/mol
A.�����¶Ȳ������һ��ʱ����NH3�IJ���
B.ͼ�����ڹ������ȣ�ͼ�����۹��̷���
C.N2�ڷ�Ӧ��������������������
D.��Ӧ�����д���NH��NH2���м����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܱ������н������·�Ӧ:X(g)+3Y(g)![]() 2Z(g)��X��Y��Z��ʼŨ�ȷֱ���0.2mo1/L��0.6mol/L��0.4mol/L�����ﵽƽ��ʱ���������ݿ�����ȷ����
2Z(g)��X��Y��Z��ʼŨ�ȷֱ���0.2mo1/L��0.6mol/L��0.4mol/L�����ﵽƽ��ʱ���������ݿ�����ȷ����
A. XΪ0.25mol/L��ZΪ0.5mol/L B. YΪ1.2mo1/L
C. XΪ0.3mol/L��ZΪ0.3mol/L D. ZΪ0.6mo1/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪһ��������ȼ�����ʾ��ͼ������ˮLiCl-KCl������������ںɹ������õ���ܷ�ӦΪ��PbSO4(s)+2LiCl+Ca(s) = CaCl2(s)+Li2SO4+Pb(s)������˵������ȷ����( )
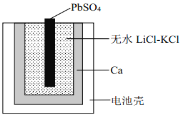
A.PbSO4�缫������ԭ��Ӧ
B.�����ĵ缫��Ӧ��Ca + 2Cl��-2e����CaCl2
C.��LiCl��KClˮ��Һ������ˮLiCl-KCl���ɽ��õ�ظ�Ϊ����ʹ�õĵ��
D.�ŵ�ʱ Li���� K���������ƶ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com