
【题目】化学反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是

A.N2(g)+3H2(g)=2NH3(l) ΔH=2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g)=2NH3(g) ΔH=2(b-a)kJ·mol-1
C.![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
D.![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
科目:高中化学 来源: 题型:
【题目】关于能源,以下说法中不正确的是( )
A.煤、石油、天然气等燃料属不可再生能源
B.煤、石油、水煤气可从自然界直接获取,属一级能源
C.太阳能是一级能源、新能源、可再生能源
D.潮汐能来源于月球引力做功
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.同温同压下,H2(g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H相同
C.生成物的总焓大于反应物的总焓时,反应放热,ΔH<0
D.ΔH的大小与热化学方程式的化学计量数无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,充分燃烧一定量的丁烷放出热量为Q kJ(Q>0),经测定完全吸收生成的CO2需消耗 5 mol·L-1的KOH溶液100 mL,恰好生成正盐,则此条件下反应C4H10(g)+O2(g)===4CO2(g)+5H2O(g)的ΔH为
A.+8Q kJ·mol-1 B. -16Q kJ·mol-1
C.-8Q kJ·mol-1 D. +16Q kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃、101kPa条件下:
①4Al(s)+3O2(g)=2Al2O3(s);△H=-2834.9kJ·mol-1
②4Al(s)+2O3(g)=2Al2O3(s);△H=-3119.1kJ·mol-1
由此得出的正确结论是( )
A.等质量的O2比O3能量低,由O2变O3为吸热反应
B.等质量的O2比O3能量低,由O2变O3为放热反应
C.O3比O2稳定,由O2变O3为吸热反应
D.O2比O3稳定,由O2变O3为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出表示含有8个质子,10个中子的原子的化学符号:____________。
(2)已知阴离子aX2-和阳离子bYn+具有相同的核外电子排布,则a、b、n之间的关系为a=________。
(3)某元素的一种核素的质量数为A,含N个中子,它与1H原子组成HmX分子,在a g HmX中所含质子的物质的量为________mol。
(4)某元素R气态氢化物的化学式为RH3,其最高价氧化物中含氧量为![]() ,已知该元素的原子核内质子数和中子数相等,则该元素的名称为________。
,已知该元素的原子核内质子数和中子数相等,则该元素的名称为________。
(5)下列物质中:①氩单质 ②MgCl2 ③NH4Cl ④CH4 ⑤CO2 ⑥金刚石 ⑦H2SO4 ⑧KOH ⑨Na2O2 ⑩K2O
只存在共价键的是_______(填序号);
属于离子化合物,但含有极性共价键的是______(填序号)。
(6)如图所示每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是______
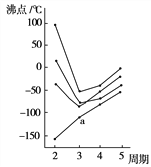
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究固体A的组成和性质,设计实验并完成如下转化。

已知:X由两种化合物组成,若将X通入品红溶液,溶液褪色。若将X通入足量双氧水中,X可全部被吸收且只得到一种强酸,再稀释到1000mL,测得溶液的PH=1。在溶液2中滴加KSCN溶液,溶液呈血红色。请回答:
(1)固体A的化学式______________。
(2)写出反应①的化学方程式____________。
(3)写出反应④中生成A的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下某溶液中由水电离出的离子浓度符合c(H+)·c(OH﹣)=1×10﹣20的溶液,其pH为 ,此时水的电离受到 .
(2)在某温度下,H2O的离子积常数为1×10﹣13 mol2·L﹣2,则该温度下:100mL 0.1mol·L﹣1H2SO4溶液与100mL 0.4mol·L﹣1的KOH溶液混合后,pH= .
(3)已知一溶液有4种离子:X+、Y﹣、H+、OH﹣,下列分析结果肯定错误的是 .
A.c(Y﹣)>c(X+)>c(H+)>c(OH﹣)
B.c(X+)>c(Y﹣)>c(OH﹣)>c(H+)
C.c(H+)>c(Y﹣)>c(X+)>c(OH﹣)
D.c(OH﹣)>c(X+)>c(H+)>c(Y﹣)
(4)在25℃下,将a mol·L﹣1的氨水与0.01mol·L﹣1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl﹣).则溶液显 (填“酸”“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb= .
(5)水溶液中的行为是中学化学的重要内容.已知下列物质的电离常数值:HClO:Ka=3×10﹣8;H2CO3:Ka1=4.3×10﹣7;Ka2=5.6×10﹣11;84消毒液中通入少量的CO2,该反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往1.0 mol·L-1KI溶液中加入固体I2,发生反应:I2(aq)+I- (aq)![]() I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是
I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是

A.该反应的△H>0
B.a、c两点对应的I-反应速率相等
C.b点时0~10s I-的平均反应速率为0.04mol·L-1·s-1
D.d点时该反应在对应温度下处于平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com