
【题目】为探究固体A的组成和性质,设计实验并完成如下转化。

已知:X由两种化合物组成,若将X通入品红溶液,溶液褪色。若将X通入足量双氧水中,X可全部被吸收且只得到一种强酸,再稀释到1000mL,测得溶液的PH=1。在溶液2中滴加KSCN溶液,溶液呈血红色。请回答:
(1)固体A的化学式______________。
(2)写出反应①的化学方程式____________。
(3)写出反应④中生成A的离子方程式______________。
【答案】FeSO42FeSO4![]() Fe2O3+SO2↑+SO3↑2Fe3++SO32-+H2O=2Fe2++SO42-+2H+
Fe2O3+SO2↑+SO3↑2Fe3++SO32-+H2O=2Fe2++SO42-+2H+
【解析】
本题考查无机物的推断以及实验方案设计。X由两种化合物组成,若将X通入品红溶液,溶液褪色,能使品红溶液褪色的有SO2,若将X通入足量双氧水中,X可全部被吸收且只得到一种强酸,根据化学反应SO2+H2O2 =H2SO4 、SO3+H2O =H2SO4可知,X由SO2 和SO3两种气体组成。在溶液2中滴加KSCN溶液,溶液呈红色,说明溶液中有Fe3+,红棕色固体是氧化铁。
(1)根据上述分析,固体A加热分解生成SO2、SO3和氧化铁,硫元素的化合价降低,铁元素的化合价升高,则A为FeSO4。
(2)根据上述分析,反应①的化学方程式为2FeSO4![]() Fe2O3+SO2↑+SO3↑ 。
Fe2O3+SO2↑+SO3↑ 。
(3)气体X为SO2、SO3的混合物气体,通入NaOH溶液中发生反应生成硫酸钠和亚硫酸钠,亚硫酸根离子具有还原性,氧化铁和硫酸反应生成硫酸铁,溶液2为硫酸铁,Fe3+具有氧化性,SO32-与Fe3+能发生氧化还原反应生成Fe2+和SO42-,根据得失电子守恒、电荷守恒和原子守恒配平,则反应④中生成A的离子方程式为2Fe3++SO32-+H2O=2Fe2++ SO42- + 2H+。


科目:高中化学 来源: 题型:
【题目】在一定条件下,将3 mol A和1 mol B两种气体混合于2L恒容密闭容器中,发生如下反应:3A(g) + B(g)![]() xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol.L-l。下列判断正确的是( )
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol.L-l。下列判断正确的是( )
A. A的转化率为40%
B. 2 min内B的反应速率为0.2 mol.L-l.min-1
C. x=2
D. 若混合气体的密度不变,则表明该反应已达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示:△H1=-393.5kJmol-1,△H2=-395.4kJmol-1,下列说法正确的是( )
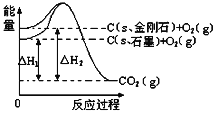
A. 石墨转化为金刚石是放热反应
B. 石墨和金刚石的相互转化是物理变化
C. 金刚石的稳定性强于石墨
D. 等质量的石墨与金刚石完全燃烧,金刚石放出的能量更多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是

A.N2(g)+3H2(g)=2NH3(l) ΔH=2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g)=2NH3(g) ΔH=2(b-a)kJ·mol-1
C.![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
D.![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据某种共性,可将CO2、SO2归为一类氧化物。下列物质中,也属于同类氧化物的是( )
A.CaCO3 B.SO3 C.CuO D.KMnO4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.金属氧化物不一定是碱性氧化物
B.HC1、H2S、NH3都是电解质
C.强酸强碱都是离子化合物
D.FeBr3、FeCl2、CuS都不能直接用化合反应制备
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的比较,结论正确的是
A. 溶解度:Na2CO3<NaHCO3
B. 热稳定性:HCl<PH3
C. 沸点:HCl<HBr
D. 碱性:LiOH<Be(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com