
�Կ��淴ӦN2��g��+3H2��g�� 2NH3��g������H=-92��4 kJ��mol��1������
2NH3��g������H=-92��4 kJ��mol��1������
����ȷ����
| A���ﵽ��ѧƽ��ʱ���������¶ȣ�������Ӧ���ʼ�С���淴Ӧ�������� |
| B������λʱ��������x mol N2��ͬʱ����2x mol NH3����Ӧ�ﵽƽ��״̬ |
| C�����ﵽƽ��ʱ�����ų�46��2kJ����������l mo1NH3��g������ |
| D���ﵽƽ������������СΪԭ����һ�룬���´ﵽƽ���c��NH3����Ϊԭƽ��ʱ��2�� |
 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
2SO2+O2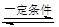 2SO3�ǹ�ҵ��������ķ�Ӧ�����й��ڸ÷�Ӧ��˵����ȷ����( )
2SO3�ǹ�ҵ��������ķ�Ӧ�����й��ڸ÷�Ӧ��˵����ȷ����( )
| A������O2��Ũ���ܼӿ췴Ӧ���� |
| B��������ϵ�¶��ܼӿ췴Ӧ���� |
| C��ʹ�ô�����Ӱ�췴Ӧ���� |
| D��һ�������´ﵽ��Ӧ��ʱSO2����ת��ΪSO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������KSCN��SCN-�ǡ���±���ӡ������������������ƣ���Һ�������Եĺ���Fe3+����Һ�У���Һ���Ѫ��ɫ�����ú�ɫ��Һ��Ϊ���ݣ���һ���м�������KMnO4��Һ����ɫ��ȥ��������һ����ͨ��SO2����ɫҲ��ȥ��
����˵������ȷ����
| A���ٺ�ɫ��ȥ��ԭ�������KMnO4��SCN-������ʹ[Fe��SCN��]2+��ʧ |
| B��[Fe��SCN��]2+��Fe3+��SCN-����λ����ϡ� |
| C���ں�ɫ��ȥ��ԭ����SO2����Ư���� |
| D��SCN-���ʵ������¿�ʧȥ���ӱ�����������Ϊ��SCN��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ͬ�¶��£��������ȵ����������ܱ������з������淴Ӧ��N2(g)+3H2(g)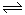 2NH3(g)��H=-92.4kJ/mol,ʵ������ʼ��ƽ��ʱ���й��������±���
2NH3(g)��H=-92.4kJ/mol,ʵ������ʼ��ƽ��ʱ���й��������±���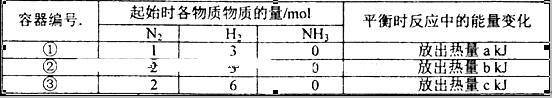
����������ȷ����
| A���ų�������ϵ��a<b <92.4 |
| B�����������ڷ�Ӧ��ƽ�ⳣ������>��>�� |
| C����ƽ��ʱ�����������������>�� |
| D��N2��ת���ʣ���>��>�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
CaCO3��ϡ���ᷴӦ�����ȷ�Ӧ������CO2�����뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ�����н��۲���ȷ����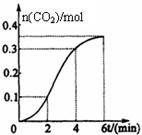
| A����Ӧ��ʼ2������ƽ����Ӧ������� |
| B����Ӧ4���Ӻ�ƽ����Ӧ������С |
| C����Ӧ��ʼ4�������¶ȶԷ�Ӧ���ʵ�Ӱ���Ũ�ȴ� |
| D����Ӧ4���Ӻ�Ӧ�����½���ԭ��������Ũ����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
4NH3���磩��5O2���磩 4NO���磩��6H2O���磩��10 L�ܱ������н��У�10s��ˮ���������ʵ���������0.60 mol����˷�Ӧ��ƽ�����ʦ�(X)(��Ӧ����������ʻ�������������)�ɱ�ʾΪ
4NO���磩��6H2O���磩��10 L�ܱ������н��У�10s��ˮ���������ʵ���������0.60 mol����˷�Ӧ��ƽ�����ʦ�(X)(��Ӧ����������ʻ�������������)�ɱ�ʾΪ
| A���ԣ�NH3����0.0060 mol/��L���� |
| B���ԣ�NO����0.0040 mol/��L���� |
| C���ԣ�O2����0.0060 mol/��L���� |
| D���ԣ�H2O����0.036 mol/(L��min) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��4 mol A�����2 mol B������2 L�������л�ϲ���һ�������·������·�Ӧ��2A(g)+B(g) 2C(g)������2 s����C��Ũ��Ϊ0.6 mol��L-1���������м���˵����
2C(g)������2 s����C��Ũ��Ϊ0.6 mol��L-1���������м���˵����
��������A��ʾ�ķ�Ӧƽ������Ϊ0.6 mol��L-1��s-1
��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.15mol��L-1��s-1
��2sʱ����A��ת����Ϊ30%
��2sʱ����B��Ũ��Ϊ0.3 mol��L-1
������ȷ����
| A���٢� | B���٢� | C���ڢ� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��Ӧ2CO��g��=2C��s��+O2��g���ġ�HΪ��ֵ����SΪ��ֵ�����H�͡�S�����¶ȶ��䣬����˵����ȷ����
| A�����������Է����� |
| B�����������Է����� |
| C�������²����Է����У����������Է����� |
| D���κ��¶��¶������Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ݻ�������ܱ������д������·�Ӧ��2SO2(g)��O2(g)  2SO3(g)��H��0��ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����
2SO3(g)��H��0��ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����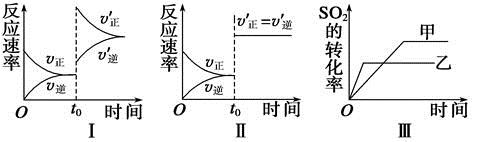
| A��ͼ���о�����t0ʱ������O2�����ʵ���Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� |
| B��ͼ���о�����t0ʱ��ͨ�뺤��������ϵѹǿ�Է�Ӧ���ʵ�Ӱ�� |
| C��ͼ���о����Ǵ����Ի�ѧƽ���Ӱ�죬�ҼĴ�Ч�ʱ��Ҹ� |
| D��ͼ���о������¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϸ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com