
【题目】铬、硼的合金及其化合物用途非常广泛。回答下列问题:
(1)基态Cr原子核外电子的排布式是[Ar] ___;基态硼原子中占据最高能级的电子云轮廓图为____形。
(2)铬的配合物有氯化三乙二胺合铬![]() 和三草酸合铬酸铵{(NH4)3[Cr(C2O4)3]}等。
和三草酸合铬酸铵{(NH4)3[Cr(C2O4)3]}等。
①配体en表示NH2CH2CH2NH2,其中碳原子的杂化方式是____。
②NH4+空间构型为____,与其键合方式相同且空间构型也相同的含硼阴离子是_____ 。
③C、N、O三种元素第一电离能由小到大的顺序为 ___;![]() 含有三个五元环,画出其结构:_______________。
含有三个五元环,画出其结构:_______________。
(3)硼酸[H3BO3或B(OH)3]为白色片状晶体,熔点为171℃。下列说法正确的是___填字母)。
A.硼酸分子中,∠OBO的键角为120° B.硼酸分子中存在σ键和π键
C.硼酸晶体中,片层内存在氢键 D.硼酸晶体中,片层间存在共价键
(4)2019年11月《EurekAlert》报道了铬基氮化物超导体,其晶胞结构如图所示:

由三种元素Pr(镨)、Cr、N构成的该化合物的化学式为 ___。
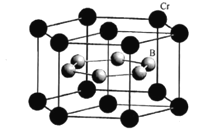
(5)CrB2的晶胞结构如图所示,六棱柱底边边长为acm,高为c cm,阿伏加德罗常数的值为NA,CrB2的密度为 ___gcm-3(列出计算式)。
【答案】3d54s1 哑铃(纺锤) sp3 正四面体 BH4- C<O<N 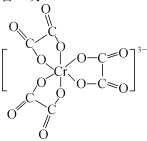 ABC Pr3Cr10N11
ABC Pr3Cr10N11 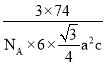 (或
(或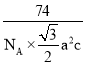 )
)
【解析】
(1)Cr为24号元素,基态Cr原子核外电子的排布式1s22s22p63s23p63d54s1,可表示为[Ar] 3d54s1;基态硼原子核外电子的排布式1s22s22p1,占据最高能级为2p,电子云轮廓图为哑铃(纺锤)型;
(2)①配体en表示NH2CH2CH2NH2,其中碳原子都是以单键连接,类似于甲烷中的碳原子键连方式,为sp3杂化;
②NH4+的中心原子为N,价层电子对数=4+![]() ×(5-1-1×4)=4,为sp3杂化,空间构型为正四面体型;互为等电子体的微粒,键合方式和空间构型相同,与NH4+互为等电子体的含硼阴离子为BH4-;
×(5-1-1×4)=4,为sp3杂化,空间构型为正四面体型;互为等电子体的微粒,键合方式和空间构型相同,与NH4+互为等电子体的含硼阴离子为BH4-;
③同周期元素从左到右电离能逐渐增大,处于全满、半满、全空状态处于稳定状态,比相邻元素电离能大;N原子最外层电子为半充满稳定状态,C、N、O三种元素第一电离能由小到大的顺序为C<O<N;![]() 含有三个五元环,Cr3+为配体,与C2O42-形成六个键,其结构为:
含有三个五元环,Cr3+为配体,与C2O42-形成六个键,其结构为: ;
;
(3)A.硼酸分子中心原子为B,B是sp2杂化,B和3个O共面形成平面三角形,则∠OBO的键角为120°,故A正确;
B.硼酸分子中每个硼原子最外层连有三个共价键,硼原子本身含有电子,故分子中硼原子最外层为6电子结构,形成离域π键,O原子与H原子以共价单键相连即含有σ键,故B正确;
C.硼酸是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连,故C正确;
D.硼酸晶体熔沸点较低,属于分子晶体,片层间是分子间作用力,故D错误;
答案选ABC;
(4)Pr6N9位于晶胞的棱上和体心,个数为12×![]() +1=4个,Cr8N13位于晶胞的顶点和面心,个数为8×
+1=4个,Cr8N13位于晶胞的顶点和面心,个数为8×![]() +6×
+6×![]() =4个,Cr6位于晶胞的体心,个数为8个,则一个晶胞中含有24个Pr、88个N和80个Cr,则分子式为Pr3Cr10N11;
=4个,Cr6位于晶胞的体心,个数为8个,则一个晶胞中含有24个Pr、88个N和80个Cr,则分子式为Pr3Cr10N11;
(5)Cr位于晶胞的顶点和上下面的面心,个数为12×![]() +2×
+2×![]() =3,B原子位于晶胞的体心,个数为6个,即一个晶胞中含有3个CrB2,底面积是6×
=3,B原子位于晶胞的体心,个数为6个,即一个晶胞中含有3个CrB2,底面积是6×![]() a2,高为c,则六棱柱的体积V=6×
a2,高为c,则六棱柱的体积V=6×![]() a2c,根据ρ=
a2c,根据ρ=![]() =
=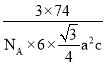 。
。


科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.12g石墨中含有σ键的物质的量为1.5mol
B.硫离子电子共有18种运动状态,且其2p与3p轨道形状和能量相等
C.电负性:C<N<O
D.I3+离子的几何构型是V型
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为______。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关。已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,E(H﹣Cl)=432kJ/mol,E(Cl﹣Cl)=243kJ/mol则E(H﹣H)=_____。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注.已知:2Cu(s)+ ![]() O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,C(s)+
O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,C(s)+ ![]() O2(g)═CO(g)△H=﹣110.5kJmol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJmol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____。
O2(g)═CO(g)△H=﹣110.5kJmol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJmol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____。
(4)如图是N2(g)和H2(g)反应生成2molNH3(g)过程中能量变化示意图:
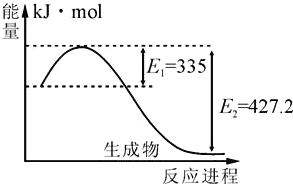
①请计算每生成1molNH3放出热量为:______。
②若起始时向容器内充入1molN2和3molH2达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨甲环酸(G),别名止血环酸,是一种已被广泛使用半个世纪的止血药,它的一种合成路线如下(部分反应条件和试剂略)。
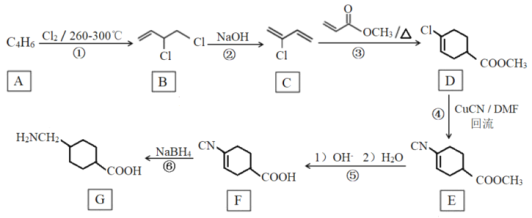
(1)A的名称是_________________。
(2)②的化学方程式是___________。
(3)③的反应类型是_____________。
(4)D中的官能团名称是_________。
(5)下列说法正确的是_____________(填字母序号)。
a.反应⑥是还原反应
b.F与![]() 互为同分异构体
互为同分异构体
c.G在碱性条件下可以转变成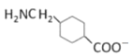
d.G在酸性条件下可以转变成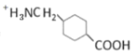
(6)写出满足以下条件的所有E的同分异构体的结构简式______________________。
a. 与硝基苯互为同系物 b.苯环上只有两个取代基 c.苯环上一氯代物有2种
(7)以CH3CH=CH2、HCHO为有机原料,选用必要的无机试剂合成上述流程中的A:CH3-CH=CH2![]() Br-CH2-CH=CH2→___________。已知:RX
Br-CH2-CH=CH2→___________。已知:RX![]() R—MgX
R—MgX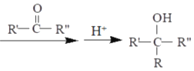 (R、R'、R〃代表烃基或氢)
(R、R'、R〃代表烃基或氢)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用该矿石制备BaCl22H2O的流程如图,且三次滤渣的主要成分各不相同:
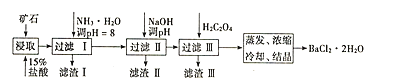
如表为常温时各离子转化为氢氧化物沉淀时的pH:
Fe3+ | Mg2+ | Ca2+ | |
开始沉淀时的pH | 1.9 | 9.1 | 11.9 |
完全沉淀时的pH | 3.2 | 11.1 | 13.9 |
(1)用15%盐酸浸取前需充分研磨,目的是______。
(2)滤渣Ⅰ的主要成分为______;加入NaOH调pH的范围为______;加入H2C2O4时应避免过量的原因是______。[已知难溶物质:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9]
(3)已知:25℃时,Ksp(BaCO3)=5.4×10-9,Ksp(CaCO3)=2.7×10-9。向CaCO3固体的溶液中加入高浓度的BaCl2溶液,有BaCO3沉淀生成,请写出该反应的离子方程式______,该反应的平衡常数K=______。
(4)取制得的BaCl22H2O(含少量杂质)2.5g配成100mL溶液,取10.00mL该溶液于烧杯中,加入足量(NH4)2C2O4溶液,过滤,洗涤,将得到的BaC2O4沉淀用过量稀硫酸溶液溶解,过滤除去BaSO4沉淀,将所得的H2C2O4溶液移入锥形瓶,用0.05mol/L高锰酸钾标准液滴定至终点。
已知:Ba2++C2O42-═BaC2O4↓
BaC2O4+2H++SO42-═BaSO4↓+H2C2O4
5H2C2O4+2MnO4-+16H+═10CO2↑+2Mn2++8H2O
①滴定中盛放高锰酸钾标准液的仪器为______,滴入最后一滴高锰酸钾溶液,锥形瓶中溶液颜色______,即说明达到滴定终点。
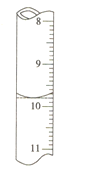
②若滴定前滴定管的读数为1.80mL,滴定终点时滴定管中液面如图,请计算BaCl22H2O的纯度为______(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.10molL-1的氨水滴定10.00mL0.05molL-1的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中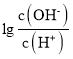 的关系如图所示。下列说法正确的是( )
的关系如图所示。下列说法正确的是( )

A.H2A的电离方程式为H2AH++HA-
B.B点溶液中,水电离出的氢离子浓度为1.0×10-6molL-1
C.C点溶液中,c(NH4+)+c(NH3H2O)=2c(A2-)
D.25℃时,氨水的电离平衡常数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1980年,古迪的夫发明了钴酸锂材料,这种材料的结构可以使锂离子在其中快速移动。以LiCoO2作电极材料的锂离子电池在充、放电时的微观粒子变化如图所示,下列说法正确的是
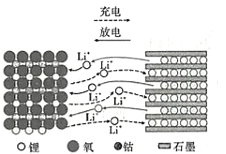
A.LiCoO2是电池的负极材料
B.充电时,LiCoO2电板的电势低于石墨电极
C.充电时,阳极发生的反应是LiCoO2+xe-=Li1-xCoO2+xLi+
D.放电时,当1mol电子转移,则石墨电极质量减少7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂的存在下可发生偶联反应,称为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应由苯A制备化合物E的一种合成路线:


回答下列问题:
(1)B的结构简式为________,D的化学名称为________。
(2)①和③的反应类型分别为________、________。
(3)E的结构简式为____________________。1 mol E与氢气反应,理论上最多消耗氢气________ mol。
(4)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3∶1,则符合条件的同分异构体有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下H2A的K1=1.0×10-4,K2=5.0×10-7。向20mLlmol·L-1的H2A溶液中逐滴滴入2mol·L-1的NaOH溶液,溶液中水电离出的c水(OH-)随加入NaOH溶液的体积V的变化如图所示,下列分析正确的是( )
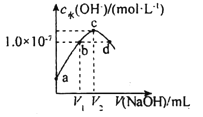
A.V1<10,V2=20
B.a点溶液的pH=3
C.c点溶液c水(H+)≈1.0×10-4mol·L-1
D.b、d点溶液均呈中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com